Сформированный мочевой пузырь из кишки
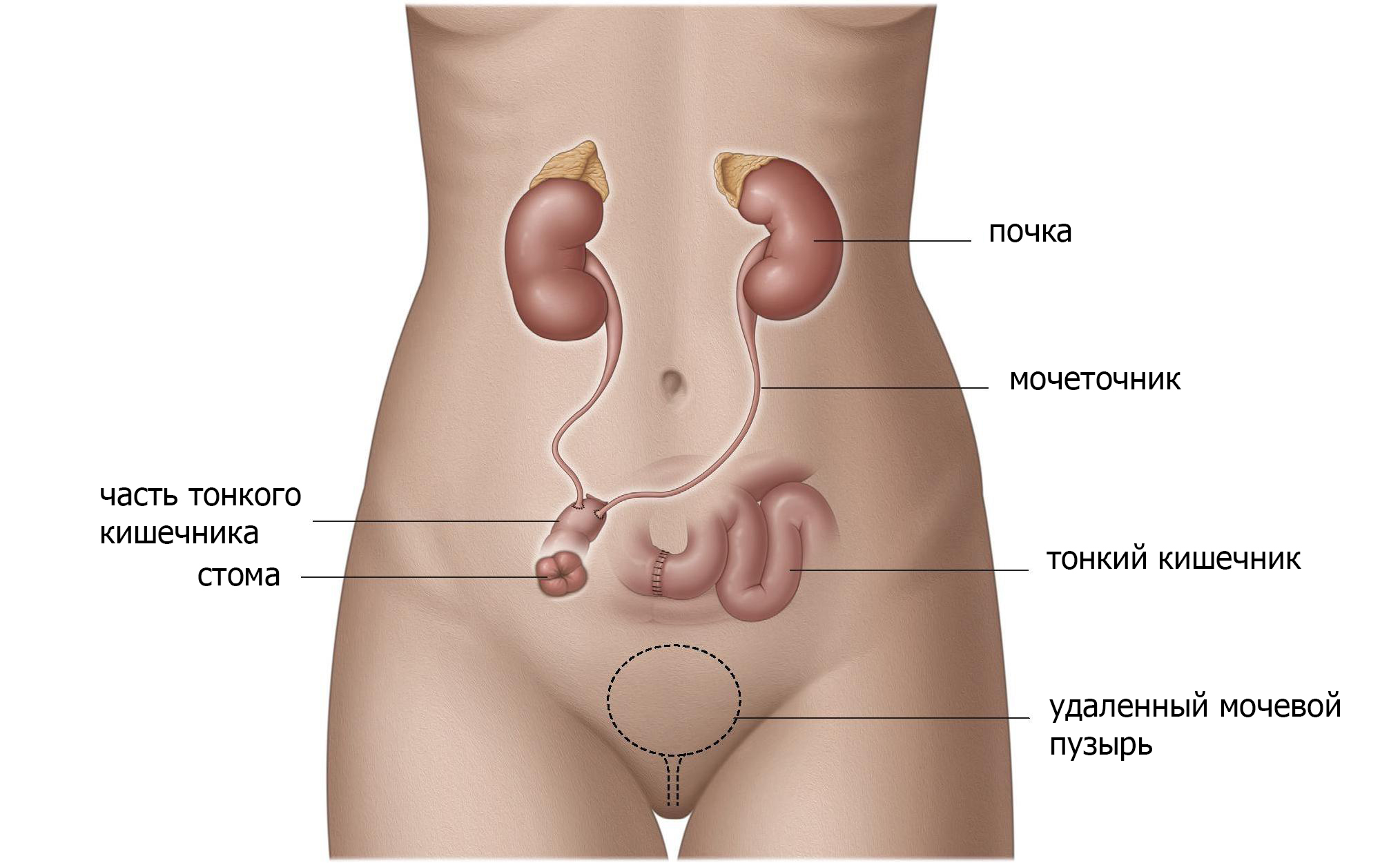
Основное лечение мышечно-инвазивного рака мочевого пузыря является хирургическое удаление мочевого пузыря.
Причины при которых может рекомендоваться удаление всего пузыря:
- Наличие мышечно-инвазивной опухоли
- Наличие опухоли, которая агрессивно растет, которая имеет множественные злокачественные очаги (мультифокальная) или поверхностная, но имеет рецидивы после химиотерапии или иммунотерапии
- Наличие постоянных болей и кровотечения у пациентов с неизлечимым заболеванием.
Оценить риск удаления мочевого пузыря, можно путем прохождения медицинской комиссии в составе (например, уролог, онколог, хирург, анестезиолог, терапевт).
Важны также такие факторы, как ваш биологический возраст (общесоматическое состояние, ваше самочувствие, измеряемое как состояние работоспособности или ожидаемая продолжительность жизни) и другие заболевания, которые у вас имеются (диабет, сердечные заболевания, гипертоническая болезнь и т.д.). Пациенты старше 80 лет труднее переносят такие операции и имеют более длительный восстановительный период.
Ранние операции на брюшной полости или лучевая терапия затрудняют хирургическое вмешательство, но редко являются причиной отказа от хирургического вмешательства. Избыточный вес не влияет на выживание после операции, но влияет на риск осложнений в послеоперационном периоде.
Удаление мочевого пузыря включает удаление мочевого пузыря, нижний отдел мочеточников и тазовых лимфатических узлов. В зависимости от таких факторов, как расположение опухоли и метод дальнейшего отведения мочи, часть прилежащих половых органов (простата и семенные пузырьки у мужчин, вся уретра, матка у женщин) удаляются.
Как проводится удаление мочевого пузыря?
Удаление мочевого пузыря осуществляется через разрез в брюшной полости (открытый) пациент под общей анестезией (сочетание внутривенных препаратов и ингаляционных газов). Мочевой пузырь, нижний отдел мочеточников, расположенные близко к мочевому пузырю, тазовые лимфатические узлы и (часть) прилежащих половые органы удаляются. Теперь должен быть сформирован другой метод хранения и отведения мочи.
Стандартная методика на данный момент – открытая хирургия. Тем не менее, это может быть сделано менее инвазивно (лапароскопическая или роботизированная хирургия). В настоящее время в специализированных центрах, имеющих специальное оборудование и опытных специалистов, малоинвазивные операции считаются методом выбора для удаления мочевого пузыря.
Как подготовиться к процедуре?
При поступлении в стационар врач информирует вас о том, как нужно готовиться до и что делать после операции.
Часть вашей кишки будет использоваться для создания мочевого резервуара. Врач подробно объяснит, как подготовиться к данной процедуре.
Перед операцией врач подробно проинформирует вас о том, как подготовиться к анестезии. Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу. Возможно, потребуется отмена некоторых препаратов за несколько дней до операции.
В течение первых нескольких дней вы находитесь под динамическим наблюдением. Врач подробно проинформирует вас о послеоперационном периоде.
Во время госпитализации вы узнаете, как обращаться с уростомой. После того, как вы научитесь использовать и опорожнять уростому, будет установлена дата выписки.
Химиотерапия перед удалением мочевого пузыря
Химиотерапию проводят перед удалением мочевого пузыря, чтобы потенциально уменьшить опухоль и убить опухолевые клетки, которые уже проникли в кровь или лимфатические узлы.
Химиотерапию перед операцией можно рекомендовать пациентам с мышечно-инвазивной формой. Это также необходимо, при опухолях большого размера (> 3 см) или если есть признаки распространения рака на лимфатические узлы (метастазы). Решение о проведении химиотерапии принимается врачебной комиссией (включая онколога, уролога и радиолога). Необходима адекватная функция почек.
Положительная реакция на химиотерапию улучшает выживаемость, но не исключает необходимость хирургического вмешательства.
Химиотерапия после удаления мочевого пузыря
Если опухоль большая (> 3 см), не может быть полностью удалена или распространяется на лимфатические узлы (определяется патологоанатомом), показана химиотерапия после удаления мочевого пузыря. Рак, который распространился на лимфатические узлы, указывает на системное заболевание и может потребоваться системное лечение (с химиотерапией) в определенных случаях.
Отведение мочи: недержание или удержание.
Важно понять двухэтапный подход к удалению мочевого пузыря. Сначала удаляют мочевой пузырь и лимфатические узлы. Затем, мочу нужно отвести. Это может быть достигнуто несколькими способами. Вообще мы различаем варианты, которые являются недержанием (непрерывный поток мочи сразу выходит за пределы тела), и удержание (моча, хранится в организме и отводится при необходимости). Биологический возраст, функция почек и другие заболевания, качество жизни пациента имеют решающее значение при выборе тактики операции. Чтобы определиться, какой вариант лучше подходит в вашей конкретной ситуации, вы должны знать и понимать ограничения после каждого вида операции и побочные эффекты.
В дополнение к вашим личным предпочтениям важна способность физически и морально привыкнуть, и уметь обращаться с таким отведением мочи.
Перемещение мочеточников
Выведение мочеточников через кожу (уретерокутанеостомия).
Перемещая мочеточники или вместе или отдельно через кожу сбоку живота для отведения мочи от почек (стома) (рис.1), моча может просто вытекать через стому в мешок. Это отведение мочи является самым простым. Хотя он редко используется. Данный метод безопасен и доступен для пациентов, с отягощенным анамнезом (предшествующие операции, множественные проблемы со здоровьем, паллиативный уход) или у пациентов, которые не могут позаботиться о себе после операции. Основные осложнения встречаются редко, однако рецидивирующие инфекции и затягивание отверстия (стеноз) являются общими и могут потребовать лечения. Пациентам часто необходимо стентирование мочеточника, который необходимо регулярно менять.
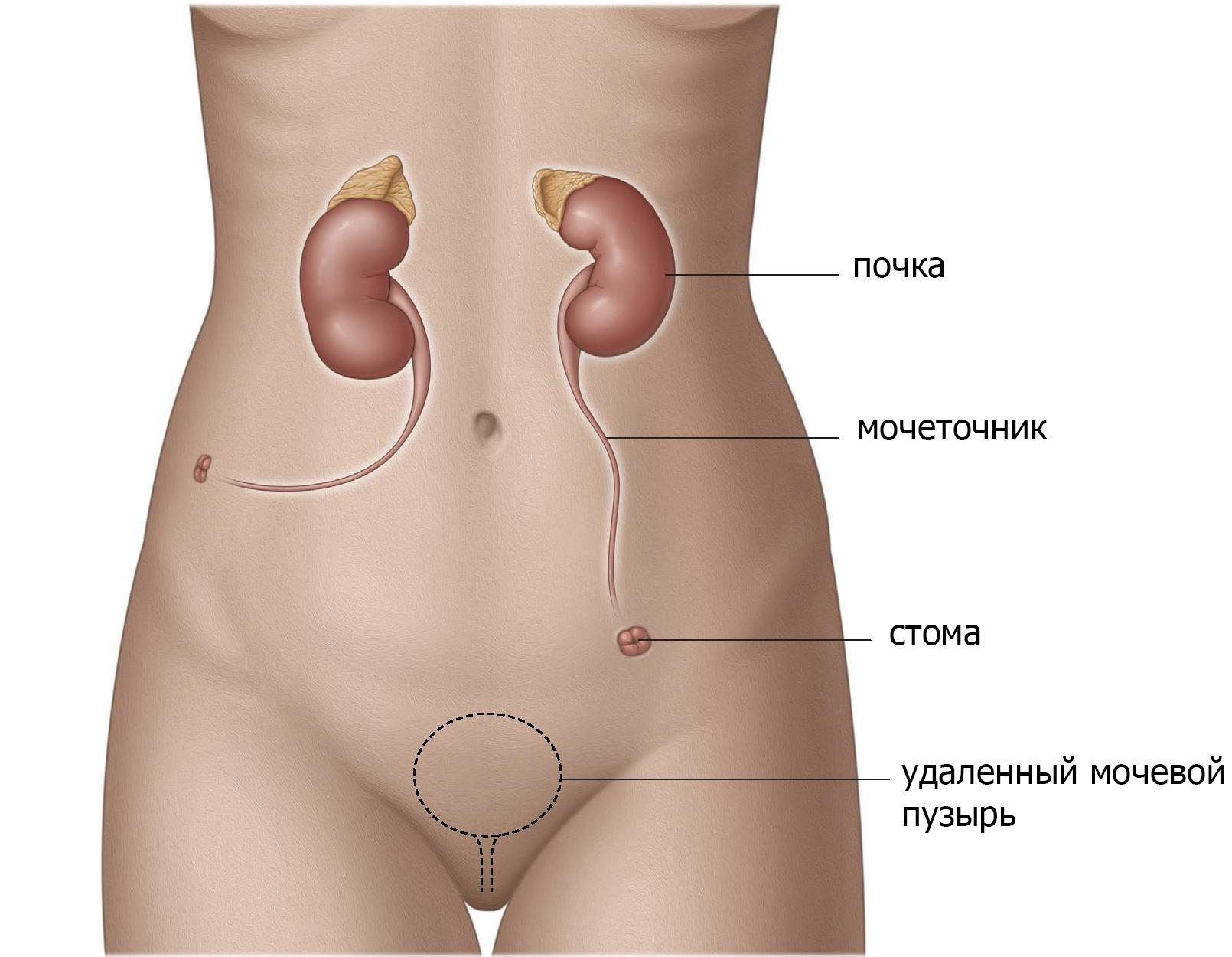
Рис. 1 уретерокутанеостома
Установить часть тонкой кишки между мочеточниками и кожей (подвздошный канал).
Подвздошный канал можно создать, поместив тонкую кишку между мочеточниками и кожей (рис.2). Эта «кишечная стома» создает большее расстояние между почками и кожей и снижает риск инфицирования. Другим преимуществом для пациентов является то, что эта стома легче обрабатывается и имеет меньше осложнений, таких как сужение выводного отверстия (стеноз). Данная операция технически относительно проста и надежна и поэтому является наиболее часто используемой.

Рис. 2 Подвздошный канал
Выбирая данный вид отведения мочи, вы должны знать, что привыкнуть к жизни со стомой требует много времени и усилий.
Вновь сформированный мочевой пузырь. Создание резервуара внутри тела
Используя тонкую кишку или толстую кишку, а иногда и аппендикс, создается резервуар в брюшной полости, а затем соединяется с кожей с помощью клапанного механизма (рис. 3). С таким резервуаром низкого давления, моча может быть сохранена в теле. Цель этой процедуры – позволить контролировать опорожнение или обратный поток мочи в почки (рефлюкс). Резервуар опорожняется прерывистой катетеризацией небольшим пластиковым катетером каждые 2-6 часов. Отверстие может находиться где угодно на нижней части живота или в пупке.
Если выбран данный вид операции, вам потребуется регулярно катетеризировать и опорожнять данный резервуар. Функция печени и почек должна быть адекватной из-за реабсорбции мочевых компонентов (соли, мочевой кислоты, воды) в кишечной оболочке резервуара, что вызывает дополнительную нагрузку на эти органы.
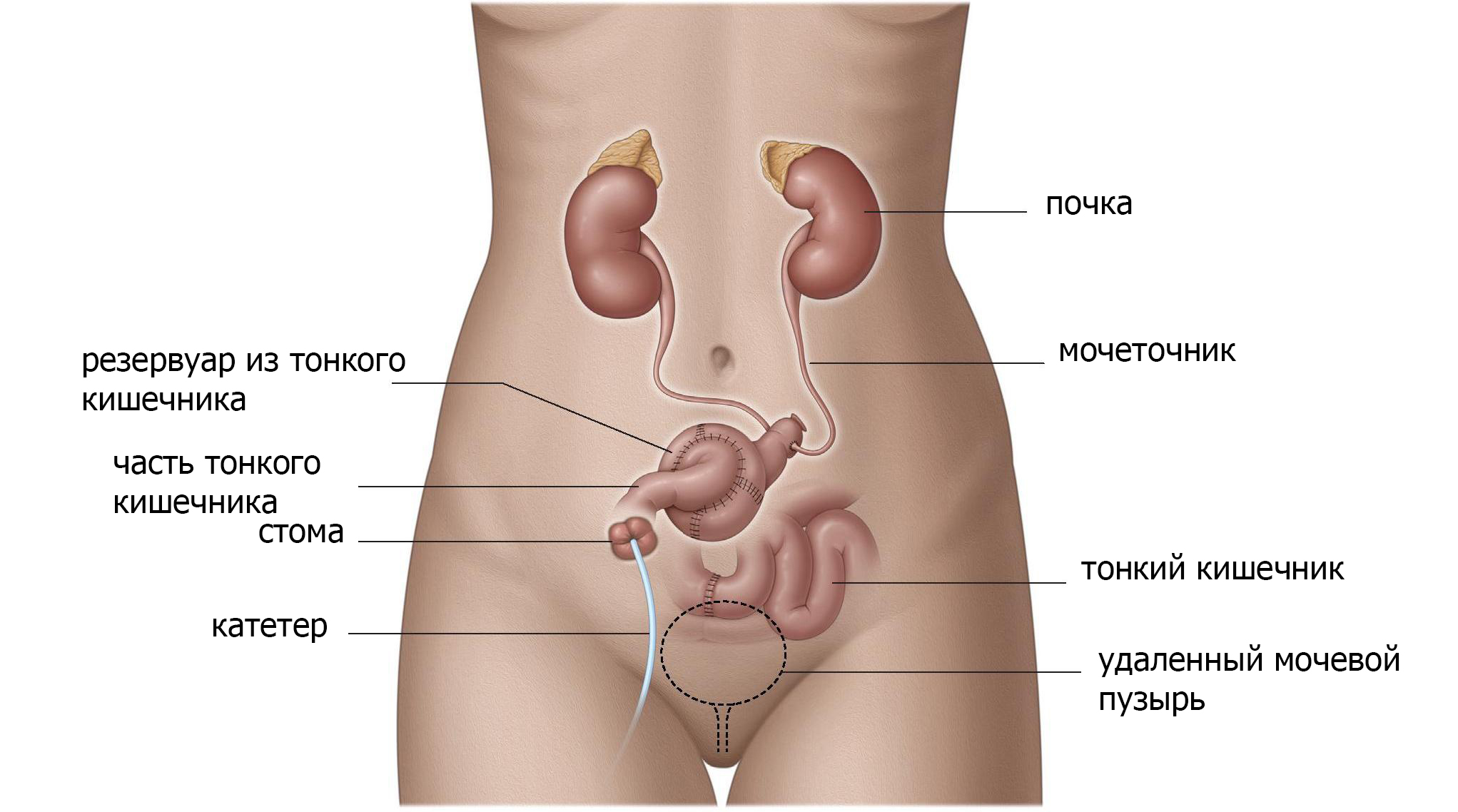
Рис. 3 Резервуар из кишечника
Осложнения включают инфекции, недержание мочи, грыжу, рефлюкс, затягивание отверстия (стеноз), а также синдром короткой кишки, метаболический и электролитный дисбаланс.
Поскольку эта операция имеет технические сложности, особенно при создание клапанного механизма, который не всегда бывает удачным, данный метод используется редко.
Имплантация мочеточников в прямую кишку (уретероректонеостомия)
Когда мочеточники имплантируют в прямую кишку, моча хранится в ампуле прямой кишки (рис.4). Анальное отверстие и тазовое дно становятся органом удерживающим мочу и должны функционировать должным образом. Данный вид отведения приводит к смешиванию фекалий с мочой, поэтому опорожнение и дефекация происходят одновременно. Этот метод имеет высокий уровень инфецирования, поэтому используется редко и только при определенных обстоятельствах. Краткосрочные осложнения включают повторяющиеся инфекции (включая воспаление брюшной стенки и почек), затягивание отверстия в прямой кишке (стеноз). Долгосрочные осложнения включают недержание мочи, раздражение кишечника и связанный с этим рак толстой кишки.
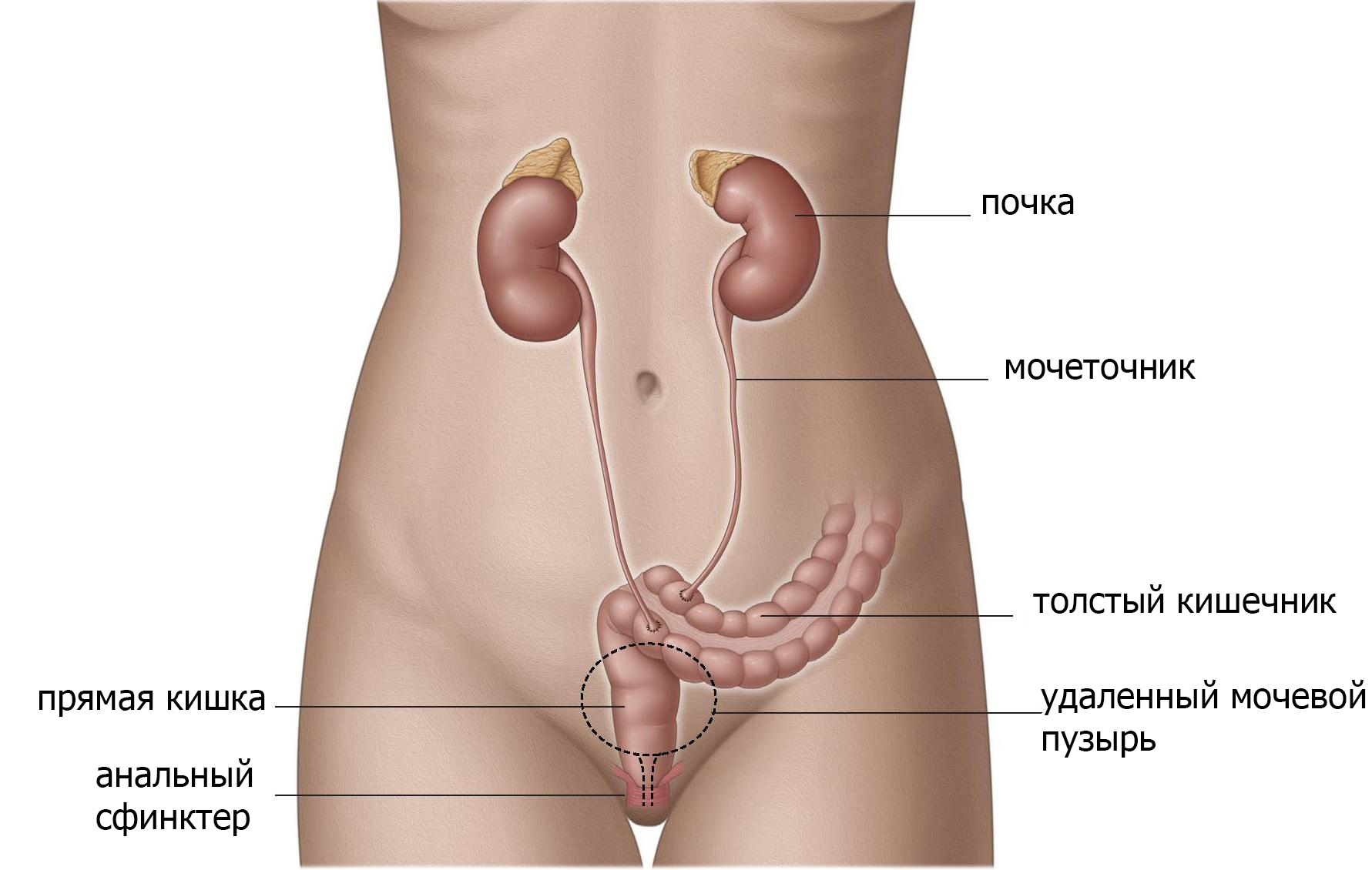
Рис. 4 Уретероректонеостома
Формирование мочевого пузыря из тонкой кишки
Новый мочевой пузырь может быть сформирован из тонкой кишки, которая изолируется от пищеварительного тракта (рис.5). Резервуар сформирован из тонкого кишечника и помещен в малый таз в качестве замены мочевого пузыря. В зависимости от используемой методики резервуар имеет сфероидальную форму, «W» или «V». Мочеточники прикреплены с обеих сторон, а нижний конец соединен с уретрой. Мочевой сфинктер сохраняется. При данный виде операции моча должна накапливаться а затем выводиться наружу как и при здоровом мочевом пузуре.
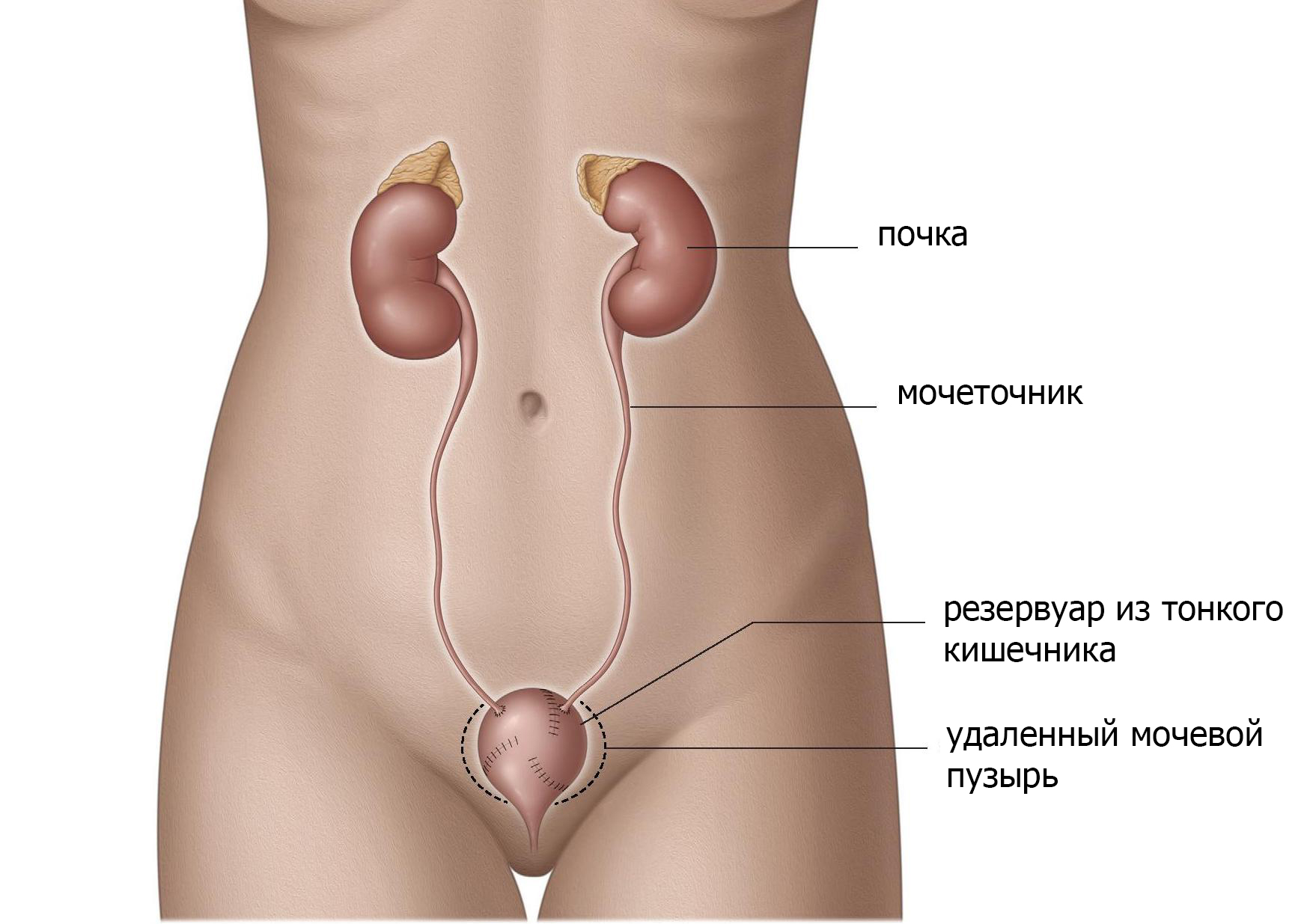
Рис. 5 мочевой пузырь из тонкой кишки
Вы не почувствуете наполнения мочевого пузыря или позыв к мочеиспусканию с пузырем из тонкого кишечника, поэтому опорожнение необходимо проводить каждые 2-4 часа. Пузырь освобождается, расслабляя мышцы тазового дна и сокращая брюшную полость (метод Вальсальвы). Нажатие на живот обеими руками может помочь для полного опорожнения. У 20% женщин необходимо выполнять периодическую самокатетеризацию для полного опорожнения, у мужчин этого не требуется.
При данном виде операции требуется удовлетворительная функция почек и печени, нормальное состояние мышц тазового дна. Осложнения после данного вмешательства включают в себя повторяющиеся инфекции (включая воспаление брюшной стенки и почек) и недержание мочи.
Долгосрочные осложнения включают затягивание отверстия в области анастамоза, изменения верхних мочевых путей, недержание мочи, синдром короткой кишки и грыжу, а также метаболический и электролитный дисбаланс.
Регулярный анализ крови поможет оценить количество мочевой кислоты которая реабсорбируется используемым участком кишечника, вызывая дисбаланс pH, который часто требует медикаментозного лечения пероральными препаратами (бикарбонат натрия – пищевая сода).
Для вновь образованного резервуара требуется время для его укрепления и начала работы. Для увеличить емкость сформированного пузыря, вам нужно будет его тренировать. Врач предоставит вам инструкции по тренировке мочевого пузыря. В начале недержание мочи может случиться из-за послеоперационного отека тазового дна.
Источник
Эндо-урологический центр клиники «Мемориал-Шишли» – один из 15 центров в мире, где практикуют уникальную операцию – создание нового мочевого пузыря из кишки пациента взамен удаленного при онкозаболевании. Все манипуляции во время вмешательства хирурги проводят с помощью робота Да-Винчи. Благодаря использованию передовых технологий рак мочевого пузыря – теперь только диагноз. Роботизированная хирургия дает шанс на нормальную жизнь.
Специалисты госпиталя «Мемориал-Шишли» выполнят любое из известных сложнейших урологических хирургических вмешательств. Клиника работает по мировым стандартам – имеет сертификат аккредитации JCI (Joint Commission International).
Лечение рака мочевого пузыря на новом уровне
Рак мочевого пузыря – заболевание распространенное. Примерно каждому четвертому онкобольному ставят такой диагноз. Причем у мужчин рак мочевого пузыря встречается в 4-5 раз чаще, чем у женщин. Традиционное лечение для таких пациентов – удаление мочевого пузыря (цистэктомия). Радикальная цистэктомия предусматривает не только удаление самого органа, но и простаты с семенными пузырьками, если рак мочевого пузыря у мужчин, или матки с яичниками и маточными трубами – у женщин.
Обычно при таких операциях вынужденная мера – удаление еще и проксимального (располагающегося после мочевого пузыря) отдела уретры и тазовых лимфоузлов с обеих сторон. В результате для поддержания жизнедеятельности пациенту вынуждены вывести мочеточник на кожу или в кишечник. Это в дальнейшем создаст ему проблемы по поддержанию гигиены и значительно увеличит риск заболеваний почек. Но есть другой вид операций – малоинвазивное хирургическое вмешательство. Его в совершенстве практикуют специалисты клиники «Мемориал-Шишли» в Стамбуле.
Уро-хирурги клиники искусно проводят необходимые удаления в мочевыводящей системе пациента через небольшое отверстие (примерно 5-10 мм) с помощью робота Да-Винчи. И таким же малоинвазивным путем из фрагмента тонкой кишки создают новый мочевой пузырь.
Уникальность операции в том, что все манипуляции проводятся с минимальным травматизмом. Пациент буквально через 3-5 дней после хирургического вмешательства может выписываться из госпиталя под домашнее наблюдение. Кроме того, в дальнейшем ему обеспечен обычный образ жизни – он будет купаться, загорать, заниматься спортом, а рак мочевого пузыря останется в прошлом.
Уро-онкологи госпиталя во главе с профессором, доктором медицины Дерья Балбай и группа операторов робота Да-Винчи клиники «Мемориал-Шишли» считаются наиболее опытной командой не только в Турции, но и в Европе.
Дерья БАЛБАЙ, профессор, доктор медицины. С 1996 – 1999 гг. работал в Онкологическом Центре Андерсона (г. Хьюстон, США). С 2010 г. по сегодняшний день преподает курс роботизированной хирургии на хирургических системах Да-Винчи в одном из институтов Калифорнии (США). И параллельно оперирует в госпитале Мемориал-Шишли (г. Стамбул, Турция).
Инновационное урологическое лечение в «Мемориал-Шишли»
Врачи клиники освоили самые новейшие хирургические вмешательства. Стоит отметить, что это первая клиника в Турции, участник AHA (Американской больничной ассоциации). И в настоящее время клиника принимает пациентов более, чем из 90 стран. Вот перечень самых современных применяемых методик, которыми поделилась клиника с журналом DoctorGEO.
Лазерная литотрипсия. Метод соединяет в себе эндоскопический способ лечения камней почек и лазеротерапию. Эндоскоп проводят через уретру и мочеточник к камню. После этого активируется лазер, который «выпаривает» камень, не оставляя мелких фрагментов. Операция характеризуется отсутствием осложнений, кровотечения и эффективна при любых типах камней.
Лапароскопическая или роботизированная простатэктомия. Или удаление простаты. Данный метод предполагает выполнение врачом 3-4 проколов на брюшной стенке, в которые вводится камера, осветительный прибор и хирургические инструменты. За ходом операции хирург наблюдает по монитору, куда выводится изображение из камеры, находящейся в брюшной полости. Метод позволяет удалить простату и оставить неповрежденными нервные сплетения.
Лимфаденэктомия при раке простаты. Это удаление тазовых лимфоузлов. Операция необходима, если раковые метастазы поразили тазовые узлы. Она может проводиться, как открыто, так и лапароскопически.
Процедуры по имплантации протезов. Это могут быть: протезирование пениса (имплантат позволит выпрямить искривление полового члена); тестикулярное протезирование (помещение в полость мошонки протеза, в связи с отсутствием яичка); искусственная уринальная имплантация сфинктера (избавляет от недержания мочи).
Лапароскопическая или роботизированная радикальная или частичная нефрэктомия. Это оперативное вмешательство, проводимое с целью удаления почки.
Лапароскопическая или роботизированная адреналектомия. Это хирургическое удаление надпочечников.
Лечение кишечника и мочевого пузыря с помощью системы InterStim. Она основана на стимуляции сакральных (крестцовых) нервов с помощью имплантированного нейростимулятора. Он передает электрические импульсы, восстанавливая функции наружного сфинктера прямой кишки, мочевого пузыря и кишечника, избавляя человека от недержания мочи и кала.
Кроме того, в клинике успешно проводят открытые и роботизированные кольпосуспензии (подшивание стенок влагалища) для лечения выпадения, а также ТVT и или TOT процедуры для лечения сложнопрогнозируемых недержаний мочи у женщин.
Педиатрические урологические хирургические вмешательства при врожденных пороках. Иногда мальчики рождаются с неопущением яичек, когда они располагаются не в мошонке, а в брюшной полости или паху. Этот порок называется орхопексия и хирурги клиники «Мемориал – Шишли» успешно восстанавливают мужское здоровьеи такому ребенку.
Например, вертикальная эписпадио-экстрофия – это хирургическое формирование (пластика) мочевого пузыря и мочевыводящей системы у новорожденного, родившегося с пороком этого органа. И хирургическое лечение патологии, при которой расщеплены мочеиспускательный канал и головка члена (у мальчиков) или не сформирована уретра (у девочек). Также успешно оперируют у детей такой порок развития, как гипоспадия. В этом случае у новорожденного наружное отверстие мочеиспускательного канала находится не на своем естественном месте, а сбоку или сверху, в мошонке или даже в промежности.
Лечения почечного рака с использованием сердечной и кавальной тромбэктомии с кардиопульмональным шунтированием или резекцией одной почки.
Такое сложное для понимания обычных людей сочетание слов объясняется так: рак почек часто осложняется развитием опухолевого тромба, который распространяется по просвету почечной вены вплоть до правых отделов сердца. Раньше это было противопоказанием для хирургического вмешательства, но хирурги клиники «Мемориал-Шишли», благодаря современным технологиям, успешно проводят операции на почках и в таких случаях. А применение кардиопульмонального шунтирования значительно снижает риск эмболических осложнений.
| Лечение в клинике «Мемориал», Турция: Любые вопросы можно решить, если обратиться к русскоговорящему менеджеру: Мадина Мирзаева, Тел.: +90 549 314 69 51 madina.mirzaeva@memorial.com.tr |
Post Views: 2 007
Источник
Перепечай В. А.2 , Коган М.И.1 , Васильев О.Н.1
1 Кафедра урологии и репродуктивного здоровья человека с курсом детской урологии-андрологии ГБОУ ВПО РостГМУ Минздрава России, г.Ростов-на-Дону
2 Клиническая больница №1, ФГУ «Южный окружной медицинский центр ФМБА России», г.Ростов-на-Дону Адрес: 344022, г. Ростов-на-Дону, пер. Нахичеванский, 29, тел. (863)2014448 Эл.почта: perepechay_va@mail.ru, dept_kogan@mail.ru, vasilyev_on@mail.ru
Введение
Радикальная цистэктомия (РЦЭ) является стандартным методом лечения инвазивного и немышечноинвазивного рака мочевого пузыря высокого риска рецидива и прогрессии. РЦЭ в настоящее время не рассматривается как инвалидизирующая операция, сопряженная с высоким риском летальности, тяжелыми послеоперационными осложнениями и последующим неблагоприятным прогнозом в отношении продолжительности жизни больных. Этого удалось достигнуть благодаря усовершенствованию техники РЦЭ и разработке новых, более надежных методов послеоперационного отведения мочи. К настоящему времени разработаны разнообразные виды деривации мочи после РЦЭ, однако ортотопическая неоцистопластика лучше всего моделирует врожденный мочевой пузырь, обеспечивая адекватную емкость созданного резервуара, функцию его опорожнения и лучшее качество жизни пациентов. Ортотопическое замещение мочевого пузыря является стандартной формой после РЦЭ при отсутствии противопоказаний. Многочисленные исследования показывают безопасность и отдаленную надежность данного вида деривации мочи, а также преимущества перед инконтинентными методиками. Создание ортотопического резервуара с достаточной емкостью, низким внутрипросветным давлением и адекватной защитой верхних мочевых путей позволяет достичь максимальной медицинской и социальной реабилитации больных, подвергнутых РЦЭ. Основным условием полноценной социальной и психологической реабилитации пациентов сегодня следует считать восстановление самостоятельного мочеиспускания. Учитывая данный факт, при возможности выполнения ортотопического замещения мочевого пузыря, его следует предпочесть другим способам деривации мочи. Для ортотопической реконструкции мочевого пузыря используются сегменты подвздошной кишки, восходящей, поперечной, нисходящей, сигмовидной толстых кишок, сочетание этих сегментов, реже – стенка желудка, кожно-мышечные лоскуты. В середине 90-х годов ортотопическое замещение мочевого пузыря в большинстве медицинских центров мира стало стандартным методом реконструкции, а у 90% больных используется с этой целью ортотопический мочевой пузырь из подвздошной кишки (Moutie J.F. 1997 г., Studer R.E. et al. 1998 г., Hautmann R.E. et al 1999, 2001 гг.).
Описывается несколько методик ортотопической кишечной цистопластики в различных модификациях, однако широко применяемыми являются методики Camey II, Hemi Kock, Hautmann и Studer. Данные методики имеют минимальные различия по функциональным результатам, при наличии как преимуществ, так и своих недостатков (таблица 1). По континентности и адекватности опорожнения имеет место закономерная дневная и ночная вариабельность. Удержание мочи улучшается на протяжении 3 лет после ортотопической деривации мочи, результатом чего является дневное удержание у 90% пациентов, ночное – у 70-85 % соответственно [8].
Таблица 1. Результаты различных методик ортотопической энтероцистопластики
| Camey I [1] | Camey I [2,3] | Hautmann И1 | Hemi-Kock [4, 5, 6, 7] | Studer [41 | |
|---|---|---|---|---|---|
| Дневное удержание | 20-80% | 96% | 83,70% | 85-87% | 92% |
| Ночное удержание | 0-80% | 78% | 66% | 75-94% | 80% |
| Рефлюкс в верхние мочевые пути | 15% | 15% | 3,30% | 17% | – |
| Максимальное давление в резервуаре | 43 см Н20 | 32 cm Н20 | 30 см Н20 | <40 см Н20 | 20-30 см Н20 |
| Ранние п/операционные осложнения | – | 12% | 15% | 17,80% | 11% |
| Поздние п/операционные осложнения | – | 24% | 23% | 15,70% | 18% |
| Средняя емкость неоциста | – | – | 433 мл | 709 мл | 450-500 мл |
В настоящее время необходимо выбирать метод деривации мочи с наименьшим количеством ранних и отдаленных осложнений и обеспечением наилучшего качества жизни больного после операции [9]. Большинство исследований за последние десять лет показывает на предпочтение при выборе метода ортотопической илеоцистопластики – операции по Studer. Однако результаты этой и других методик тонкокишечной ортотопической реконструкции значительно хуже при интраоперационно выявленной короткой брыжейке тонкой кишки, которая обусловливает натяжение тканей по линии уретрорезервуароанастомоза, что препятствует безопасному выполнению ортотопической операции и вынуждает хирурга прибегать к альтернативным вариантам кишечной деривации мочи. Таким образом, к одному из недостатков тонкой кишки относят ограниченные возможности применительно к ортотопической цистопластике из-за того, что у ряда пациентов оказываются короткими сосуды брыжейки для беспрепятственного низведения сегмента подвздошной кишки в малый таз и наложения анастомоза между кишечным мочевым пузырем и уретрой без натяжения [10]. В связи с этим известно, что одним из характерных осложнений среди прочих является несостоятельность резервуароуретрального анастомоза при всех известных и наиболее применяемых методиках ортотопической илеоцистопластики. Даже минимальное натяжение в зоне анастомоза между кишечным резервуаром и уретрой остается серьезной проблемой и является основной причиной несостоятельности анастомоза с формированием мочевых затеков, перитонита, сепсиса, кишечной непроходимости, мочевых свищей с необходимостью повторных операций.
Это заставляет хирурга в случае имеющегося натяжения в анастомозе менять интраоперационно план реконструкции, отказываться от ортотопической операции, прибегать к другим, более сложным ее вариантам (гетеротопической, кондуитной, отведению в непрерывный кишечник и др.), которые с позиции качества жизни оказываются заведомо хуже в сравнении с ортотопической деривацией, либо выполнять дополнительные резекции кишечника и т.п. Это неоправданно затягивает время операции, увеличивает ее стоимость и объем хирургической травмы, число послеоперационных койко-дней, риск осложнений и летальности.
Хирургами предпринимаются всевозможные способы ликвидации натяжения тканей в зоне уретро-резервуароанастомоза, либо, если это не удается, ортотопическая цистопластика не выполняется, что значительно ухудшает непосредственные и отдаленные результаты, а также значимо снижает качество жизни больных. В связи с этим становится очевидной необходимость создания простого, не требующего дополнительных затрат, не увеличивающего времени операции и объема хирургической травмы метода, позволяющего безопасно выполнить ортотопическую тонкокишечную реконструкцию мочевого пузыря в условиях недостаточной длины брыжейки тонкой кишки.
Материалы и методы
Анализированы результаты лечения 326 пациентов, подвергнутых радикальной цистэктомии при раке мочевого пузыря в период с 1995 по 2012 гг. Среди всех видов реконструктивной субституции мочевого пузыря чаще выполняли ортотопическую интестиноцистопластику в различных вариантах – 152 (41,3%) пациентов. При наличии противопоказаний к ортотопической реконструкции (в том числе при выявлении короткой тонколибо толстокишечной брыжейки, препятствующей ортотопической цистопластике) у 38 (10,3%) пациентов выполнили гетеротопическую континентную пластику, а у 27 (7,3%) и 53 (14,4%) – внутреннюю деривацию мочи в кишечник и наружную неконтинентную деривацию в различных вариантах соответственно. Ортотопическая интестиноцистопластика по Studer выполнена 69 (18,7%) больным, из них короткая брыжейка тонкой кишки была у 48 (69,6%). Данные пациенты были ретроспективно разделены на две группы для проведения сравнительного анализа. Критерием групповой дифференциации явилась интраоперационная оценка допустимости натяжения тканей в формируемом уретрорезервуароанастомозе, которую проводили в соответствии с общепринятыми рекомендациями: при помощи пинцета и незначительной тракции, заранее определенную зависимую точку резервуара (место предполагаемого наложение анастомоза со стороны резервуара) низводили к культе уретры. В некоторых случаях дополнительно мобилизовали выделенный сегмент кишки путе м рассечения серозы над сосудистыми аркадами брыжейки [11]. В случае адекватного сопоставления краев культи уретры и стенки резервуара выполняли их анастомозирование (I группа, 15 (31,3%) пациентов). При невозможности сопоставления краев культи уретры и стенки резервуара без значимого натяжения, применяли модификацию методики Studer – оригинальную инвертирующую ортотопическую илеоцистопластику (II группа, 33 (68,7%) пациентов).
Предложенный метод операции [12], примененный нами во II группе, направлен на предотвращение натяжения тканей в зоне резервуаро-уретрального анастомоза путем продольного, а не поперечного сшивания резервуара и его инвертирующего позиционирования в малом тазу для максимального приближения стенки резервуара к культе уретры и выполнения уретро-резервуарного анастомоза без натяжения.
Технические отличия сводятся к тому, что резецируется не 60-65 см подвздошной кишки, а 55 см. А проксимальный тубулярный конец сохраняется на протяжении 15 см, а не 20 см. Далее детубуляризированную часть кишечного трансплантата складывают симметрично U-образно (вершина U направлена каудально, длина колен – 20 см), прилежащие края сшивают однорядным обвивным непрерывным швом через все слои со стороны слизистой (Полисорб 3/0). Таким образом, формируют заднюю стенку резервуара. Затем резервуар складывают не в поперечном, как при операции Studer, а в продольном направлении (рис. 1) путем совмещения противоположных длинных сторон.
Рис. 1. Формирование задней стенки U-образного резервуара
При этом образуется трубчатый резервуар U-образной формы, который ушивают наглухо однорядным обвивным непрерывным серозно-мышечноподслизистым швом со стороны серозной оболочки кишки (рис. 2). Продольное сшивание U-образного резервуара обеспечивает более близкое прилежание нижней точки резервуара к культе уретры (на 3-4 см) в сравнении с поперечным складыванием при методике Studer.
Рис. 2. Ушивание передней стенки U-образного резервуара
Однако в большинстве случаев при короткой брыжейке это не обеспечивает отсутствия натяжения в анастомозе с уретрой. Для еще большего низведения нижней стенки резервуара в малый таз выполняют инвертирующее позиционирование сформированного резервуара в малом тазу. Для этого осуществляют «выворачивание» сформированного U-образного резервуара между листками брыжейки кверху, начиная от вершины «U» (рис. 3).
Рис. 3. Инвертирование сформированного U-образного резервуара от его вершины
После завершения полного выворачивающего позиционирования (рис. 4) и ротации резервуара вместе с приводящим тубуляризированным сегментом (рис. 5), задняя стенка резервуара, свободная от брыжейки, оказывается расположенной кпереди и еще более свободно низводится в малый таз, сокращая расстояние до культи уретры еще на 3-4 см. При этом не происходит перегиба брыжейки, она свободно ротируется под резервуаром. А сам резервуар не оказывается «перетянутым» сосудами брыжейки в сагиттальной плоскости, как при поперечном его складывании. Этот момент является весьма важным для последующего адекватного и беспрепятственного расправления резервуара в малом тазу (увеличения его емкости) в послеоперационном периоде.
Рис. 4. Выворачивание U-образного резервуара между листками брыжейки резецированного кишечного сегмента
Рис. 5. Свободная ротация брыжейки под резервуаром без ее перегиба
Далее в самой нижней точке резервуара, прилежащей к уретре, формируют отверстие, пропускающее кончик указательного пальца, производят анастомоз с уретрой узловыми швами через все слои, Полисорб 2/0, на 2, 4, 6, 8, 10 и 12 ч условного циферблата. По уретре в полость неоциста устанавливают катетер Foley Ch№ 20-22. Стентированные мочеточники проводят забрюшинно, и через разрез париетальной брюшины вводят в брюшную полость на уровне верхнего края приводящего тубуляризированного сегмента. По методике Wallace (анастомоз Y-типа) мочеточники анастомозируют с открытым концом кишки приводящего сегмента резервуара. До полного ушивания анастомоза мочеточниковые стенты выводят по уретре наружу. К катетеру Foley у меатуса фиксируют мочеточниковые стенты. Катетер Foley фиксируется к уздечке penis (либо к большой половой губе). После этого окончательно ушивают мочеточниковорезервуарный анастомоз. Дополнительный цистостомический дренаж не устанавливают. Резервуар ушивают наглухо и дренируют исключительно трансуретрально, что максимально сокращает сроки восстановления самостоятельного мочеиспускания.
Результаты
В I группе у 10 пациентов (66,6%) в раннем послеоперационном периоде развилась несостоятельность анастомоза между резервуаром и уретрой. Это потребовало реанастомозирования уретры и резервуара у 3 больных, а у 7 пациентов пролонгированного удержания уретрального катетера (от 3 до 8 недель), тогда как во II группе подобного осложнения не отмечено. Средняя емкость неоциста после удаления уретрального катетера на 14 сутки в I и II группах – 190 и 110 мл, через 3 мес. – 200 и 350 мл, через 12 мес. – 420 и 490 мл. Максимальное давление в резервуаре к 6 мес. в I группе не превышает 45 см. вод. ст. (в среднем 35 см. вод. ст.) и 40 см. вод. ст. (в среднем 30 см. вод. ст.) во II группе соответственно. Дневное удержание мочи к 6 мес. в I и II группах – 86,0 и 94,7%, ночное удержание при одной принудительной ночной микции – 70,0 и 79,0%.
Заключение
Модификация ортотопической илеоцистопластики путем инвертации резервуара целесообразна к применению у пациентов при создании ортотопического тонкокишечного мочевого резервуара и короткой брыжейке тонкой кишки. Инвертация резервуара позволяет минимизировать осложнения после цистэктомии и улучшить функциональные показатели резервуара. Предложенный способ прост, надежен и позволяет добиться максимального качества жизни больных после радикальной цистэктомии. Описанный принцип инверсии применим и при других вариантах ортотопической кишечной цистопластики, когда необходимо уменьшить натяжение в кишечно-уретральном анастомозе.
Литература
1. Roehrborn, C.G. al characteristics of the Camey ileal bladder / C.G. Roehrborn, C.M. Teigland, A.I. Sagalowsky // J. Urol. – 1987. – V.138(4). – P.739-742.
2. Camey, M. Complications of the Camey procedure / M. Camey, H. Botto, E. Richard // Urol. Clin. North. Am. – 1988. – V.15(2). – P.249-255.
3. Orthotopic bladder replacement using ileum: techniques and results / J. Ramon, P. Leandri, G. Rosol, H.Botto // Reconstructive Urology. – Oxford: Blackwell Scientific Publications, 1993. – P.445-457.
4. Коган, М.И. Современная диагностика и хирургия рака мочевого пузыря. / М.И. Коган, В.А. Перепечай. – Ростов н/Д, 2002. – 242 с.
5. Steven, K. The orthotopic Kock ileal neobladder: al results, urodynamic features, complications and survival in 166 men / K. Steven, A.L. Poulsen // J. Urol. -2000. – V.164(2). – P.288-295.
6. The Kock ileal neobladder: upd experience in 295 male patients / D.A. Elmajian, J.P. Stein, D. Esrig et al. // J. Urol. – 1996. – V.156(3). – P.920-925.
7. The urethral Kock pouch: long-term al and oncological results in men / A.A. Shaaban, A. Mosbah, M.S. ElBahnasawy et al. // BJU Int. – 2003. – V.92(4). – P.429-435.
8. Wright, E.J. Urinary diversion. Scientific Foundations and Clinical Practice / Eds K.J. Kreder, A.R. Stone / 2nd Ed. London and New York, 2005. – P.135-141.
9. Hautmann, R.E. Urinary diversion: ileal conduit to neobladder / R.E. Hautmann // J. Urol. 2003. – V.169(3). – P.834-842.
10. Zinman, L.N. Bladder Reconstruction and Continent Urinary Diversion / Eds L.R. King, A.R. Stone, G.D. Webster / 2nd Ed. St. Louis, 1991. – P.6887.
11. Морозов, А.В. Ортотопический «энтеро-неоцистис» низкого давления / A.В. Морозов, К.А. Павленко // М: ИД Медпрактика-М, 2006. – С. 66-67.
12. Перепечай, В.А. Инверсия ортотопического кишечного мочевого резервуара для предотвращения натяжения в уретрорезервуароанастомозе / В.А. Перепечай // Клиническая практика. – 2011. – №1 – С.18-26.
Статья опубликована в журнале “Вестник урологии”. Номер №3/2013 стр. 3-12
Источник
