Рецидив после удаления мочевого пузыря

 Рецидив рака мочевого пузыря означает повторное развитие опухоли после проведенного лечения и ремиссии. Многие люди сталкиваются с чрезмерным беспокойством и страхом на фоне опасения, что болезнь повторится. Проблема проявляется в виде неправильной трактовки симптомов и постоянными навязчивыми мыслями. Одной из главных задач врачей-онкологов является профилактика рецидивов после лечения рака. Уролог обговаривает с пациентом симптомы и признаки, которые могут указывать на возможный рецидив болезни, чтобы предупредить его. Пациенту важно регулярно посещать врача, проходить обследование. Так можно будет выявить рецидив на ранней стадии.
Рецидив рака мочевого пузыря означает повторное развитие опухоли после проведенного лечения и ремиссии. Многие люди сталкиваются с чрезмерным беспокойством и страхом на фоне опасения, что болезнь повторится. Проблема проявляется в виде неправильной трактовки симптомов и постоянными навязчивыми мыслями. Одной из главных задач врачей-онкологов является профилактика рецидивов после лечения рака. Уролог обговаривает с пациентом симптомы и признаки, которые могут указывать на возможный рецидив болезни, чтобы предупредить его. Пациенту важно регулярно посещать врача, проходить обследование. Так можно будет выявить рецидив на ранней стадии.
Виды рецидивов рака мочевого пузыря
Новообразование может иметь разную локализацию. От этого зависит вид рецидива патологии:
- Местный. Опухоль появляется в тканях, где была ранее локализована основная опухоль до удаления (может встречаться и в других участках в пределах мочевого пузыря).
- Региональный. Появление новообразования в уретре и мочеточнике. Развивается в первые три года после хирургического вмешательства.
- Отдаленный. Распространение рака за пределы органов малого таза. Встречается после удаления мочевого пузыря у пациентов с высоким риском рецидива.
Симптомы, указывающие на рецидив болезни
При повторном развитии опухоли пациент обычно наблюдает подобные симптомы, что и первичном раке. Основной признак – гематурия, когда в моче появляется примесь крови. Иногда глазом обнаружить ее не удается, но наличие проблемы подтверждает анализ мочи.
Если у пациента цистит, в совокупности с ростом новообразования учащаются позывы к мочеиспусканию. Причем процесс опорожнения мочевого пузыря вызывает неприятные ощущения. В нижней части живота могут появляться эпизодические, а затем постоянные боли.
Факторы риска повторного развития рака
Рецидив возникает на фоне:
- Вредных привычек (курение, употребление алкоголя).
- Хронического воспаления.
- Контакта с канцерогенами в быту или производстве.
- Карциномы мочевого пузыря у кровных родственников.
Риск повторного образования опухоли повышен у пациентов старше 65 лет, особенно среди представителей мужского пола.
Частота рецидива рака составляет 50%.
Диагностика и лечение рецидива
 Пациенты после ТУР стенки мочевого пузыря с опухолью обязательно должны наблюдаться у врача, проходить регулярно цистоскопию (в первый год каждые 3 месяца). При необходимости врач может назначать МРТ или КТ. Если опухоль выявилась во время цистоскопии, пациенту проводится операция по ее удалению. Однако в будущем это не исключает рецидив патологии. В некоторых случаях больному могут назначить курс внутрипузырной химиотерапии для снижения риска повторения заболевания.
Пациенты после ТУР стенки мочевого пузыря с опухолью обязательно должны наблюдаться у врача, проходить регулярно цистоскопию (в первый год каждые 3 месяца). При необходимости врач может назначать МРТ или КТ. Если опухоль выявилась во время цистоскопии, пациенту проводится операция по ее удалению. Однако в будущем это не исключает рецидив патологии. В некоторых случаях больному могут назначить курс внутрипузырной химиотерапии для снижения риска повторения заболевания.
Пациенты сдают цитологический анализ мочи и при необходимости проводится биопсия с целью получения гистологического заключения о состоянии тканей. Обследование может видоизменяться в каждом индивидуальном случае, учитывая состояние больного.
Тактика лечения рецидива отличается в каждом случае и зависит от стадии заболевания, степени злокачественности, локализации новообразования. При рецидиве может проводиться повторная ТУР или Эн-блок резекция стенки мочевого пузыря. При мышечноинвазивном раке, выполняют радикальную цистэктомию, когда мочевой пузырь полностью удаляют.
При повторном развитии онкологического заболевания средняя 5-летняя выживаемость составляет около 25%. Вероятность положительного исхода при рецидиве зависит от периода возникновения патологии, размера опухоли, пола и возраста больного.
Источник
Свеклина Т.А., Крупин В.Н.
Кафедра урологии ГБОУ ВПО НижГМА Минздрава России, г.Нижний Новгород
Введение
Проблема рецидивирования после органосохраняющего оперативного лечения мышечно-инвазивного рака мочевого пузыря широко обсуждается в литературе [1, 2]. В случае с поверхностными раками мочевого пузыря для профилактики рецидивов, с целью воздействия на возможно нераспознанный рак in situ в первые 6 часов после оперативного лечения внутрипузырно вводят химиопрепарат (согласно EORTC 2004 г.), что приводит к снижению рецидивов от 20% до 50% [3]. Дополнительные методы визуализации радикальности удаления опухоли во время операции при поверхностном раке мочевого пузыря (оптическая когерентная томография (ОКТ), фотодинамическая диагностика (ФД)) также позволяют снизить частоту рецидивов до 0-8,3% [4]. Одной из причин рецидивирования при мышечно-инвазивном раке мочевого пузыря могут быть ассоциированные опухоли.
По данным Переверзева А.С. 2002 г. [5] риск развития инвазивного рака мочевого пузыря при первичной карциноме in situ – 40%, при вторичной карциноме – 70-80%. По данным Carroll P.R. 2000 г. [6] к моменту постановки диагноза рака мочевого пузыря 50-70% больных имеют рак in situ. Используя дополнительные методы обследования слизистой мочевого пузыря на дооперационном этапе, внутрипузырную адъювантную химиотерапию, возможно добиться значительного снижения частоты рецидивов при органосохраняющем оперативном лечении мышечно-инвазивного рака мочевого пузыря, что подтверждается многими исследованиями по профилактике рецидивов у больных с мышечно-инвазивным раком мочевого пузыря [4]. Цель исследования: изучить выживаемость, частоту и характер рецидивов после органосохраняющего оперативного лечения мышечно-инвазивного рака мочевого пузыря при использовании дополнительных методов обследования слизистой мочевого пузыря на дооперационном этапе, внутрипузырной адъювантной химиотерапии.
Материалы и методы
В основе работы лежат результаты лечения 61 больного мышечно-инвазивным раком мочевого пузыря в стадии Т2b–Т3аN0M0G1-G3 после органосохраняющего оперативного лечения (резекция мочевого пузыря или резекция мочевого пузыря с пересадкой мочеточника), которым выполнялись цитологическое исследование мочи, оптическая когерентная томография или фотодинамическая диагностика на дооперационном этапе и проводилась адъювантная внутрипузырная химиотерапия в урологических отделениях НОКБ им. Семашко в период с 2003 по 2008 гг. В зависимости от вида оперативного лечения пациенты были поделены на 2 группы. Группу I составили 50 пациентов после резекции мочевого пузыря. Группу II – 11 пациентов после резекции мочевого пузыря с пересадкой мочеточника. По половому, возрастному признакам, по количеству сопутствующих патологий, по стадии заболевания, по степени дифференцировки группы были сопоставимы.
По результатам цитологического исследования мочи, выполненного на дооперационном этапе, заключение переходно-клеточного рака мочевого пузыря было поставлено у 33% пациентов, папиллома с малигнизацией – у 54%, carcinoma in situ – у 5%, реактивные изменения слизистой мочевого пузыря – у 7%, клетки без атипических изменений – у 1%.
На момент окончания набора материала завершенных наблюдений было 13%, цензурированных 87%.
Результаты
Общая 3-х летняя выживаемость пациентов группы I составила 82%, 5-ти летняя – 70%. Онкоспецифическая 3-х летняя выживаемость пациентов группы I – 98%, 5-ти летняя выживаемость – 96%. Безрецидивная 3-х летняя выживаемость пациентов группы I – 76%, 5-ти летняя выживаемость – 64%. Онкоспецифическая выживаемость у пациентов I группы выше, чем общая, что связано с более частой причиной смерти от сопутствующих патологий. Общая 3-х летняя выживаемость пациентов группы II составила 91%, 5-ти летняя – 82%. Онкоспецифическая 3-х летняя выживаемость пациентов группы II – 91%, 5-ти летняя выживаемость – 82%. Безрецидивная 3-х летняя выживаемость пациентов группы II – 73%, 5-ти летняя выживаемость – 64%. Онкоспецифическая выживаемость пациентов II группы равна общей, что связано с онкологической причиной смерти. Безрецидивная выживаемость пациентов обеих групп ниже, чем общая и онкоспецифическая, что связано с наличием рецидивов рака мочевого пузыря (таблица 1).
Таблица 1. Показатели выживаемости пациентов I и II групп
| Выживаемость, % | I группа, n=50 | II группа, n=11 | ||
| 3-х летняя | 5-ти летняя | 3-х летняя | 5-ти летняя | |
| Общая | 82 | 70 | 91 | 82 |
| Онкоспецифическая | 98 | 96 | 91 | 82 |
| Безрецидивная | 76 | 64 | 73 | 64 |
В I группе рецидивы возникли в 14% случаев: в зоне операции в 4% случаев, на других местах – в 10% случаев. Во II группе рецидивы возникли в 18% случаев: все рецидивы на местах, отличных от зоны резекции.
При возникновении рецидива на другом месте достоверно снижалась стадия заболевания (р=0,000573), но по степени дифференцировки достоверных закономерностей не выявлено. При появлении рецидива на том же месте достоверных изменений ни стадии заболевания, ни степени дифференцировки не выявлено. Каких-либо закономерностей в появлении рецидива на том или другом месте, отличном от первоначального очага, среди пациентов не выявлено ни от стадии заболевания, ни от степени дифференцировки, ни от локализации первичного очага, ни от количества опухолевых образований.
Обсуждение
По данным литературы общая 5-ти летняя выживаемость больных мышечно-инвазивным раком мочевого пузыря после радикальной цистэктомии составляет от 15% до 80% [7, 8], от 40 до 68% [9]. 5-ти летняя общая выживаемость после органосохраняющего лечения колеблется по разным данным от 32,5% до 93%, 3-х летняя выживаемость от 47,4-97,5% [10].
В результате данного исследования общая 5-ти летняя выживаемость пациентов I и II групп составила 70% и 82%, что не отличается от общестатистических данных, но онкоспецифическая 5-ти летняя выживаемость составила 96% и 82%, что является достаточно высоким показателем и свидетельствует о более частой причине смерти от сопутствующей патологии, нежели от рака мочевого пузыря.
По данным литературы большой процент рецидивов рака мочевого пузыря после органосохраняющего лечения (50-90%) [1, 7] является причиной выбора цистэктомий при лечении мышечно-инвазивного рака мочевого пузыря. В данном исследовании частота рецидивов составила 14% и 18%, при этом большинство рецидивов выявлены на местах, отличных от зон резекции. При обнаружении рецидива в другом месте статистически достоверно снижалась стадия заболевания, что свидетельствует о возможно нераспознанном очаге рака in situ, а не об истинном рецидиве.
Выводы
С целью расширения показаний к органосохраняющим операциям при мышечно-инвазивном раке мочевого пузыря необходимы дополнительные исследования слизистой мочевого пузыря на дооперационном этапе для исключения ассоциированного поверхностного рака мочевого пузыря (цитологическое исследование мочи, оптическая когерентная томография, фотодинамическая диагностика), проведение адъювантной внутрипузырной химиотерапии для профилактики образования рецидивов рака мочевого пузыря.
ЛИТЕРАТУРА
1. Карякин О.Б. Органосохранная тактика при инвазивном раке мочевого пузыря: «за» и «против» // Практическая онкология – 2003. – Т.4, № 4. – С. 252-255.
2. Попов А.М., Карякин О.Б. Органосохраняющее лечение инвазивного рака мочевого пузыря // Росссийский онкологический журнал – 2005. – № 3. – С. 49-52.
3. Стрельцова О.С. Методы диагностики состояния слизистой оболочки мочевого пузыря: учебное пособие для врачей. – Н.Новгород: Изд-во Нижегородской государственной медицинской академии, 2007. – 56 с.
4. Мартов А.Г., Чернышев И.В., Сысоев П.А. и соавт. Эндоскопические операции при инвазивном раке мочевого пузыря. НИИ урологии, Москва, Липецкий областной онкологический диспансер. // Урология. – 2005, – № 2. – С. 35-39.
5. Переверзев А.С., Петров С.Б. Опухоли мочевого пузыря: Монография. – Х.: Факт, 2002. – 303 с.
6. Grossfeld G.D., Carrol P.R. Invasive Bladder Cancer // Comprehensive Urology – 2001. – P. 373-393.
7. Гранов А.М, Винокуров В.Л. Лучевая терапия в онкогинекологии и онкоурологии / Под ред. А.М. Гранова, В.Л. Винокурова. – Спб.: «Фолиант», 2002. – 352 с.
8. Красный С.А. Радикальное хирургическое лечение инвазивного рака мочевого пузыря // Онкоурология – 2007. – №1. – С. 69-73.
9. Bassi P. et al. Prognostic factors of outcome after radical cystectomy for bladder cancer: a retrospective study of a homogeneous patient cohort // J. Urol. – 1999. – Vol. 161. – P. 1494-1497.
10. Клиническая онкоурология / Под ред. Б.П. Матвеева. – М.: АБВПресс, 2011. – 934 с.
Статья опубликована в журнале “Вестник уролгии”. Номер №1/2013 – стр. 3-7
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Леонов М.Г.
1
Алексеенко С.Н.
2
Тхагапсо А.А.
1
Шадринова М.Д.
3
Тесленко Л.Г.
3
1 ГБУЗ «Онкологический диспансер № 3»
2 ФБОУ «Кубанский государственный медицинский университет»
3 ГБУЗ «Клинический онкологический диспансер № 1»
В статье представлены результаты ретроспективного исследования 627 больных раком мочевого пузыря (РМП), изучены частота и сроки возникновения рецидивов заболевания после проведенного лечения. По результатам обследования 173 больных РМП после проведенного лечения с использованием цистоскопии и цитологического исследования промывных вод мочевого пузыря с помощью метода жидкостной цитологии. Показано, что эффективность метода жидкостной цитологии в диагностике местных рецидивов РМП превышает традиционное цитологическое исследование на 29,6 % и количество неудовлетворительных цитологических препаратов снижается на 24,6 %.
рак мочевого пузыря
рецидив заболевания
цитологическая диагностика
жидкостная цитология
1. Лопаткин Н.А., Камалов А.А., Кудрявцев Ю.В. и соавт. Флуоресцентная диагностика рака мочевого пузыря // Урология. – 2000. – № 4. – С. 3–6.
2. Матвеев Б.П., Фигурин К.М. Результаты оперативного лечения больных раком мочевого пузыря // Урология и нефрология. – 1997. – № 2. – С. 25–28.
3. Переверзев А.С., Петров С.Б. Опухоли мочевого пузыря. – Харьков: Факт, 2002. – 303 с.
4. Поляничко М.Ф. Усовершенствование, диагностика и разработка восстановительных операций при хирургическом и комбинированном лечении злокачественных новообразований мочевого пузыря: Автореф. дис. д-ра мед. наук. – Ростов-на-Дону, 1980. – 26 с.
5. Семыкин Ю.А. Аутопластика после расширенных резекций в хирургическом и комбинированном лечении глубокоинвазивного рака мочевого пузыря: дис. … канд. мед. наук. – Томск, 1991. – 214 с.
6. Badjuk M., Dvoracek J. Diagnosis and therapy of superficial tumors of urinary bladder // Cas. Lek. Cesk. – 2002. – Vol. 22. – P. 723–728.
7. El-Bolkainy M.N., Mokhtar N.M., Ghoneim M.A. et al. The impact of schistosomatosis on the pathology of bladder carcinoma // Cancer. – 1981. – № 18. – P. 2643–2648.
8. Konofaos P., Zietman A., Wishnow K. Bladder cancer. In: Cancer of medicine, ed. 5 Ed. by J.F. Holland et al. Lea&Febiger. – 2001. – P. 1544–1558.
9. Pieras E., Palou J., Salvador J. et al. Management and prognosis of transitional cellcarcinoma. Superficial recurrence in muscle invasive bladder cancer after bladderpreservation. // Eur. Urol. – 2003. – Vol. 44. – P. 222–225.
10. Sweeney P., Kursh E.D., Resnick M.I. Partial cystesctomy // Urol. Clin. North. Amer. – 1992. – Vol. 19. – P. 701–711.
Частота местных рецидивов РМП после проведенного лечения, по данных разных авторов, составляет 50–95 % [1]. Долгие годы стандартом оказания медицинской помощи больным с мышечно-инвазивным РМП была цистэктомия. Цистэктомия является травматичной операцией, а пожилой и старческий возраст больных, наличие выраженной сопутствующей патологии часто ограничивают возможности и объем оперативного вмешательства, также немаловажное значение имеет отказ части больных от этого вида хирургического лечения [4].
Учитывая тот факт, что в последние годы изменилось отношение к вопросам качества жизни, то в настоящее время большое значение уделяется органосохраняющему лечению при инфильтративных формах опухолей мочевого пузыря – трансуретральной резекции (ТУР) мочевого пузыря в сочетании с адъювантной химиолучевой терапией [2, 7, 8, 10].
Поверхностный РМП среди злокачественных новообразований мочевого пузыря встречается в 80 % случаев. Частота рецидивов заболевания при этой форме РМП колеблется от 56,0 % до 65,5 % при I стадии заболевания, от 31,5 % при Т2а до 70,1 % – при T2b стадии [2, 5].
Возникновение рецидивов РМП после проведенного лечения зависит от многих факторов, среди которых наиболее значимыми являются: стадия процесса, величина опухоли и мультицентричность ее роста [1, 3, 7, 9].
Основными методами диагностики местных рецидивов РМП после окончания лечения являются цистоскопия и цитологическое исследование промывных вод мочевого пузыря. Диагностическая точность традиционного цитологического исследования в диагностике РМП невелика и составляет не более 40–54 % [1].
Для РМП характерна высокая частота рецидивов и прогрессии опухоли, что предполагает длительное наблюдение за больным, включающее проведение лабораторных и инструментальных методов исследований. В связи с этим совершенствование существующих методов своевременной диагностики рецидивов РМП остается актуальной задачей, решение которой позволит улучшить качество и увеличить продолжительность жизни больных [3]
Цель исследования – изучение частоты и сроков рецидивирования РМП после проведенного лечения и оценка эффективности использования метода жидкостной цитологии в своевременной диагностике местных рецидивов этого заболевания.
Материалы и методы исследования
Проведено ретроспективное изучение данных 627 больных РМП I–IV стадий, проходивших лечение в ГБУЗ «Клинический онкологический диспансер № 1» (г. Краснодар) в 2008–2010 гг.
Больные были разделены на две группы в зависимости от стадии первичной опухоли. В первую группу вошли 528 (84,2 %) пациентов, проходивших лечение по поводу поверхностного РМП (Tis–T1N0M0 стадии), подвергнутых органосохраняющему лечению. Во вторую группу – 99 (22,8 %) больных, лечившихся по поводу инвазивного РМП (II–IVстадий), которым была выполнена резекция мочевого пузыря или цистэктомия.
При проведении стадирования первичного опухолевого процесса использовалась Международная классификация злокачественных опухолей TNM 7-го пересмотра (2009), в рубрике С67 мочевой пузырь.
В каждой группе больных изучены частота и сроки возникновения рецидивов в течение трех лет.
С целью улучшения цитологической диагностики местных рецидивов РМП за период 2011–2013 гг. в ГБУЗ «Онкологический диспансер № 3» (г. Новороссийск) былои обследованы 173 больных РМП после проведенного лечения (комплексного или комбинированного) с использованием эндоскопического (фиброцистоскопия) и цитологического (жидкостная цитология и традиционное исследование) методов.
Всем обследуемым выполняли цистоскопию гибким фиброцистоскопом Karl Storz (Германия). Перед проведением цистоскопии выполняли общие клинические обследования, позволяющие определить противопоказания к проведению внутрипузырного инвазивного вмешательства и необходимые мероприятия по подготовке пациента к фиброцистоскопии. После окончания фиброцистоскопии получали спиртовой смыв мочевого пузыря по методу В.Т. Кузьмина (1963), делили его на две порции, одну из которых исследовали традиционным цитологическим методом, другую – методом жидкостной цитологии. При выполнении жидкостной цитологии полученный смыв центрифугировали на центрифуге «Эликон ЦЛМН-Р10-01» при скорости 1 500 об/мин в течение 10 мин. Из полученного клеточного осадка готовили традиционные цитологические препараты. При выполнении жидкостной цитологии к клеточному осадку в объеме 100–400 мкл добавляли 4 мл питательной среды 199 для получения клеточной суспензии. Клеточную суспензию цитофугировали в CytoFuge 2 (Stat Spin, США) при скорости 1 000 об/мин в течение 8 мин. Полученные монослойные препараты высушивали на воздухе. Фиксацию препарата проводили фиксатором Май-Грюнвальда, окраску – по методу Романовского-Гимзе автоматизированным методом на универсальном настольном роботе Shandon Varistain Gemini ES (Англия), обеспечивающем быстрое и одновременное окрашивание большого количества цитологических препаратов. Микроскопирование цитологических препаратов проводилось под иммерсионной системой с использованием видеомикроскопа МС 1000 (LCD), Австрия (окуляр 10х, объектив 100х, увеличение 1000). Видеомикроскоп МС (LCD) со встроенной электронной системой, жидкокристаллическим сенсорным дисплеем, позволяющим проводить просмотр изображения в реальном времени. Результаты микроскопирования фотографировались и сохранялись на CD Cart, что позволило составить фотоархив микропрепаратов.
Была проведена сравнительная оценка эффективности метода жидкостной цитологии и традиционного цитологического исследования путем сопоставления полученных результатов.
Результаты исследования и их обсуждение
Возраст 627 больных РМП колебался от 49 до 79 лет. Средний возраст составил 63,2 ± 1,8 года. По полу больные распределились следующим образом: мужчин – 559 (89,2 %), женщин – 68 (10,8 %) (соотношение 8:1).
У 528 больных поверхностным РМП была выполнена ТУР мочевого пузыря с последующей внутрипузырной химиотерапией (ВПХТ). При инвазивном РМП выполнены следующие виды лечения: 18 пациентам – резекция мочевого пузыря с последующей ВПХТ, 27 – резекция мочевого пузыря с последующей лучевой терапией, 42 – резекция мочевого пузыря с последующей химиолучевой терапией и 12 больным проведена цистэктомия.
У пяти пациентов из группы больных с проведенным лечением в объеме резекции мочевого пузыря с последующей лучевой терапией в лечении применяли препарат УРО-БЦЖ. Инстилляции проводили в течение шести недель.
В следующей группе больных с резекцией мочевого пузыря и последующей ВПХТ (четырем больным из 18) сразу после ТУР мочевого пузыря в мочевой пузырь вводили 50 мг доксорубицина или цисплатина, а через 3 недели проводили БЦЖ-терапию.
Большинство больных инвазивным РМП имели выраженную сопутствующую соматическую патологию, препятствующую проведению радикальной операции, а часть пациентов отказалась от цистпростатэктомии. Комплексное лечение в этих случаях включало проведение органосохраняющего хирургического вмешательства в объеме ТУР-опухоли мочевого пузыря, химиотерапии и/или дистанционной лучевой терапии.
Таблица 1
Частота рецидивов РМП (через 36 месяцев наблюдения) в зависимости от стадии первичной опухоли
Рецидивы РМП | Стадия первичного РМП | Всего | ||||
группа (Tis–T1 стадии) | группа (II–IV стадии) | |||||
абс. | % | абс. | % | абс. | % | |
Поверхностные рецидивы | 189 | 91,7 | 16 | 28,1 | 206 | 77,9 |
Инвазивные рецидивы | 17 | 8,3 | 41 | 71,9 | 57 | 22,1 |
Всего | 206 | 100 | 57 | 100 | 263 | 100 |
Таблица 2
Сравнительная оценка эффективности цитологических методов
Исследуемая группа | Количество исследуемых, N | Метод жидкостной цитологии, N ( %) | Традиционное цитологическое исследование, N ( %) | Р |
Диспансерные больные РМП | 173 | 70 (40,4) | 54 (31,2) | < 0,05 |
Через три года после окончания специального лечения было диагностировано 57 рецидивов (57,6 %) у 99 больных с инвазивным раком мочевого пузыря, относящихся ко второй группе исследования.
В группе больных с поверхностным раком мочевого пузыря рецидив заболевания после проведенного лечения диагностирован у 206 (39 %) (табл. 1).
При этом установлено, что у большинства больных, проходивших лечение по поводу поверхностного РМП, выявлены неинвазивные рецидивы. Среди больных после лечения изначально инвазивного РМП большинство рецидивов также имело инвазивный характер.
При изучении сроков возникновения рецидива у больных РМП после окончания лечения можно отметить, что в первой группе больных с поверхностным РМП наиболее часто рецидив заболевания возникал на первом году наблюдения – у 176 (85,4 %), на втором году – у 19 (9,2 %), на третьем – у 11 (5,4 %).
Во второй группе больных с инвазивным РМП также на первом году наблюдения частота рецидивов была наиболее высокой и составила 41 (72,0 %), на втором году – 11 (19,3 %), на третьем году – 5 (8,7 %).
В связи с вышеприведенным анализом, учитывая высокую частоту рецидивирования рака мочевого пузыря после проведенного лечения, был проведен поиск наиболее надежного и информативного метода своевременной диагностики рецидивов РМП с помощью метода жидкостной цитологии.
В результате проведенного исследования обнаружена существенная разница в диагностике местных рецидивов РМП после проведенного лечения среди сравниваемых методов (табл. 2).
Из 173 больных, находящихся на диспансерном наблюдении после проведенного лечения по поводу РМП, рецидив заболевания диагностирован в 54 (31,2 %) случаях, а при использовании метода жидкостной цитологии – в 70 (40,4 %). Диагностическая точность жидкостной цитологии на 29,6 % выше (р < 0,05), чем при обычном цитологическом методе.
В результате применения метода жидкостной цитологии снизилось количество неудовлетворительных микроскопических препаратов на 24,6 %.
Клинический случай использования метода жидкостной цитологии в диагностике местного рецидива РМП. Больной П., 62 лет, мужского пола. 04.06.13 г. выполнена операция ТУР опухоли мочевого пузыря. ПГИ № 2134–07 переходно-клеточный рак. В послеоперационном периоде получил семь курсов внутрипузырной химиотерапии (препарат доксорубицин 50 мг еженедельно). Больной находился под диспансерным наблюдением.
При контрольном обследовании 02.09.13 г. проведена фиброцистоскопия. При эндоскопическом исследовании обнаружен подозрительный участок в области послеоперационного рубца. Полученный спиртовый смывы мочевого пузыря был разделен на две порции. Цитологическое исследование первой порции было проведено традиционным методом. Опухолевых клеток обнаружено не было. Вторая порция смыва мочевого пузыря была исследована методом жидкостной цитологии с использованием питательной среды 199. При этом в смыве мочевого пузыря были обнаружены клетки переходно-клеточного рака (рисунок). По результатам выполненного обследования у больного диагностирован местный рецидив РМП.
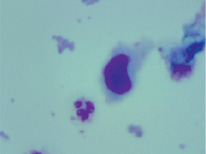
Цитологический микропрепарат – переходно-клеточный РМП (микрофотография). Окраска по Романовском-Гимзе, х1000
Заключение
Таким образом, жидкостная цитология с использованием питательной среды 199, в отличие от традиционного цитологического исследования осадка мочи или смыва мочевого пузыря, значительно повышает чувствительность цитологического метода исследования за счет получения монослойных препаратов, которые характеризуются равномерным, монослойным распределением клеточного материала на небольшом участке предметного стекла, хорошей визуализацией деталей ядра и цитоплазмы, значительным снижением числа элементов воспаления, эритроцитов, слизи, бактерий, кристаллов мочевых солей, артефактов, сокращает время и повышает производительность исследования.
Использование метода жидкостной цитологии в онкологии, урологии, клинической лабораторной диагностике значительно повышает чувствительность метода цитологического исследования в диагностике местных рецидивов РМП.
Библиографическая ссылка
Леонов М.Г., Алексеенко С.Н., Тхагапсо А.А., Шадринова М.Д., Тесленко Л.Г. РЕЦИДИВЫ РАКА МОЧЕВОГО ПУЗЫРЯ И ВОЗМОЖНОСТИ ЦИТОЛОГИЧЕСКОГО МЕТОДА ИХ ДИАГНОСТИКИ // Международный журнал прикладных и фундаментальных исследований. – 2016. – № 9-3. – С. 393-396;
URL: https://applied-research.ru/ru/article/view?id=10258 (дата обращения: 31.01.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
