Рак шейки матки поражение мочевого пузыря

Рак шейки матки представляет собой чрезвычайно опасное злокачественное онкологическое заболевание, сокращающее жизнь пациенток в среднем на 24–30 лет.
Симптомы рака шейки матки
На ранних стадиях рака шейки матки и при предраковых изменениях женщину ничего не беспокоит. Обычно возникновение симптомов говорит о том, что опухоль уже проросла в соседние органы.

Проявления заболевания неспецифичны и могут встречаться при других патологиях, например, урогенитальных инфекциях:
- Обильные, длительные месячные. Этот симптом имеет значение, если месячные изменились недавно, если прежде они были нормальными.
- Вагинальные кровотечения в промежутках между месячными, после полового акта, после наступления менопаузы.
- Необычные выделения из влагалища: обильные, розового цвета, с неприятным запахом.
- Тазовые боли во время полового акта.
В большинстве случаев эти проявления вызваны не онкологическим заболеванием. Но риск, пусть и небольшой, есть всегда, поэтому при возникновении первых симптомов нужно посетить врача.
На более поздних стадиях к перечисленным симптомам присоединяются такие признаки, как резкая беспричинная потеря веса, боли в пояснице и в ногах, постоянное чувство усталости, патологические переломы костей (признак костных метастазов), подтекание мочи из влагалища.
Причины возникновения
Точные причины рака шейки матки назвать сложно. Но известны факторы риска, которые повышают вероятность возникновения рака шейки матки.
Наиболее значимый фактор риска – папилломавирусная инфекция. По разным данным, до 99% случаев рака шейки матки связаны с вирусами папилломы человека (ВПЧ). До 80% женщин в течение жизни оказываются инфицированы этим возбудителем. Всего существует около 100 типов ВПЧ, из них 30–40 передаются половым путем, лишь 165 повышают риск рака. Но это не значит, что они гарантированно вызовут рак. Типы вируса 16, 18, 31, 33, 35, 39, 45, 51, 52, 56 и 58 относят к высокоонкогенным, 6, 11, 42, 43 и 44 – к низкоонкогенным. Чаще всего виновниками рака шейки матки становятся ВПЧ 16 и 18 типов. Наиболее уязвима к ним зона трансформации (см. ниже). Помимо рака шейки матки, ВПЧ вызывают злокачественные опухоли других органов репродуктивной системы, глотки, ротовой полости, анального канала.
Другие факторы риска:
- Ослабленная иммунная система. Если иммунитет женщины работает нормально, ее организм избавляется от вируса папилломы в течение 12–18 месяцев. Но если защитные силы ослаблены, инфекция сохраняется дольше и повышает риск рака.
- Беспорядочные половые связи. Частая смена партнеров повышает вероятность заражения ВПЧ.
- Акушерский анамнез. Если у женщины было три или более беременностей, либо если первая беременность была до 17 лет, риски повышены в два раза.
- Наследственность. Если у матери или родной сестры женщины диагностирован рак шейки матки, ее риски повышены в 2–3 раза.
- Курение. Вредная привычка также повышает риски вдвое.
- Применение оральных контрацептивов в течение 5 лет и дольше. После прекращения их приема риски снижаются в течение нескольких лет.
Разновидности рака шейки матки
Чтобы понять классификацию рака шейки матки, в первую очередь нужно немного разобраться в ее анатомическом и гистологическом строении. Шейка матки имеет длину 2–3 см и состоит из двух частей:
- Влагалищная часть (экзоцервикс) выступает во влагалище, это то, что гинеколог видит во время осмотра на зеркалах. Слизистая оболочка эндоцервикса состоит из многослойного плоского эпителия.
- Цервикальный канал (эндоцервикс) находится внутри и соединяет влагалище с маткой. Он выстлан цилиндрическим эпителием.
Граница между влагалищной частью и цервикальным каналом называется зоной трансформации.
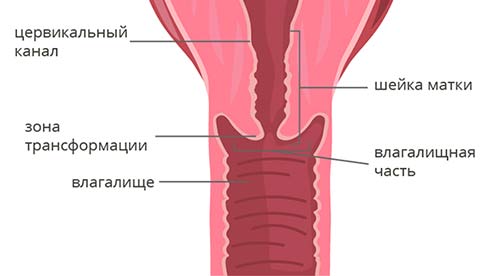
В 70–90% случаев злокачественные опухоли шейки матки представлены плоскоклеточным раком. Он развивается из многослойного плоского эпителия. Чаще всего злокачественное перерождение происходит в зоне трансформации. В зависимости от того, как выглядит опухолевая ткань под микроскопом, плоскоклеточный рак шейки матки делят на ороговевающий и неороговевающий:
- Ороговевающий плоскоклеточный рак шейки матки называется так потому, что клетки, из которых он состоит, склонны к ороговению. Они крупные, имеют неправильную форму, относительно низкую интенсивность деления. При микроскопическом исследовании обнаруживаются образования, которые называются кератогиалиновыми гранулами и “раковыми жемчужинами”.
- При неороговевающем плоскоклеточном раке шейки матки клетки не склонны к ороговению. Они крупные, имеют форму овала или многоугольника, размножаются более интенсивно.
В зависимости от того, насколько раковые клетки отличаются от нормальных, злокачественные опухоли шейки матки делят на высоко-, умеренно- и низкодифференцированные. Последние ведут себя наиболее агрессивно. Плоскоклеточный ороговевающий рак относят к зрелым формам, он встречается примерно в 20% случаев. Неороговевающий рак – это опухоли средней степени зрелости, они составляют 60-70%. Незрелая форма – это низкодифференцированный рак.
В остальных случаях рак шейки матки представлен аденокарциномой. Она развивается из железистых клеток, продуцирующих слизь. За последние 20–30 лет этот тип злокачественных опухолей стал более распространенным.
Намного реже встречаются аденосквамозные карциномы. Эти опухоли сочетают в себе черты плоскоклеточного рака и аденокарциномы. Чтобы определить тип злокачественной опухоли, нужно провести биопсию.
Распространение рака шейки матки в организме
По мере роста, рак шейки матки распространяется на соседние органы. В первую очередь поражаются регионарные лимфатические узлы, окружающая клетчатка (параметрий).
Часто отмечается поражение верхней трети влагалища, что неудивительно, так как оно находится в непосредственном контакте с шейкой матки. Распространение раковых клеток происходит прямым путем при прорастании опухоли во влагалище, лимфогенно (через лимфатические сосуды), путем контактной имплантации – там, где стенка влагалища соприкасается с опухолью. Также вовлекается тело матки.
Распространение опухолевых клеток в прямую кишку, мочевой пузырь и мочеточники, как правило, происходит контактным путем.
Отдаленные метастазы чаще всего встречаются в забрюшинных лимфатических узлах, легких, костях, печени. Менее чем в 1% случаев метастазирование происходит в селезенку, почки, головной мозг.
Диагностика рака шейки матки
Высокие показатели смертности от рака шейки матки связаны с поздним выявлением заболевания: в 35–40% случаев в России диагноз впервые ставится пациенткам с III–IV стадиями болезни.
Так как рак шейки матки может долго протекать бессимптомно, своевременная диагностика возможно только при регулярном прохождении специальных обследований у гинеколога.
Согласно исследованиям ученых из Кильского университета (Великобритания), возрастных ограничений для регулярного скрининга на рак шейки матки не существует. Вопреки сложившемуся мнению, у женщин сохраняется риск развития опухоли и после 65 лет, так как вирус папилломы человека, который в подавляющем большинстве случаев становится причиной онкологического заболевания, может попасть в организм еще в период сексуальной активности, долго «дремать» и в пожилом возрасте привести к развитию рака.
Анализы на вирус папилломы человека
Проведение ПЦР-анализа на наличие вируса папилломы человека может лишь выявить наличие в организме соответствующего вируса. Для определения его способности провоцировать развитие рака шейки матки (онкогенности) и степени активности вируса в организме требуются дополнительные исследования, также проводимые методом ПЦР.
Но даже выявление ВПЧ высокого онкогенного риска не превращает рак шейки матки в нечто фатальное.Во-первых, болезнь может вообще не развиться.Во-вторых, современные технологии позволяют выявлять данную форму рака на самых ранних стадиях и с успехом лечить его, не допуская превращения предраковых изменений в собственно онкологическое заболевание. Следовательно, положительные результаты анализа на ВПЧ должны рассматриваться только как основание для регулярного наблюдения у гинеколога, знакомого с эффективными алгоритмами ведения пациенток из групп риска.
Гинекологический осмотр с кольпоскопией
Иногда рак шейки матки выявляется непосредственно во время осмотра на гинекологическом кресле. Однако так определяется, как правило, запущенный онкологический процесс. И напротив, ранние стадии заболевания обычно проходят без каких-либо заметных изменений, поэтому для своевременной диагностики рака шейки матки используются дополнительные исследования. Во время кольпоскопии влагалищную часть шейки матки осматривают с помощью кольпоскопа – прибора, напоминающего бинокль с источником освещения.
Цитологический мазок (ПАП-тест, тест Папаниколау)
Классический метод цитологического исследования шейки матки, или ПАП-тест, предполагает осторожное «соскабливание» материала особым шпателем с поверхности органа и «размазывание» его по предметному стеклу. Данный метод был разработан в начале прошлого века, в 1923 году. Для своего времени ПАП-тест демонстрировал прекрасные результаты, однако годы использования выявили ряд недостатков метода. Избирательность захвата клеток и неравномерное их распределение по стеклу могут существенно исказить результаты цитологического анализа. Таким образом, чувствительность метода составляет всего 85–95%, причем на ранних стадиях заболевания, характеризующихся небольшим количеством раковых клеток, данный показатель может быть даже ниже.
Метод жидкостной цитологии
Метод жидкостной цитологии предполагает использование специальной «щеточки», позволяющей получить материал для исследования со всей поверхности шейки матки, а не с отдельных ее фрагментов, как это происходит во время ПАП-теста.
Затем материал со «щеточки» переходит в специальный раствор, проходит обработку в особом аппарате и лишь после этого равномерно наносится на предметное стекло. Все это повышает чувствительность метода практически до 100% и исключает вероятность возникновения ошибок, характерных для ПАП-теста.
Также полученный в ходе этого анализа материал может быть использован для определения активности ВПЧ, которая является важным фактором прогноза и может влиять на тактику лечения. И, наконец, раствор с находящимися в нем клетками пригоден для проведения анализа на определение особого белка (Р16ink4a), появляющегося в клетках еще до начала непосредственно онкологического процесса. Таким образом, метод жидкостной цитологии способен не только выявить рак шейки матки, но и предупредить о повышении риска его развития. После одной-единственной процедуры в распоряжении врача появляются результаты трех точных и информативных анализов, позволяющих определить тактику и стратегию ведения конкретной пациентки.
В профилактических целях (при отсутствии жалоб) данные анализы рекомендуется проводить 1 раз в год.
Прогноз при выявлении рака шейки матки
Прогноз при первичной диагностике рака шейки матки определяется степенью запущенности процесса. К сожалению, в нашей стране на протяжении последних десятилетий сохраняется очень высокая доля женщин, впервые обращающихся за медицинской помощью на поздних стадиях заболевания. При своевременно поставленном диагнозе у пациентов на 1-й стадии рака шейки матки показатель 5-летней выживаемости составляет 75-80%, для 2-й стадии — 50-55%. Напротив, при выявлении на 4-й стадии рака шейки матки большинство пациенток не доживает до пятилетнего рубежа, умирая от распространения опухоли или осложнений.
Лечение рака шейки матки
Исходя из опыта клиники, сохранить матку и возможность деторождения возможно при предраковых изменениях шейки матки. При раке шейки матки одинаково широко используют лучевую терапию и хирургическое лечение — расширенная экстирпация матки с придатками.
Лечение зависит от стадии заболевания. При ранних стадиях рака шейки матки проводится преимущественно хирургическое лечение. Во время операции производится удаление матки. Иногда операцию необходимо дополнять удалением лимфатических узлов малого таза. Вопрос об удалении яичников решается индивидуально, при ранней стадии опухоли у молодых женщин возможно оставление яичников. Не менее значимым является лучевое лечение. Лучевая терапия может как дополнять хирургическое лечение, так и являться самостоятельным методом. При ранних стадиях рака шейки матки результаты хирургического и лучевого лечения практически одинаковы. В лечении рака шейки матки может применяться химиотерапия, но к сожалению, возможности химиотерапии при этом заболевании значительно ограничены.
При 0 стадии раковые клетки не распространяются за пределы поверхностного слоя шейки матки. Иногда эту стадию даже рассматривают как предраковое состояние. Такая опухоль может быть удалена разными способами, но при органосохраняющих вмешательствах в дальнейшем сохраняется риск рецидива, поэтому после операции показаны регулярные сдачи цитологических мазков.
Методы лечения плоскоклеточного рака шейки матки, стадия 0:
- Криохирургия – уничтожение опухоли с помощью низкой температуры.
- Лазерная хирургия.
- Конизация шейки матки – иссечение участка в виде конуса.
- Петлевая электроконизация шейки матки.
- Гистерэктомия. К ней прибегают в том числе при рецидиве злокачественной опухоли после вышеперечисленных вмешательств.
Методы лечения аденокарциномы шейки матки, стадия 0:
- Гистерэктомия.
- В некоторых случаях, если женщина планирует иметь детей, может быть выполнена конизация. При этом важным условием является негативный край резекции по данным биопсии. Впоследствии женщина должна наблюдаться у гинеколога, после родов выполняют гистерэктомию.
Выбор метода лечения всегда осуществляется индивидуально лечащим врачом.
При 1а стадии — микроинвазивный рак шейки матки — выполняют экстирпацию матки с придатками. В случаях, когда опухоль прорастает в кровеносные и лимфатические сосуды, также показано удаление тазовых лимфатических узлов. Если женщина планирует иметь детей, возможны органосохраняющие операции. При стадии Iб — рак ограничен шейкой матки — проводят дистанционное или внутриполостное облучение (брахитерапию) с последующей расширенной экстирпацией матки с придатками. В ряде случаев первоначально проводят операцию, а затем дистанционную гамма-радиотерапию.
При 2-й стадии рака шейки матки — вовлечение верхней части влагалища, возможен переход на тело матки и инфильтрация параметрия без перехода на стенки таза — основным методом лечения является лучевая терапия. Также может быть назначена химиотерапия, обычно препаратом цисплатином или его сочетанием с фторурацилом. В этом случае хирургическое лечение проводится редко.
При 3-й стадии рака шейки матки — переход на нижнюю часть влагалища, инфильтрация параметрия с переходом на кости таза — показана лучевая терапия.
При 4-й стадии (переход рака на мочевой пузырь, прямую кишку или отдаленное метастазирование) применяют лишь паллиативное облучение. У пациентов на поздних стадиях рака шейки матки с метастазами лечение носит паллиативный характер, возможно применение химиотерапевтического лечения. В большинстве случаев схема химиотерапии предусматривает применение одного из препаратов платины (карбоплатин или цисплатин) в сочетании с гемцитабином (Гемзар), паклитакселом (Таксол) или топотеканом.
Профилактика
Один из главных факторов риска рака шейки матки — вирус папилломы человека. Поэтому меры профилактики в первую очередь должны быть направлены на предотвращение заражения:
- Беспорядочные половые связи нежелательны, особенно с мужчинами, у которых было много партнерш. Это не защищает от заражения на 100%, но все же помогает сильно снизить риски.
- Презервативы помогут защититься не только от ВПЧ, но и от ВИЧ-инфекции. Стопроцентную защиту они тоже не обеспечивают, потому что не могут полностью исключить контакт с инфицированной кожей.
- Вакцины против ВПЧ — хорошее средство профилактики, но они работают лишь в случае, если женщина пока еще не инфицирована. Если вирус уже проник в организм, вакцина не поможет. Девочек начинают прививать с 9–12 лет.
Второй фактор риска, который связан с образом жизни, и на который можно повлиять — курение. Если вы страдаете этой вредной привычкой, от нее лучше отказаться.
Огромное значение имеет скрининг — он помогает вовремя выявить предраковые изменения и рак шейки матки на ранних стадиях. Нужно регулярно являться на осмотры к гинекологу, проходить PAP-тест и сдавать анализы на ВПЧ.
Основным прогностическим фактором выживаемости пациенток при раке шейки является степень распространенности процесса. Поэтому самым эффективным средством против развития рака являются регулярные профилактические осмотры у специалистов.
Прогноз при плоскоклеточном раке шейки матки
Ориентировочный прогноз определяют на основании статистики. Среди женщин, у которых был диагностирован рак шейки матки, подсчитывают процент выживших в течение определенного времени, как правило, пяти лет. Этот показатель называют пятилетней выживаемостью. Он зависит от того, на какой стадии было выявлено онкологическое заболевание. Чем раньше диагностирован рак и начато лечение — тем лучше прогноз:
- При локализованных опухолях (рак не распространяется за пределы шейки матки, соответствует I стадии) пятилетняя выживаемость составляет 92%.
- При опухолях, которые распространились на близлежащие структуры (стадии II, III и IVA) — 56%.
- При метастатическом раке (стадия IVB) — 17%.
- Средняя пятилетняя выживаемость при всех стадиях рака шейки матки — 66%.
Несмотря на низкие показатели пятилетней выживаемости, рак с метастазами — это не повод опускать руки. Существуют методы лечения, которые помогают затормозить прогрессирование заболевания, продлить жизнь, справиться с мучительными симптомами. Врачи в Европейской клинике знают, как помочь.
Цены на лечение рака шейки матки
- Консультация онколога — 5100 руб.
- Консультация химиотерапевта — 6900 руб.
- Конизация шейки матки — 26 100 руб.
- Влагалищная экстирпация матки — 154 600 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 15 000 руб.
Источник
Комментарии
Опубликовано в журнале:
Мир Медицины »» №7-8’2000 »» Новая медицинская энциклопедия Существует два основных метода лечения больных раком шейки матки (РШМ): лучевая терапия и хирургическое лечение. При отсутствии метастазов в регионарные лимфатические узлы у более чем 90% пациенток они позволяют добиться стойкого излечения. У большинства (75-80%) пациенток с РШМ лучевая терапия (ЛТ) используется в качестве самостоятельного метода:
1. Предоперационная ЛТ – применяется у пациенток, когда есть шанс перевода неоперабельной опухоли в операбельную (используется внутриполостное облучение).
2. Послеоперационная ЛТ – выполняется в случаях обнаружения метастазов в регионарных лимфатических узлах или разрастания опухоли за пределы шейки матки (используется дистанционное облучение).
К сожалению, у 20-30% больных РШМ после ЛТ вследствие различных причин формируются лучевые повреждения (ЛП) прямой кишки и мочевого пузыря. Они могут возникать сразу непосредственно после лучевой терапии или в сроки свыше 3-х месяцев после окончания курса (поздние лучевые поражения).
По клиническим проявлениям ЛП прямой кишки и мочевого пузыря различаются на легкие (катаральные, эрозивные) и тяжелые (язвенные и свищевые).
К числу основных факторов, которые определяют вероятность возникновения и степень тяжести ЛП, относятся:
- величина суммарной поглощенной дозы;
- режим фракционирования дозы;
- объем облучаемых тканей;
- сопутствующие заболевания, прежде всего органов, входящих в зону облучения;
- индивидуальная радиочувствительность тканей у конкретной пациентки.
В 1984 году Г.М. Жаринов и А.А. Габелов разработали систему прогнозирования ЛП прямой кишки и мочевого пузыря, которая на основе анализа современной ЛТ больных РШМ была усовершенствована в 2000 году (Г.М. Жаринов, В.Л. Винокуров, Г.В. Заикин, А.В. Зорин). Система позволила не только с высокой надежностью определять вероятность возникновения поздних лучевых повреждений у конкретной пациентки с РШМ, но и начать разработку программы активной профилактики ЛП у больных с высоким риском их возникновения и поиск новых методов лечения.
Профилактика
Первым шагом в данном направлении было использование локальной радиомодификации (Г.М. Жаринов, 1993). В клинике Центрального научно-исследовательского рентгенорадиологического института МЗ РФ (ЦНИИРИ МЗ РФ) была разработана система мероприятий по активной профилактике поздних ЛП прямой кишки и мочевого пузыря. Она включает в себя:
- коррекцию общесоматического статуса больных;
- общеукрепляющую терапию, направленную на активизацию иммунозащитных систем организма;
- симптоматическую терапию сопутствующих заболеваний;
- нормализацию функций желудочно-кишечного тракта;
- диагностику и лечение воспалительных процессов урогенитальных органов;
- лечебную физкультуру;
- психотерапию, социальную адаптацию;
- местное применение (внутрипузырное и/или интраректальное) лечебных препаратов (дибунол, смеси витаминов, гидрокортизон, антибиотики, аналгетики, диметилсульфоксид и пр.).
В период с 1979 по 1996 год среди 169 больных РШМ, подвергавшихся ЛТ в клинике ЦНИИРИ МЗ РФ, были выделены группы пациенток с высоким риском возникновения поздних ЛП прямой кишки и мочевого пузыря. С момента завершения ЛТ им проводились курсы активной профилактики общей продолжительностью 2 года. В результате частота и степень тяжести ЛП существенно снизились: поздние лучевые ректиты зарегистрированы у 7 из 52 (13.5%) больных, то есть частота их возникновения в 2.5 раза ниже, чем у женщин, не получавших активную профилактику лучевых поражений после ЛТ; поздние ЛП мочевого пузыря возникли у 6 из 25 (24%) пациенток, в отличие от 40% в группе пациенток, не получавших активную профилактику.
Подобные результаты свидетельствуют о том, что осуществление относительно несложных и недорогостоящих мероприятий у больных РШМ с высоким риском возникновения ЛП, начатое сразу после курса ЛТ, позволяет значительно снизить частоту и степень тяжести поздних ректитов и циститов.
Новые подходы к лечению
Лечение сформировавшихся ЛП прямой кишки и мочевого пузыря представляет серьезную проблему и требует комплексного подхода. Общепринятой для лечения подобных осложнений является методика, разработанная в ЦНИРРИ МЭ РФ (А.А. Габелов, 1970). Она включает в себя коррекцию соматического состояния больной, нормализацию функций кишечника, санацию мочевыводящих путей, а также местного (внутрипузырного и/или интраректального) применения лечебных препаратов. Стандартный курс лечения продолжается 3-4 недели.
Известно, что при проведении лучевой терапии ослабляются репаративные процессы в окружающих опухоль тканях и органах. У онкологических больных значительно снижаются процессы адаптации. В последние десятилетия в клинической практике достаточно широко применяется низкоинтенсивное лазерное излучение. Оно обладает метаболическим, противовоспалительным, анальгетическим, иммуномодулирующим, денсенсибилизирующим и бактерицидным действием. На фоне лазерного воздействия более выражена пролиферация элементов соединительной ткани и эпителия, усиление фибринолитической активности крови, более интенсивное заживление ран (Kleinkort, Foley, 1984; В.П. Арсютов,1989; Гуща с соавт., 1989; А.К. Полонский, 1995). Эффект лазерного воздействия опосредуется сложной гаммой процессов, в числе которых доминируют реакции организма, ответственные за клеточную адаптацию и повышение регенераторного потенциала. Низкоинтенсивный лазер использовался нами для лечения поздних лучевых повреждений прямой кишки и мочевого пузыря у больных раком шейки матки, подвергшихся сочетанной лучевой терапии в различных клиниках Санкт-Петербурга в период с 1979 по 1996 годы. Лазеротерапия применялась у пациенток с катаральными и эрозивно-десквамативными ректитами и циститами. Такой выбор определялся тем, что эффективность лечения ЛП легкой и средней степени тяжести может быть оценена количественно по срокам достижения клинического результата, а также по частоте последующих обострений.
Рак шейки матки является одной из наиболее распространенных опухолей у женщин. На земном шаре ежегодно выявляется около 500 тыс. новых случаев этого заболевания. В 90-95% случаев опухоль имеет гистологическое строение плоско-клеточного рака, в 3-5% – аденокарциномы.
В зависимости от метода лечения все больные были разделены на три группы. Каждая группа состояла из 20 пациенток (10 с катаральными и 10 с эрозивными ректитами и циститами), выбор методики лечения осуществлялся методом “слепого” отбора.
Первой группе пациенток проводилось лечение по стандартной методике. Во второй группе, помимо стандартной терапии, осуществлялось локальное воздействие низкоинтенсивным лазером “Узор-Янис” с длиной волны 890 нм. Использование матричного излучателя с 16 световодами позволило увеличить площадь лазерного воздействия и сместить в глубину область энергетического максимума (Л.Г. Малышева с соавт., 1998). Зонами лазерного воздействия являлись надлобковая и крестцово-ягодичная области. Сеанс лазеротерапии на каждую область продолжался 10 минут, всего за курс лечения проводилось 12-15 лазерных воздействий.
В третьей группе пациенток стандартная – “базовая” – терапия и локальная лазеротерапия сочетались с системным лазерным воздействием, зонами которого были область грудины, шейный, грудной и поясничный отделы позвоночника, подвздошные и седалищные кости, а также кубитальная вена. Продолжительность лазеротерапии на каждую зону составляла 10 минут, курс лечения также состоял из 12-15 сеансов.
В качестве критериев эффекта оценивались сроки исчезновения клинических симптомов лучевых повреждений. Момент полного прекращения болей, макрогематурии и выделения крови из прямой кишки считался началом ремиссии. Все больные после завершения лечения наблюдались не менее двух лет с контрольными осмотрами через 2-3 месяца. Частота обострений, а также время их наступления также являлись количественными характеристиками эффективности проведенного лечения. Среди 20 больных первой группы у 18 (90%) в результате проведенного лечения удалось полностью ликвидировать клинические проявления лучевых повреждений. Средний срок наступления полной ремиссии составил 25+/-4 сут.
Во второй и третьей группах у всех больных удалось добиться наступления полной клинической ремиссии в сроки соответственно 16+/-2 и 10+/-2 сут. По частоте полных ремиссий различий между группами не было. Средние сроки наступления ремиссии достоверно (р<0,05) различались между всеми сравниваемыми группами.
Различия в эффективности методов лечения лучевых повреждений были особенно наглядными при сопоставлении таких показателей, как частота обострений и сроки их наступления. При наблюдении в течение двух лет клиника лучевых ректитов и циститов возобновилась у 8 (40%) больных I группы, 4 (20%) – II и лишь у 2 пациенток (10%) III группы. При этом средняя продолжительность ремиссии у этих больных составила соответственно 146+/-11, 188+/-10 и 264+/-36 сут. Различия в частоте обострений и сроках их наступления между всеми группами были статистически значимыми (р<0.05).
Результаты исследования свидетельствуют о том, что низкоинтенсивная лазеротерапия является эффективным дополнением стандартного лечения поздних лучевых повреждений прямой кишки и мочевого пузыря. Локальное лазерное воздействие приводит к сокращению сроков достижения положительного эффекта, снижению частоты повторных обострений, а также к увеличению продолжительности между началом ремиссии и обострением лучевых повреждений. Системная лазеротерапия, включающая воздействие на основные зоны костно-мозгового кроветворения, приводит к еще более выраженным положительным эффектам.
Г.М. Жариков – д-р мед. наук, профессор ЦНИРРИ МЗ РФ;
В.Л. Винокуров – д-р мед. наук, профессор ЦНИРРИ МЗ РФ;
Г.В. Заикин – врач высшей категории, ТМО N2 Санкт-Петербурга
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
