Рак шейки матки дыра в мочевом пузыре

Комментарии
Опубликовано в журнале:
Мир Медицины »» №7-8’2000 »» Новая медицинская энциклопедия Существует два основных метода лечения больных раком шейки матки (РШМ): лучевая терапия и хирургическое лечение. При отсутствии метастазов в регионарные лимфатические узлы у более чем 90% пациенток они позволяют добиться стойкого излечения. У большинства (75-80%) пациенток с РШМ лучевая терапия (ЛТ) используется в качестве самостоятельного метода:
1. Предоперационная ЛТ – применяется у пациенток, когда есть шанс перевода неоперабельной опухоли в операбельную (используется внутриполостное облучение).
2. Послеоперационная ЛТ – выполняется в случаях обнаружения метастазов в регионарных лимфатических узлах или разрастания опухоли за пределы шейки матки (используется дистанционное облучение).
К сожалению, у 20-30% больных РШМ после ЛТ вследствие различных причин формируются лучевые повреждения (ЛП) прямой кишки и мочевого пузыря. Они могут возникать сразу непосредственно после лучевой терапии или в сроки свыше 3-х месяцев после окончания курса (поздние лучевые поражения).
По клиническим проявлениям ЛП прямой кишки и мочевого пузыря различаются на легкие (катаральные, эрозивные) и тяжелые (язвенные и свищевые).
К числу основных факторов, которые определяют вероятность возникновения и степень тяжести ЛП, относятся:
- величина суммарной поглощенной дозы;
- режим фракционирования дозы;
- объем облучаемых тканей;
- сопутствующие заболевания, прежде всего органов, входящих в зону облучения;
- индивидуальная радиочувствительность тканей у конкретной пациентки.
В 1984 году Г.М. Жаринов и А.А. Габелов разработали систему прогнозирования ЛП прямой кишки и мочевого пузыря, которая на основе анализа современной ЛТ больных РШМ была усовершенствована в 2000 году (Г.М. Жаринов, В.Л. Винокуров, Г.В. Заикин, А.В. Зорин). Система позволила не только с высокой надежностью определять вероятность возникновения поздних лучевых повреждений у конкретной пациентки с РШМ, но и начать разработку программы активной профилактики ЛП у больных с высоким риском их возникновения и поиск новых методов лечения.
Профилактика
Первым шагом в данном направлении было использование локальной радиомодификации (Г.М. Жаринов, 1993). В клинике Центрального научно-исследовательского рентгенорадиологического института МЗ РФ (ЦНИИРИ МЗ РФ) была разработана система мероприятий по активной профилактике поздних ЛП прямой кишки и мочевого пузыря. Она включает в себя:
- коррекцию общесоматического статуса больных;
- общеукрепляющую терапию, направленную на активизацию иммунозащитных систем организма;
- симптоматическую терапию сопутствующих заболеваний;
- нормализацию функций желудочно-кишечного тракта;
- диагностику и лечение воспалительных процессов урогенитальных органов;
- лечебную физкультуру;
- психотерапию, социальную адаптацию;
- местное применение (внутрипузырное и/или интраректальное) лечебных препаратов (дибунол, смеси витаминов, гидрокортизон, антибиотики, аналгетики, диметилсульфоксид и пр.).
В период с 1979 по 1996 год среди 169 больных РШМ, подвергавшихся ЛТ в клинике ЦНИИРИ МЗ РФ, были выделены группы пациенток с высоким риском возникновения поздних ЛП прямой кишки и мочевого пузыря. С момента завершения ЛТ им проводились курсы активной профилактики общей продолжительностью 2 года. В результате частота и степень тяжести ЛП существенно снизились: поздние лучевые ректиты зарегистрированы у 7 из 52 (13.5%) больных, то есть частота их возникновения в 2.5 раза ниже, чем у женщин, не получавших активную профилактику лучевых поражений после ЛТ; поздние ЛП мочевого пузыря возникли у 6 из 25 (24%) пациенток, в отличие от 40% в группе пациенток, не получавших активную профилактику.
Подобные результаты свидетельствуют о том, что осуществление относительно несложных и недорогостоящих мероприятий у больных РШМ с высоким риском возникновения ЛП, начатое сразу после курса ЛТ, позволяет значительно снизить частоту и степень тяжести поздних ректитов и циститов.
Новые подходы к лечению
Лечение сформировавшихся ЛП прямой кишки и мочевого пузыря представляет серьезную проблему и требует комплексного подхода. Общепринятой для лечения подобных осложнений является методика, разработанная в ЦНИРРИ МЭ РФ (А.А. Габелов, 1970). Она включает в себя коррекцию соматического состояния больной, нормализацию функций кишечника, санацию мочевыводящих путей, а также местного (внутрипузырного и/или интраректального) применения лечебных препаратов. Стандартный курс лечения продолжается 3-4 недели.
Известно, что при проведении лучевой терапии ослабляются репаративные процессы в окружающих опухоль тканях и органах. У онкологических больных значительно снижаются процессы адаптации. В последние десятилетия в клинической практике достаточно широко применяется низкоинтенсивное лазерное излучение. Оно обладает метаболическим, противовоспалительным, анальгетическим, иммуномодулирующим, денсенсибилизирующим и бактерицидным действием. На фоне лазерного воздействия более выражена пролиферация элементов соединительной ткани и эпителия, усиление фибринолитической активности крови, более интенсивное заживление ран (Kleinkort, Foley, 1984; В.П. Арсютов,1989; Гуща с соавт., 1989; А.К. Полонский, 1995). Эффект лазерного воздействия опосредуется сложной гаммой процессов, в числе которых доминируют реакции организма, ответственные за клеточную адаптацию и повышение регенераторного потенциала. Низкоинтенсивный лазер использовался нами для лечения поздних лучевых повреждений прямой кишки и мочевого пузыря у больных раком шейки матки, подвергшихся сочетанной лучевой терапии в различных клиниках Санкт-Петербурга в период с 1979 по 1996 годы. Лазеротерапия применялась у пациенток с катаральными и эрозивно-десквамативными ректитами и циститами. Такой выбор определялся тем, что эффективность лечения ЛП легкой и средней степени тяжести может быть оценена количественно по срокам достижения клинического результата, а также по частоте последующих обострений.
Рак шейки матки является одной из наиболее распространенных опухолей у женщин. На земном шаре ежегодно выявляется около 500 тыс. новых случаев этого заболевания. В 90-95% случаев опухоль имеет гистологическое строение плоско-клеточного рака, в 3-5% – аденокарциномы.
В зависимости от метода лечения все больные были разделены на три группы. Каждая группа состояла из 20 пациенток (10 с катаральными и 10 с эрозивными ректитами и циститами), выбор методики лечения осуществлялся методом “слепого” отбора.
Первой группе пациенток проводилось лечение по стандартной методике. Во второй группе, помимо стандартной терапии, осуществлялось локальное воздействие низкоинтенсивным лазером “Узор-Янис” с длиной волны 890 нм. Использование матричного излучателя с 16 световодами позволило увеличить площадь лазерного воздействия и сместить в глубину область энергетического максимума (Л.Г. Малышева с соавт., 1998). Зонами лазерного воздействия являлись надлобковая и крестцово-ягодичная области. Сеанс лазеротерапии на каждую область продолжался 10 минут, всего за курс лечения проводилось 12-15 лазерных воздействий.
В третьей группе пациенток стандартная – “базовая” – терапия и локальная лазеротерапия сочетались с системным лазерным воздействием, зонами которого были область грудины, шейный, грудной и поясничный отделы позвоночника, подвздошные и седалищные кости, а также кубитальная вена. Продолжительность лазеротерапии на каждую зону составляла 10 минут, курс лечения также состоял из 12-15 сеансов.
В качестве критериев эффекта оценивались сроки исчезновения клинических симптомов лучевых повреждений. Момент полного прекращения болей, макрогематурии и выделения крови из прямой кишки считался началом ремиссии. Все больные после завершения лечения наблюдались не менее двух лет с контрольными осмотрами через 2-3 месяца. Частота обострений, а также время их наступления также являлись количественными характеристиками эффективности проведенного лечения. Среди 20 больных первой группы у 18 (90%) в результате проведенного лечения удалось полностью ликвидировать клинические проявления лучевых повреждений. Средний срок наступления полной ремиссии составил 25+/-4 сут.
Во второй и третьей группах у всех больных удалось добиться наступления полной клинической ремиссии в сроки соответственно 16+/-2 и 10+/-2 сут. По частоте полных ремиссий различий между группами не было. Средние сроки наступления ремиссии достоверно (р<0,05) различались между всеми сравниваемыми группами.
Различия в эффективности методов лечения лучевых повреждений были особенно наглядными при сопоставлении таких показателей, как частота обострений и сроки их наступления. При наблюдении в течение двух лет клиника лучевых ректитов и циститов возобновилась у 8 (40%) больных I группы, 4 (20%) – II и лишь у 2 пациенток (10%) III группы. При этом средняя продолжительность ремиссии у этих больных составила соответственно 146+/-11, 188+/-10 и 264+/-36 сут. Различия в частоте обострений и сроках их наступления между всеми группами были статистически значимыми (р<0.05).
Результаты исследования свидетельствуют о том, что низкоинтенсивная лазеротерапия является эффективным дополнением стандартного лечения поздних лучевых повреждений прямой кишки и мочевого пузыря. Локальное лазерное воздействие приводит к сокращению сроков достижения положительного эффекта, снижению частоты повторных обострений, а также к увеличению продолжительности между началом ремиссии и обострением лучевых повреждений. Системная лазеротерапия, включающая воздействие на основные зоны костно-мозгового кроветворения, приводит к еще более выраженным положительным эффектам.
Г.М. Жариков – д-р мед. наук, профессор ЦНИРРИ МЗ РФ;
В.Л. Винокуров – д-р мед. наук, профессор ЦНИРРИ МЗ РФ;
Г.В. Заикин – врач высшей категории, ТМО N2 Санкт-Петербурга
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Качество жизни при раке матки. Осложнения
Обструкция мочеточников при раке шейки матки поздних стадий. Больные с двусторонним сдавленней мочеточников и уремией вследствие прогрессирования рака шейки матки (РШМ) и рака эндометрия (РЭ) представляют серьезную проблему для врачей. Этих женщин желательно разделить на две группы:
1) не получавших ранее ЛТ;
2) с рецидивом заболевания после тазовой ЛТ.
Отличие сдавления мочеточников, вызванного РЭ, от их обструкции при РШМ заключается в том, что в первом случае причина чаще всего связана с распространением процесса за пределами таза, что создает более трудные условия для лечения. Кроме того, при использовании стандартной брахитерапии необходимые дозы облучения сложнее подвести к телу матки, чем к шейке. Этим обусловлен более низкий эффект лечения больных РЭ с помощью ЛТ.
Двустороннее сдавление мочеточников вследствие нелеченного злокачественного новообразования или рецидива рака после хирургического лечения считают серьезным показанием для отвода мочи с последующей адекватной ЛТ. Процент успешных исходов в этой ситуации низкий. Поэтому, несмотря на то что поддерживающая терапия не может остановить прогрессирование уремии и летального исхода, она должна рассматриваться как альтернатива более агрессивному лечению.
Если от поддерживающей терапии в качестве единственного метода воздержались и выбрали активную тактику ведения больной, первым делом следует попытаться установить ретроградные мочеточниковые стенты во время цистоскопии. Если эта попытка не удалась, выполняют чрескожную нефростомию, а затем стент устанавливают антеградно. Третий вариант хирургического отведения мочи заключается в формировании мочевого проводника из петли подвздошной кишки, в которую имплантируют мочеточники, а дистальный конец выводят на кожу (операция Бриккера), либо в создании мочевого резервуара из сегмента кишечника.
Как правило, отведение мочи выполняют до начала ЛТ, что позволяет во время лапаротомии оценить распространенность заболевания. Если обнаруживают метастазы за пределами таза, тактику изменяют, т. к. шансы на выздоровление значительно снижены.
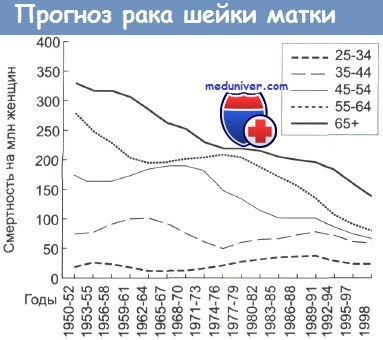
Смертность от цервикального рака в зависимости от возраста женщин.
Больные с двусторонней обструкцией мочеточников после полного курса тазовой ЛТ представляют еще более сложную проблему. Менее чем у 5 % из них сдавление мочеточников вызвано радиационным фиброзом; эту группу больных очень сложно выявить. Для того чтобы исключить рецидив заболевания, выполняют обследование под наркозом: цистоскопию, ректороманоскопию и множественные биопсии.
Если рецидив опухоли не обнаружен, отведение мочи спасает жизнь больной. Поэтому всех больных с двусторонним сдавленней мочеточников после курса облучения необходимо тщательно обследовать с целью дифференциальной диагностики лучевого фиброза и рецидива злокачественного новообразования.
Если доказано, что причина двусторонней обструкции мочеточников обусловлена рецидивом заболевания, решение о дальнейшем лечении — трудная и, в какой-то степени, умозрительная задача. Многочисленные исследования указывают на то, что отведение мочи не обеспечивает приемлемое качество жизни этой группе больных. Brin и соавт. сообщили о 47 больных (5 из них с диагнозом РШМ), которым в связи с обструкцией мочеточников вследствие распространенных злокачественных опухолей, локализованных в тазу, выполнено отведение мочи.
Результаты неутешительны: медиана выживаемости составила 5,3 мес; 50 % больных прожили 3 мес. и только 20 % — 6 мес; после отвода мочи 63,8 % времени оставшейся жизни приходилось па стационар. Delgado сообщил о незначительном увеличении выживаемости больных с выявленными рецидивными опухолями в тазу и почечной недостаточностью, которым проведено отведение мочи. Автор полагает, что не следует прибегать к этой операции, т. к. она исключает более легкую смерть от уремии.
Очевидно, решение об операции следует принимать вместе с семьей и даже, по возможности, с больной. После отведения мочи наблюдается усиление других симптомов рецидива заболевания, вызывающих страдания: мучительной боли в тазу, повторных инфекций и кровотечений. Боль и прогрессирующая кахексия тяготят и больную, и врача. Массивные тазовые кровотечения поднимают непростую в этих ситуациях проблему переливания крови. Неизбежно увеличивается время пребывания в стационаре, а следовательно, финансовые затраты семьи больной достигают огромного размера.

Свищи при раке шейки матки поздних стадий
Свищи ободочной кишки и мочевых путей — типичные осложнения прогрессирующего рака шейки матки (РШМ) и рака эндометрия (РЭ), которые значительно ухудшают качество жизни. Лечение всегда начинают с отведения мочи или кала, что уменьшает соответствующую симптоматику. Постоянная катетеризация мочевого пузыря устраняет недержание мочи, обусловленное наличием свища, что отменяет необходимость хирургического вмешательства. Ушивание свища мочеточника с чрескожной нефростомией — второй вариант лечения.
Однако для эффективного отведения мочи требуется сформировать мочевой резервуар или выполнить другие хирургические вмешательства. Существующие методы хирургической коррекции свищей мочевых путей, возникших вследствие рецидива рака или облучения, редко дают удовлетворительные результаты.
Паллиативное лечение влагалищно-толстокишечного свища сводится к наложению колостомы. Согласно мнению одних хирургов, петлевая колостома обеспечивает адекватное опорожнение кишечника и препятствует выделению кала через свищ. Другие отдают предпочтение одноствольной колостоме, утверждая, что ушивание культи кишки, как при операции Хартманна, полностью блокирует попадание кала во влагалище. При любой ситуации требуется мини-лапаротомия, во время которой и определяют объем операции.
Сексуальная дисфункция при раке шейки матки поздних стадий
Лечение женщин со злокачественными новообразованиями половых органов может осложниться патологическими изменениями влагалища, вызывающими сексуальные расстройства. Чаще они развиваются после лечения рака вульвы, влагалища и РШМ по сравнению с РЭ и РЯ. Это объясняется более частым применением комбинированного лечения (радикальных хирургических операций и ЛТ) при лечении первых трех локализаций опухолей. Согласно публикациям, частота сексуальных расстройств после хирургического лечения, ЛТ или комбинации обоих методов колеблется в широких пределах.
На сухость и укорочение влагалища после радикальной гистерэктомии жалуется 17—58 и 4—100 % женщин соответственно. До настоящего времени точные данные о частоте уменьшения эластичности влагалища и притока крови к наружным половым органам во время полового возбуждения у перенесших эту операцию отсутствовали. В 1999 г. в Швеции выполнено ретроспективное исследование у 256 больных РШМ, закончивших лечение, в сравнении с 350 женщинами группы контроля; результаты опубликованы в журнале «New England Journal of Medicine». Обнаружено статистически значимое снижение эластичности влагалища у 23 % женщин, получивших лечение по поводу начального РШМ, по сравнению с контрольной группой (4 %).
Кроме того, зафиксировано укорочение влагалища после лечения и снижение увлажнения во время полового акта. Женщины жаловались, что эти изменения отрицательно влияют на половую жизнь и вызывают глубокие переживания. Тем не менее частота оргазмов была одинаковой в обеих группах, но диспареуния наблюдалась чаще у женщин, перенесших РШМ. Наконец, данное ретроспективное исследование не выявило статистически значимых различий в количестве сексуальных расстройств между женщинами, перенесшими радикальную операцию и ЛТ. В других же аналогичных исследованиях обнаружено существенное превалирование сексуальных дисфункций у женщин, получивших ЛТ, по сравнению с теми, кто перенес хирургическое лечение РШМ.
Важно учитывать и сравнивать не только результаты лечения рака шейки матки (РШМ), полученные с помощью лучевого или хирургического метода, но и показатели качества жизни и половой функции. Рекомендуют регулярно проводить бужирование влагалища после ЛТ с целью сохранить его длину и эластичность. Заметим, что эффективность этого вмешательства в проспективных исследованиях не изучена. Грамотное назначение ЗГТ и мазей улучшает качество половой жизни у этих женщин.
Следует выявлять и лечить диспареунию, возникающую после лечения злокачественных опухолей женских половых органов, т. к. она ведет к снижению либидо, а это ухудшает отношения между женщиной и ее партнером. Потеря полового влечения женщинами, перенесшими онкологическое заболевание, — типичное явление, представляющее сложную проблему. Спустя длительное время после улучшения общего состояния женщины жалуются на снижение полового влечения или его отсутствие. Психологическая помощь и участие в группах поддержки могут быть полезными в решении этой омрачающей жизнь проблемы.
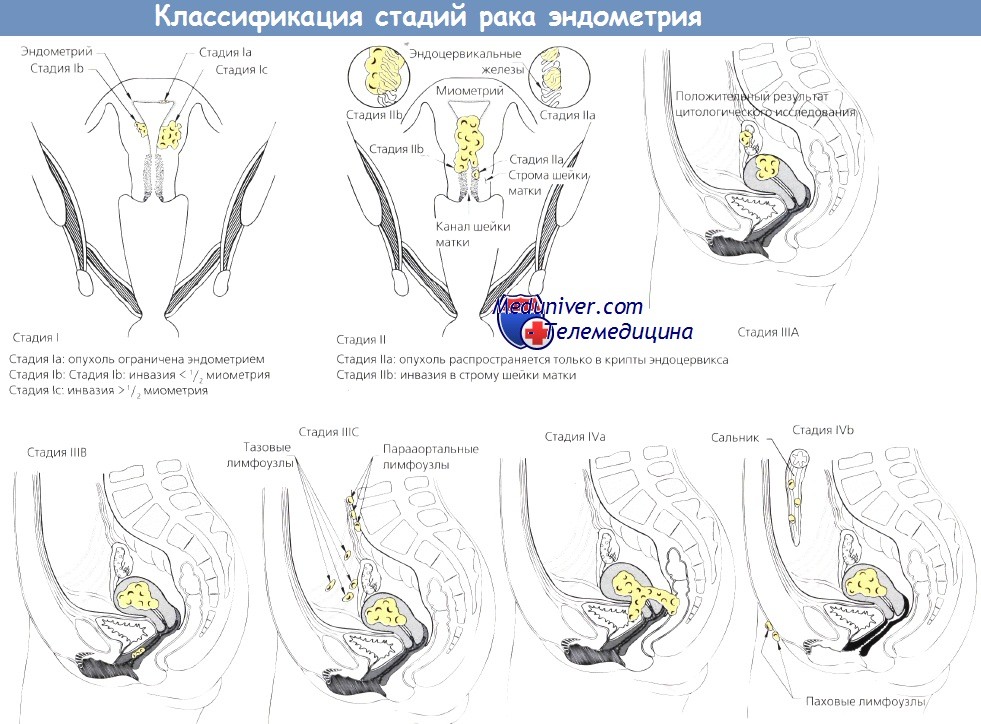
Классификация стадий рака эндометрия

– Также рекомендуем “Принятие решения по лечению онкологического больного в США в конце жизни”
Оглавление темы “Симптоматическое лечение рака”:
- Помощь при тошноте и рвоте у онкологического больного
- Помощь при поносе и запоре у онкологического больного
- Правила сообщения пациенту об онкологическом заболевании
- Психосоциальные проблемы больных раком
- Качество жизни при раке яичников поздних стадий. Осложнения
- Качество жизни при раке матки. Осложнения
- Принятие решения по лечению онкологического больного в США в конце жизни
- Принятие решения о бесполезности лечения рака
- Хосписы для онкологических больных – условия, требования
Источник
