Последствия внутрипузырной химиотерапии мочевого пузыря
Лечение рака мочевого пузыря (стадии Та, T1, Cis)
Адъювантная химио- и иммунотерапия
Несмотря на то что радикально выполненная ТУР, как правило, позволяет полностью удалить поверхностные опухоли мочевого пузыря, тем не менее, они часто (в 30-80% случаев) рецидивируют, а у части больных заболевание прогрессирует.
На основании результатов 24 рандомизированных исследований, в которых участвовали 4863 больных с поверхностными опухолями мочевого пузыря, Европейская организация по исследованию и лечению рака мочевого пузыря в 2007 г. разработала методику проспективной оценки риска рецидивирования и прогрессирования опухолей. В основе методики лежит 6-балльная система оценки нескольких факторов риска: количество опухолей, максимальные размеры опухоли, частота рецидивов в анамнезе, стадия заболевания, наличие CIS, степень дифференциации опухоли. По сумме этих баллов определяют риск рецидивирования или прогрессирования заболевания в %.
Система расчёта факторов риска рецидивирования и прогрессирования поверхностных опухолей мочевого пузыря
Фактор риска | Рецидивирование | Прогрессирование |
Количество опухолей | ||
Единственная | ||
От 2 до 7 | 3 | 3 |
28 | б | 3 |
Диаметр опухоли | ||
23 см | 3 | 3 |
Отмечаемое ранее рецидивирование | ||
первичный рецидив | ||
менее 1 рецидива в год | 2 | 2 |
более 1 рецидива в год | 4 | 2 |
Стадия заболевания | ||
Та | ||
Т1 | 1 | 4 |
CIS | ||
Нет | ||
Есть | 1 | 6 |
Степень дифференцировки | ||
G1 | ||
G2 | 1 | |
G3 | 2 | 5 |
Всего баллов | 0-17 | 0-23 |
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11]
Группы поверхностных опухолей мочевого пузыря в соответствии с факторами риска
- Опухоли малого риска:
- единственные;
- Та;
- высокодифференцированные;
- размером
- Опухоли высокого риска:
- Т1;
- низкодифференцированные;
- множественные;
- высокорецидивные;
- CIS.
- Опухоли промежуточного риска:
- Та-Т1;
- среднедифференцированные;
- множественные;
- размером >3 см.
Из приведённых выше данных становится понятной необходимость адъювантной химио- или иммунотерапии после ТУР мочевого пузыря практически у всех больных с поверхностным раком.
Цели и предположительные механизмы местной химио- и иммунотерапии заключаются в предупреждении имплантации раковых клеток в ранние сроки после ТУР. уменьшении возможности рецидивирования или прогрессирования заболевания и абляции резидуальной опухолевой ткани при неполном её удалении («гемиреэекция»).
Внутрипузырная химиотерапия
Существуют две схемы внутрипузырной химиотерапии после ТУР мочевого пузыря по поводу поверхностного рака: однократная инсталляция в ранние сроки после операции (в течение первых 24 ч) и адъювантное многократное введение химиопрепарата.
Однократная инстилляция в ранние сроки после операции
Для внутрипузырной химиотерапии с одинаковым успехом применяют митомицин, эпирубицин и доксорубицин. Внутрипузырное введение химиопрепаратов осуществляют при помощи уретрального катетера. Препарат разводят в 30-50 мл 0.9% раствора натрия хлорида (или дистиллированной воды) и вводят в мочевой пузырь на 1-2 ч. Обычные дозы для митомицина составляют 20-40 мг, для эпирубицина – 50-80 мг. для доксорубицина 50 мг. С целью предупреждения разведения препарата мочой больным в день инстилляции резко ограничивают приём жидкости. Для лучшего контакта химиопрепарата со слизистой оболочкой мочевого пузыря рекомендуют часто менять положение тела до мочеиспускания.
При использовании митомицина следует учитывать возможность аллергической реакции с покраснением кожи ладоней и гениталий (у 6% больных), что легко предупредить тщательным мытьём рук и гениталий сразу же вслед за первым мочеиспусканием после инстилляции препарата. Серьёзные местные и даже системные осложнения обычно возникают при экстравазации препарата, поэтому ранняя инсталляция (в течение 24 ч после ТУР) противопоказана при подозрении на вне- или внутрибрюшинную перфорацию мочевого пузыря, что обычно может происходить при агрессивной ТУР мочевого пузыря.
В связи с опасностью системного (гематогенного) распространения местная химио- и иммунотерапия противопоказаны также при макрогематурии. Однократная инсталляция химиопрепарата снижает риск рецидивирования на 40-50%, на основании чего её осуществляют практически у всех больных. Однократное введение химиопрепарата в более поздние сроки уменьшает эффективность метода в 2 раза.
Снижение частоты рецидивирования происходит в течение 2 лет, что имеет особое значение у больных с малым онкологическим риском, для которых однократная инсталляция стала основным методом метафилактики. Однако однократная инсталляция недостаточна при среднем и, особенно, высоком онкологическом риске, и такие больные в связи с большой вероятностью рецидивирования и прогрессирования заболевания нуждаются в дополнительной адъювантной химио- или иммунотерапии.
Адъювантное многократное введение химиопрепарата
Лечение рака мочевого пузыря заключается в многократном внутрипузырном введении тех же химиопрепаратов. Химиотерапия эффективна с точки зрения уменьшения риска рецидивирования. но недостаточно эффективна для предупреждения прогрессирования опухоли. Данные об оптимальной продолжительности и частоте внутрипузырной химиотерапии противоречивы. Согласно рандомизированному исследованию
Европейской организации по исследованию и лечению рака мочевого пузыря, ежемесячная инсталляция в течение 12 мес не улучшала результаты лечения по сравнению с таковой в течение 6 мес при условии, что первую инсталляцию осуществляли сразу после ТУР Согласно другим рандомизированным исследованиям. частота рецидивирования при годовом курсе лечения (19 инсталляций) была ниже по сравнению с 3-месячным курсом (9 инстилляции) приёма эпирубицина.
[12], [13], [14], [15], [16], [17], [18], [19], [20], [21], [22], [23], [24]
Внутрипузырная иммунотерапия
Для больных с поверхностным раком мочевого пузыря с высоким риском рецидивирования и прогрессирования наиболее эффективный метод метафилактики внутрипузырная иммунотерапия вакциной БЦЖ, введение которой приводит к выраженному иммунному ответу: в моче и стенке мочевого пузыря происходит экспрессия цитокинов (интерферон у, интерлейкин-2 и др.). стимуляция клеточных факторов иммунитета. Этот иммунный ответ активирует цитотоксические механизмы, которые составляют основу эффективности БЦЖ в предупреждении рецидивирования и прогрессирования заболевания.
Вакцина БЦЖ состоит из ослабленных микобактерий. Её разработали в качестве вакцины для туберкулёза, но она также обладает противоопухолевой активностью. Вакцина БЦЖ – лиофилизированный порошок, который хранят в замороженном виде. Её выпускают различные фирмы, но все производители используют культуру микобактерий. полученную в институте Пастера во Франции.
Вакцину БЦЖ разводят в 50 мл 0,9% раствора натрия хлорида и сразу же вводят в мочевой пузырь по уретральному катетеру под силой тяжести раствора. Адъювантное лечение рака мочевого пузыря начинают через 2-4 нед после ТУР мочевого пузыря (время, необходимое для реэпителизации) для уменьшения риска гематогенного распространения живых бактерий. В случае травматичной катетеризации процедуру инстилляции откладывают на несколько дней. После инстилляции в течение 2 ч больной не должен мочиться, необходимо часто менять положение тела для полноценного взаимодействия препарата со слизистой оболочкой мочевого пузыря (повороты с одного бока на другой). В день инстилляции следует прекратить приём жидкости и диуретиков для уменьшения разведения препарата мочой.
Больных следует предупредить о необходимости мытья унитаза после мочеиспускания, хотя риск бытовой контаминации считают гипотетическим. Несмотря на преимущества БЦЖ по сравнению с адъювантной химиотерапией, общепризнано, что иммунотерапия рекомендована лишь больным с высоким онкологическим риском. Это связано с вероятностью развития различных, в том числе и грозных, осложнений (цистит, подъём температуры, простатит, орхит, гепатит, сепсис и даже летальный исход). Из-за развития осложнений часто приходится прекращать адъювантную терапию. Именно поэтому её назначение больным с низким онкологическим риском не оправданно.
Основные показания к назначению вакцины БЦЖ:
- CIS;
- наличие резидуальной опухолевой ткани после ТУР;
- метафилактика рецидивиривания опухолей у больных с высоким онкологическим риском.
Большое значение придают применению вакцины БЦЖ у больных с высоким риском прогрессирования заболевания, так как доказано, только этот препарат способен уменьшить риск или отстрочить прогрессирование опухоли.
Абсолютные противопоказания к БЦЖ-терапии:
- иммунодефицит (например, на фоне приёма цитостатиков);
- сразу после ТУР;
- макрогематурия (риск гематогенной генерализации инфекции, сепсиса и смерти);
- травматичная катетеризация.
[25], [26], [27], [28], [29], [30], [31], [32], [33], [34]
Относительные противопоказания к БЦЖ-терапии:
- инфекция мочевыводящих путей;
- заболевания печени, исключающие возможность применения изониазида в случае туберкулёзного сепсиса;
- туберкулёз в анамнезе;
- тяжёлые сопутствующие заболевания.
Классическую схему адъювантной БЦЖ-терапии эмпирически разработал Morales более 30 лет тому назад (еженедельная инсталляция в течение 6 нед). Однако в дальнейшем установили, что 6-недельного курса лечения недостаточно. Существуют несколько вариантов этой схемы: от 10 инсталляций в течение 18 нед до 30 инсталляций в течение 3 лет. Хотя оптимальная общепризнанная схема применения БЦЖ ещё не разработана, большинство экспертов сходятся во мнении, что при её хорошей переносимости продолжительность лечения должна
составлять не менее 1 года (после первого 6-недельного курса проводят повторные 3-недельные курсы через 3, 6 и 12 мес).
Рекомендации по внутрипузырной химио- или БЦЖ-терапии
- При низком или среднем риске рецндивирования и очень низком риске прогрессирования необходимо обязательно осуществлять однократную инсталляцию химнопрепарата.
- При низком или среднем риске прогрессирования независимо от степени риска рециднвнровання. после однократного введения химнопрепарата необходима поддерживающая адъювантная внутрипузырная химио- (6-12 мес) или иммунотерапия (БЦЖ в течение 1 года).
- При высоком риске прогрессирования показана внутрипузырная иммунотерапия (БЦЖ по крайней мере в течение 1 года) либо немедленная радикальная цистэктомия.
- При выборе той или иной терапии необходимо оценивать возможные осложнения.
Лечение рака мочевого пузыря (стадии Т2, ТЗ, Т4)
Лечение рака мочевого пузыря (стадии Т2, ТЗ, Т4) – системная химиотерапия рака мочевого пузыря.
Примерно у 15% больных при выявлении рака мочевого пузыря также диагностируют региональные либо отдалённые метастазы, и почти у половины больных метастазирование происходит после радикальной цистэктомии или лучевой терапии. Без дополнительного лечения выживаемость таких больных незначительная.
Основной химиопрепарат при системной химиотерапии цисплатин, однако в виде монотерапии результаты лечения значительно уступают таковым по сравнению с комбинированным применением этого препарата с метотрексатом, виноластином и доксорубицином (MVAC). Однако лечение рака мочевого пузыря MVAC сопровождается выраженной токсичностью (смертность на фоне лечения составляет 3-4%).

В последние годы предложили использовать новый химиопрепарат гемцитабин в сочетании с цисплатином, что позволило достичь аналогичных MVAC результатов при существенно меньшей токсичности.
Комбинированная химиотерапия у 40-70% больных частично или полностью эффективна, что и послужило основанием для её применения в сочетании с иистэктомией или лучевой терапией в режиме неоадъювантной или адъювантной терапии.
Неоадъювантиая комбинированная химиотерапия Показана больным со стадией Т2-Т4а до радикальной цистэктомии или лучевого лечения и направлена на лечение рака мочевого пузыря возможных микрометастазов, снижение вероятности реиидивирования. а у части больных на сохранение мочевого пузыря. Больные переносят её легче до основного лечения (цистэктомия или облучение), однако рандомизированные исследования выявили её незначительную эффективность либо отсутствие таковой. У некоторых больных (опухоль малых размеров. отсутствие гидронефроза, папиллярное строение опухоли, возможность полного визуального удаления опухоли путём ТУР) в 40% случаев адъювантная химиотерапия в сочетании с облучением позволила избежать цистэктомии, однако для подобной рекомендации необходимы рандомизированные исследования.
Адъювантная системная химиотерапия
Различные её схемы (стандартный режим MVAC, те же препараты в высоких дозах, гемцитабин в сочетании с цисплатином) находятся на стадии изучения в рандомизированном исследовании Европейской организации по исследованию и лечению рака мочевого пузыря, что пока не позволяет рекомендовать один из её вариантов.
Схема MVAC при метастатическом поражении была эффективна лишь > 15-20% больных (продление жизни только на 13 мес). При этом результаты были лучше у больных с метастазированием в региональные лимфатические узлы по сравнению с метастазированием в отдалённые органы. При неэффективности сочетания MVAC была выявлена высокая эффективность замены режима на гемцитабин и паклитаксел. В качестве первичной терапии хорошие результаты были получены при сочетании цисплатина гемцитабина и паклитаксела.
В заключении следует отметить, что системная химиотерапия не показана пои инвазивном раке мочевого пузыря без наличия метастазов. Оптимальные показания к её применению можно будет определить только после завершения рандомизированных исследований.
[35], [36], [37], [38], [39], [40], [41], [42], [43], [44], [45], [46]
Источник
Внутрипузырная химиотерапия – методика лечения рака мочевого пузыря, предполагающая введение химиопрепарата непосредственно в полость мочевого пузыря, а не внутривенно, как при стандартной химиотерапии онкологических заболеваний.

Рак мочевого пузыря у мужчин занимает 5 место среди всех онкопатологий, у женщин – 11 место.
Ведущие клиники России организуют эффективное внутрипузырное химиотерапевтическое лечение, применяя современные медикаментозные препараты. Для эффективного лечения на высоком уровне в клиниках создаются комфортные условия, осуществляется индивидуальный подход, в том числе предусмотрена психологическая поддержка наших пациентов. Опытные специалисты активно внедряют в ежедневную практику самые современные и передовые методы лечения, ориентированные на замедление и лечение онкопатологии, а также снижение риска возникновения побочных эффектов.
При диагностированном образовании мочевого пузыря, первым этапом необходимо провести ТУР мочевого пузыря (трансуретральную резекцию опухоли мочевого пузыря). Это делается для удаления основного опухолевого очага и отправки ткани на гистологическое исследования, с целью диагностики типа опухолевого роста и определения дальнейшей тактики лечения. Невзирая на совершенствование хирургических методик при лечении рака мочевого пузыря, в большинстве случаев избежать рецидива заболевания не удается. В частности, статистика демонстрирует что у 60-70% пациентов возникают рецидивы опухоли после первичного оперативного лечения.
Таким образом, проведение внутрипузырной химиотерапии при раке мочевого пузыря повышает эффективность лечения и снижает риски рецидива опухоли.
Проведение внутрипузырной химиотерапии
Препараты вводятся непосредственно в полость мочевого пузыря, обеспечивая контакт со злокачественными клетками, вызывая их гибель.
Для обеспечения более высокой концентрации химиопрепарата в мочевом пузыре перед проведением внутрипузырной химиотерапии больным рекомендуют:
- ограничить потребление жидкости;
- отказаться от приема мочегонных препаратов и напитков.
Процедура предполагает:
- введение в мочевой пузырь уретрального катетера;
- введение химиопрепарата по уретральному катетеру с последующим удалением катетера;
- пациенту рекомендуют в течение рекомендованного времени не мочиться;
- выведение химиопрепарата происходит естественным путем при самостоятельном мочеиспускании.
Внутрипузырная химиотерапия при раке мочевого пузыря отличается от внутривенной тем, что:
- химиопрепарат практически не всасывается в кровь;
- в связи с чем, отсутствуют побочные эффекты от проводимой химиотерапии (выпадение волос, тошнота, рвота).
Внутривенная химиотерапия при раке мочевого пузыря
Даже после проведения радикального оперативного лечения в объеме цистэктомии (полного удаления мочевого пузыря) существует риск рецидива заболевания. В ряде случаев, с целью повышения эффективности оперативного лечения и снижения риска рецидива и прогрессии заболевания, в современной онкоурологии применяют внутривенную химиотерапию до и после оперативного лечения.
Преимущества химиотерапии при онкологии мочевого пузыря
Ведущие клиники России, партнеры компании “Русский Доктор”, осуществляют химиотерапию при раке мочевого пузыря и имеют ряд преимуществ:
- надежность и безопасность химиотерапии (перед применением химиотерапевтического препарата проводится обязательная процедура его проверки согласно специальному протоколу);
- применение химиопрепаратов нового поколения (использование инновационных методик с применением самых современных химиопрепаратов и схем лечения, демонстрирующих наилучший результат);
- «таргетная терапия» (обеспечивает воздействие химиопрепарата непосредственного на опухолевый очаг);
- применение «препаратов прикрытия» (нашим пациентам назначают сопутствующую терапию, уменьшающую побочные эффекты основной химиотерапии).
Как правильно выбрать клинику?
Отзывы пациентов о химиотерапии, как способе лечения рака мочевого пузыря, демонстрируют успешность лечения при своевременном обращении за помощью к ведущим онкологам. Компания “Русский Доктор” помогает выбрать клинику, в которой применяют инновационные и самые современные методы лечения химиопрепаратами нового поколения.
Источник
Проведен анализ результатов лечения 77 пациентов с немышечно-инвазивным раком мочевого пузыря, подвергнутых ТУР и внутрипузырной химиотерапии. Рецидив опухоли определен после проведения внутрипузырной химиотерапии у 10,4% больных при временном диапазоне его возникновения в среднем 23,1 месяца. В 6,5% случаев отмечена прогрессия опухоли.
Выявлено, что применение немедленной (в течение 6 часов) внутрипузырной химиотерапии после ТУР немышечно-инвазивного рака мочевого пузыря ведет к значительному снижению количества рецидивов и риска прогрессии опухоли мочевого пузыря, а использование для внутрипузырной химиотерапии цисплатина наряду с митомицином обеспечивает лучшие результаты в сравнении с доксорубицином.
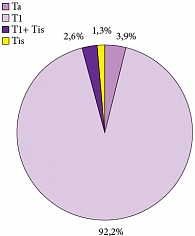
Рис. 1. Стадия опухоли
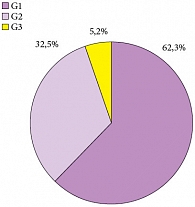
Рис. 2. Дифференцировка опухоли
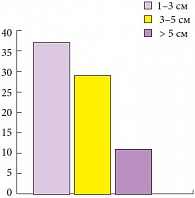
Рис. 3. Размеры опухоли
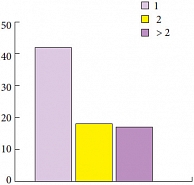
Рис. 4. Количество опухолей
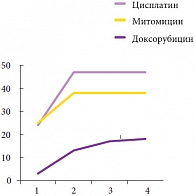
Рис. 5. Количество рецидивов опухоли
Введение
Рак мочевого пузыря является вторым по распространенности злокачественным заболеванием мочеполовой системы и второй наиболее распространенной причиной смерти среди мочеполовых опухолей. Примерно 75% новых случаев рака мочевого пузыря в США и Европе ограничиваются слизистой оболочкой и/или собственной пластинкой, тогда как в России данный показатель составляет всего 20-30%. Лечение немышечно-инвазивного рака мочевого пузыря представляет для врача и пациента значительные сложности. До 80% пациентов с немышечно-инвазивным раком мочевого пузыря требуется лечение путем трансуретральной резекции (ТУР) с внутрипузырной химио- или иммунотерапией [1]. Риск рецидива немышечно-инвазивного рака мочевого пузыря приближается к 80%. Относительное значение клинических и патологических факторов течения опухолевого процесса зависит от вида адъювантной внутрипузырной терапии.
Адъювантная внутрипузырная БЦЖ-терапия снижает риски рецидива опухоли на 30% по сравнению только с ТУР [2, 3] и продлевает время до прогрессии заболевания [3, 4]. Большинство исследователей придерживаются мнения, что для снижения риска рецидива и прогрессии немышечно-инвазивного рака мочевого пузыря необходимо проводить внутрипузырную химиотерапию непосредственно после ТУР опухоли мочевого пузыря. Риск рецидивирования опухоли статистически значимо снижается (до 16-50%) по сравнению с больными, не получавшими внутрипузырную химиотерапию (32-34%), прогрессия отмечена в 8-17% и 11-63% случаев соответственно [5-7]. Эффективность внутрипузырной химиотерапии после ТУР мочевого пузыря при немышечноинвазивном раке мочевого пузыря остается неоднозначной. В связи с этим нами был проведен анализ результатов лечения у пациентов с немышечноинвазивным раком мочевого пузыря, у которых после ТУР мо+чевого пузыря проводилась внутрипузырная химиотерапия.
Материалы и методы
В исследование включены 77 пациентов с немышечноинвазивным раком мочевого пузыря, подвергнутых ТУР и внутрипузырной химиотерапии с 2003 по 2008 г. Всем больным выполняли ТУР опухолей мочевого пузыря по стандартной методике до глубокого мышечного слоя с непосредственным внутрипузырным введением после нее химиопрепарата. В 74% случаев использовали цисплатин в дозе 50 мг с экспозицией 60 минут, в 15,6% – митомицин в дозе 40 мг, в 10,4% – доксорубицин 50 мг с аналогичной экспозицией. Степень дифференцировки оценивали по классификации ВОЗ 1973 г. Патологическую стадию устанавливали в соответствии с системой TNM. Наличие рака in situ (Tis) определяли как наличие Tis в сочетании с другими патологическими категориями либо в моноформе.
Наблюдение больных после ТУР с внутрипузырной химиотерапией проводили в соответствии с существующими протоколами послеоперационного наблюдения: РеТУР производили в сроки 4-6 недель после первичного лечения, контрольные цистоскопии для исключения или подтверждения рецидива опухоли и/или ее прогрессии выполняли 3-4 раза в течение первого года, раз в полгода в течение второго года, а затем ежегодно. Статистический анализ осуществлен при помощи программы istica 6.0. Различия в распределениях по нескольким градациям признаков оценивали по критериям Фишера и хиквадрат, используя абсолютные значения частот, в модуле непараметрической статистики. Кроме того, сравнение альтернативных показателей, представленных в виде процентов, проводили по t-критерию Стьюдента – с помощью дифференцировочного теста в модуле описательной статистики. Во всех случаях сравнения результаты различий считали статистически достоверными при вероятности ошибки менее 5% (р
Результаты
Средний возраст больных составил 58 лет (18-78 лет), 88,7% из них были мужчины. Медиана наблюдения за пациентами составила 29,2 месяца (6-72 месяца). Преобладающей была стадия рТ1 – 71 больной (92,2%). Tis в моноформе встретился в единичном случае (1,3%) (рис. 1). Высокодифференцированные (G1) опухоли доминировали в структуре всех опухолей и обнаруживались у 48 больных (62,3%), тогда как умеренно-дифференцированные (G2) и низкодифференцированные (G3) встречены в 25 (32,5%) и 4 (5,2%) случаях соответственно (рис. 2). Размеры опухолей и количество опухолей в мочевом пузыре показаны на рисунках 3, 4. Размеры опухолей составили от 1 до 6 см, при этом опухоли размерами 1-3 см преобладали у 37 (48,1%) больных, тогда как опухоли > 3 см определены у 40 (51,9%) больных, опухоли > 5 см удалены у 11 (14,3%) пациентов.
Клинически значимых осложнений после интравезикальной химиотерапии у больных выявлено не было, за исключением поллакиурии, отмеченной в 1 случае. Рецидив опухоли определен при использовании всех 3 химиопрепаратов у 8 больных (10,4%). Причем развитие рецидива выявлено достоверно чаще при внутрипузырной инстилляции доксорубицина – 4 случая (50% от случаев с доксорубицином), тогда как при использовании митомицина и цисплатина рецидив отмечен в 2 (16,6% и 3,5%) случаях соответственно (р
Более быстрое возникновение рецидива опухоли имело место в группе больных с интравезикальными инстилляциями доксорубицина, и более поздний рецидив рака мочевого пузыря – в группе с интравезикальным введением цисплатина. Группа больных с введением митомицина занимает промежуточное положение по возникновению рецидивов опухоли. При этом необходимо отметить, что в 92% случаев рецидивы возникали при размерах опухолей более 3 см и наличии умеренной или низкой дифференцировки опухолей по данным гистологического исследования после ТУР. Кроме этого, в 5 случаях (6,5%) отмечена прогрессия опухоли, потребовавшая выполнения радикальной цистэктомии, в 3 случаях из которых определялся Tis как наряду с папиллярной опухолью мочевого пузыря, так и в моноформе, что указывает на необходимость учитывать данный фактор как фактор риска прогрессии опу оли мочевого пузыря.
Обсуждение
Стандартом лечения немышечноинвазивного рака мочевого пузыря остается выполнение ТУР опухоли мочевого пузыря с адъювантной внутрипузырной химиотерапией [8]. Однако, по последним данным, только 4% урологов США используют непосредственное введение химиопрепарата после ТУР опухоли, что свидетельствует о снижении результативности данной терапии [9, 10]. По данным недавних исследований, риск развития рецидива рака мочевого пузыря при монотерапии путем ТУР составляет до 75%, а прогрессия опухоли отмечается в 11-63% случаев [3, 5-7].
В нашем исследовании был отмечен значительно меньший процент развития рецидивирования рака мочевого пузыря после ТУР с непосредственной внутрипузырной химиотерапией – 10,4% при медиане наблюдения 29 месяцев. При этом рецидив развивается достоверно реже при внутрипузырной химиотерапии цисплатином в дозе 50 мг с экспозицией в мочевом пузыре 60 минут. Время до возникновения рецидива опухоли увеличивается при применении митомицина и цисплатина в сравнении с докмногочисленным исследованиям по оценке эффективности митомицина и доксорубицина для внутрипузырной химиотерапии [10-12]. Прогрессия опухоли в когорте наших больных отмечена только в 6,5% случаев, тогда как некоторые зарубежные исследования указывают на отсутствие влияния внутрипузырной химиотерапии на снижение прогрессии немышечно-инвазивного рака мочевого пузыря [11, 13].
Рецидив и прогрессия опухоли зависят от патогистологических характеристик: так, количество рецидивов опухоли возрастает при опухолях больших размеров, умеренно- и низкодифференцированных, а также при наличии Tis. Указанные факторы являются определяющими, по данным некоторых исследований, для развития рецидива и прогрессии немышечно-инвазивного рака мочевого пузыря [5, 12, 14]. Таким образом, применение внутрипузырной химиотерапии ведет к улучшению результатов лечения немышечно-инвазивного рака мочевого пузыря, однако требуется продолжение изучения специализированных молекулярных и генетических маркеров, опреде яющих эффективность ответа проводимой терапии.
Выводы
Применение немедленной (в течение 6 часов) внутрипузырной химиотерапии после ТУР немышечно-инвазивного рака мочевого пузыря ведет к значительному снижению количества рецидивов и риска прогрессии опухоли мочевого пузыря. Использование для внутрипузырной химиотерапии цисплатина наряду с митомицином обеспечивает лучшие результаты в сравнении с доксорубицином. Для полноты оценки эффективности внутрипузырной химиотерапии и оценки прогноза рецидива и прогрессии рака мочевого пузыря необходимы дальнейшие ретро- и проспективные исследования в многочисленных специализированных центрах.
Источник
