Полиоксидоний в лечении цистита
В статье приведены результаты собственного исследования, целью которого было изучение влияния препарата Полиоксидоний на эффективность комплексной терапии хронических инфекционно-воспалительных заболеваний нижних отделов мочевых путей у женщин. Препарат оказывает иммуномодулирующее, дезинтоксикационное, антиоксидантное, мембранопротекторное действия.
Применение Полиоксидония способствовало оптимизации традиционной этиотропной противовоспалительной терапии у пациенток и более раннему заживлению послеоперационных ран после хирургических вмешательств на нижних мочевых путях. Ни в одном случае не было отмечено ни местных, ни общих побочных реакций.
Таблица 1. Возбудители, выявленные у больных с хроническим рецидивирующим циститом (n = 88)
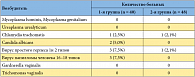
Таблица 2. Возбудители, выявленные у больных с хроническим рецидивирующим циститом (n = 88) после хирургической коррекции и медикаментозной терапии
Осложненная и неосложненная инфекция нижних мочевых путей (ИНМП) у женщин лидирует среди поводов обращения к урологу. Изнурительные дизурические симптомы острой и хронической инфекции нижних отделов мочевых путей значительно снижают качество жизни этих пациенток и весьма часто становятся причиной диспареунии и неврозоподобных состояний. Они нередко лишают женщин полноценного ночного сна, нормальной работоспособности днем и привычного образа жизни в целом. У некоторых больных хроническая ИНМП в процессе длительного течения осложняется симптомами инконтиненции, а также возникает восходящий пиелонефрит и другие осложнения, приводящие к инвалидизации. Около 40% женщин на территории Северо-Кавказского федерального округа отмечают в анамнезе хотя бы один эпизод острой ИНМП – цистита. В России, по статистике, ежегодно регистрируется до 35 млн случаев острой ИНМП. Чаще всего они возникают у женщин в возрастных группах 18-38 лет и от 65 лет и старше. Это объясняется интенсивностью половой жизни и реализацией репродуктивной функции пациенток первой группы и снижением уровня эстрогенов и, соответственно, общего и местного иммунитета пациенток второй группы.
По данным отечественных и зарубежных авторов, возбудителями неосложненной ИНМП являются E. coli, Enterococcus faecalis, Staphylococcus saprophyticus, Klebsiella pneumoniae, Proteus mirabilis. Установленным этиологическим фактором также является урогенитальная флора, передаваемая половым путем: Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum, Mycoplasma hominis, грибы рода Candida, Gardnerella vaginalis, вирус простого герпеса 1 и 2 типов и вирус папилломы человека 16-18 типов. Это доказывает необходимость тщательного комплексного лабораторного и клинико-инструментального обследования всех категорий больных ИНМП, а также оптимизации комплексной терапии, воздействующей не только на сам инфекционный агент, но и на все звенья иммунитета пациенток. Целью нашего исследования явилось изучение влияния препарата Полиоксидоний на эффективность комплексной терапии хронических инфекционно-воспалительных заболеваний нижних мочевых путей у женщин для улучшения результатов их лечения. Нами наблюдались 88 пациенток с различными формами хронической ИНМП и ее осложнениями в возрасте от 15 до 74 лет: 80 больных c хроническим рецидивирующим циститом (22 случая – в результате гипермобильности наружного отверстия уретры, 38 – в результате женской гипоспадии и 20 – вследствие лейкоплакии мочевого пузыря) и 8 больных с хроническим циститом и уретритом с формированием парауретральной кисты с нагноением. Длительность заболевания составила от 6 месяцев до 28 лет.
План обследования включал анализ жалоб пациенток, данных анамнеза заболевания с уточнением дебюта цистита и его связи с началом половой жизни, гигиеническими привычками, наличием острого или хронического процесса органов репродуктивной системы, выявление связи обострений хронического цистита с интенсивностью половой жизни, а также спектр обнаруженных урогенитальных инфекций, гормональный статус пациентки (особенно у женщин старше 65 лет), анализы крови и мочи, в том числе ПЦР мочи на инфекции, передаваемые половым путем (ИППП). Всем больным также выполнялось инструментальное исследование для выявления органической и обструктивной урологической патологии.
Лейкоцитурия отмечалась у всех обследуемых женщин. У женщин фертильного возраста, активно живущих половой жизнью и страдающих острым или хроническим воспалением гениталий, при молекулярно-биологическом исследовании (ПЦР) мочи было выявлено наличие влагалищной условно-патогенной микрофлоры и инфекционных агентов в клинически значимых титрах: Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum, Mycoplasma hominis в сочетании с кишечной палочкой и другими грамотрицательными бактериями, а также Trichomonas vaginalis, Gardnerella vaginalis, грибы рода Candida, вирус простого герпеса 1 и 2 типов и вирус папилломы человека 16-18 типов. Все эти возбудители выявлялись в различных комбинациях – микст-инфекциях. У пациенток пожилого возраста преобладала условно-патогенная, в основном грибковая, флора. Следует отметить, что тяжесть инфекционного процесса и его осложнений усиливалась у пациенток старшего возраста, пребывавших в менопаузе, что обусловливалось снижением уровня эстрогенов и развитием урогенитальной атрофии. Эпителий во влагалище и уретре в период менопаузы истончается, возникает дефицит гликогена, снижается продукция молочной кислоты и повышаются значения влагалищного pH. Эти изменения способствуют чрезмерному росту некисломолочных полиморфных видов бактерий и исчезновению лактобактерий, создаются благоприятные условия для колонизации влагалища условно-патогенной и патогенной микрофлорой. Частота восходящей ИНМП, включая поражения уретры, в период менопаузы возрастает.
Патогенная микрофлора мочи, уретры и соскоба из влагалища, как правило, была идентичной и являлась непосредственной причиной хронического рецидивирующего цистита (табл. 1). Все больные ранее неоднократно получали консервативное лечение длительными курсами, которое вызывало нестойкий клинический эффект и оценивалось ими как неудовлетворительное. Все женщины отмечали обострения хронической ИНМП 2-3 раза в год. Всем пациенткам было проведено хирургическое лечение по поводу выявленной органической патологии (гипермобильности наружного отверстия уретры, женской гипоспадии, лейкоплакии мочевого пузыря), а также иссечение парауретральных кист, так как это являлось пусковым и поддерживающим объективным механизмом хронизации инфекционного процесса в мочевых путях. Больным также проводилась медикаментозная периоперационная этиотропная антибиотикотерапия согласно спектру выявленных возбудителей (методом ПЦР-анализа мочи и исследования соскоба из влагалища). Предыдущие неоднократные курсы антибиотикотерапии вызывали значительное снижение общего и местного иммунитета у женщин. Результатом длительного течения хронической ИНМП явились нарушения со стороны гуморального иммунитета, которые проявились в снижении уровня IgG в 2 раза, снижении уровней IgA в 5 раз и секреторного IgA в 2 раза при неизмененном уровне IgM, что указывало на хронизацию процесса. Выявленный дисбаланс иммуноглобулинов указывал на иммунодефицитное состояние, а исход воспалительного процесса напрямую зависел от полноценности иммунного ответа.
Выявленные нарушения в иммунном статусе пациенток с хроническими ИНМП определили показания для проведения комплексной терапии с использованием иммуномодулятора. Учитывая длительность воспалительного процесса, с целью оптимизации терапии ИНМП и улучшения результатов лечения применялся высокомолекулярный химически чистый препарат Полиоксидоний, оказывающий иммуномодулирующее, дезинтоксикационное, антиоксидантное, мембранопротекторное действие. В основе механизма иммуномодулирующего действия Полиоксидония лежит прямая активация фагоцитирующих клеток и естественных киллеров, а также стимуляция антителообразования. Он оказывает корригирующее действие только на исходно измененные параметры иммунитета и не влияет на показатели, находящиеся в пределах нормальных значений. Препарат не нарушает естественных механизмов торможения иммунных реакций, не истощает резервных возможностей кроветворной системы, может назначаться без предварительного иммунологического обследования. Наряду с иммуномодулирущим действием Полиоксидоний обладает выраженной дезинтоксикационной активностью, которая определяется его высокомолекулярной природой. В ходе исследования все больные были разделены на 2 группы:
- 1-я группа (40 человек, контрольная) – пациентки, получавшие только противовоспалительную и антибактериальную терапию согласно спектру выявленного возбудителя ИНМП в сочетании с хирургическим лечением;
- 2-я группа – 48 пациенток, получавших противовоспалительную и антибактериальную терапию и хирургическое лечение в сочетании с Полиоксидонием 12 мг (суппозитории) по следующей схеме: 1 суппозиторий интравагинально 1 раз в сутки ежедневно в течение 3 дней; далее – 1 суппозиторий через день в течение недели; на курс лечения – 10 суппозиториев.
Эффективность препарата Полиоксидоний оценивалась на основании клинических и микробиологических параметров, а также данных субъективного состояния и клинических симптомов ИНМП. Положительная динамика в клиническом анализе крови отмечалась у 48 (100%) больных второй группы уже на 5-7-й день комплексной терапии и проявлялась в исчезновении лейкоцитоза и палочкоядерного сдвига лейкоцитарной формулы, снижении СОЭ. Влияние Полиоксидония на показатели иммунного статуса проявлялось в увеличении содержания CD3+-, CD4+-лимфоцитов. Отмечалась нормализация функциональной активности нейтрофилов, тенденция к увеличению содержания моноцитов в периферической крови. В контрольной группе положительная динамика со стороны вышеперечисленных показателей отмечалась только у 28 (70%) больных. Субъективное улучшение отметили 46 (95,8%) пациенток из второй группы.
Дизурия на фоне приема Полиоксидония купировалась на 3-и сутки, лейкоцитурия – на 7-8-е сутки. В контрольной группе женщины, получавшие только традиционную антибактериальную терапию, отметили исчезновение дизурии на 5-6-е сутки, лейкоцитурия сохранялась до 12-14-х суток. Результаты хирургического лечения во второй группе проявлялись следующим образом: на фоне применения Полиоксидония уменьшились сроки полного заживления послеоперационных ран с 10-11 до 6-7 дней. В первой группе послеоперационные раны заживали в стандартные сроки – в течение 10-11 дней. В результате полное клиническое выздоровление и элиминация возбудителей в результате включения Полиоксидония в комплексную терапию ИНМП наступили у 46 (95,8%) пациенток. В контрольной группе элиминация патогенов и клиническое выздоровление отмечены у 31 (77,5%) пациентки (табл. 2). Ни в одном случае применения Полиоксидония не было отмечено ни местных, ни общих побочных реакций.
Все пациентки второй группы, получавшие комплексную терапию с применением Полиоксидония, после выписки из стационара находились под наблюдением в течение 6 месяцев. Ни в одном случае не было отмечено рецидивов обострения хронической ИНМП. У 8 (20%) пациенток 1-й группы в течение 6 месяцев после лечения отмечался 1 рецидив ИНМП. Мы считаем, что хороший клинический эффект проводимой терапии обусловлен иммуномодулирующим действием Полиоксидония, его способностью к увеличению резистентности организма к инфекциям, а также к активизации клеточного звена иммунитета и стимуляции антителообразования. Таким образом, препарат Полиоксидоний способствует оптимизации традиционной этиотропной противовоспалительной терапии у пациенток с хроническими инфекционно-воспалительными заболеваниями нижних отделов мочевых путей и более раннему заживлению послеоперационных ран после хирургических вмешательств на нижних мочевых путях.
Источник
Какие свойства полиоксидония легли в основу его применения у больных с инфекцией урогенитального тракта?
В чем преимущества введения в терапевтическую схему иммуномодуляторов?
В настоящее время одной из центральных проблем инфекционной патологии является проблема урогенитальных инфекций, среди возбудителей которых выделяется внутриклеточный микроб Chlamydia trachomatis. В данной статье представлены данные о клинической и иммунологической эффективности иммуномодулятора полиоксидония в лечении урогенитальных инфекций.
Механизм действия полиоксидония. Полиоксидоний (ПО) представляет собой уникальную полимерную молекулу, обладающую многогранным положительным воздействием на организм человека. Это воздействие заключается в иммуномодулирующем, детоксицирующем, антиоксидантном, мембраностабилизирующем эффектах.
Иммуномодулирующий эффект связан со способностью полиоксидония нормализовать функциональную активность клеток моноцитарно-макрофагальной системы, активация клеток которой ведет к повышению функциональной активности практически всех звеньев защиты организма от инфекции:
- факторы естественной резистентности: нейтрофилов, моноцитов, макрофагов, NK-клеток;
- факторы приобретенного иммунитета: гуморального и клеточного.
Детоксицирующее действие связано с особенностями химической структуры полиоксидония, который, являясь высокомолекулярным веществом, содержит на своей поверхности большое количество активных группировок. В силу этого полиоксидоний обладает способностью сорбировать различные токсические вещества, в том числе микробной природы.
Антиоксидантное и мембраностабилизирующее свойства полиоксидония также тесно связаны с особенностями его химической структуры.
Полиоксидоний выпускается в виде лиофилизированного порошка для инъекций и суппозиториев.
Клиническая эффективность суппозиториев при лечении урогенитальных инфекций. Разработка неинвазивных методов лечения заболеваний является актуальной задачей медицины. Создание и внедрение в медицинскую практику лекарственной формы полиоксидония в виде суппозиториев может рассматриваться как большое научное достижение. Эта форма препарата использовалась в некоторых лечебно-профилактических учреждениях России для лечения урогенитальных инфекций. Применяли дозы препарата 3, 6 и 12 мг. Дозы 6 и 12 мг имели примерно одинаковую эффективность в плане элиминации возбудителя, тогда как в дозе 3 мг препарат хотя и обладал положительным воздействием, но менее выраженным, чем в предыдущих случаях. Эти данные явились основанием для использования в дальнейшем суппозиториев в дозе 6 мг.
Хламидиоз. Применение суппозиториев в дозе 6 мг выявило высокую клиническую эффективность препарата у женщин с хламидиозом в сочетании с хроническим сальпингоофоритом и односторонним гидросальпинксом; у больных с эндоцервицитом на фоне трихомониаза, с уреаплазмозом, гарднереллезом, микоплазмозом в сочетании с уреаплазмозом. Идентификация возбудителя осуществлялась с помощью прямой иммунофлуоресценции. Суппозитории (№ 10) больные получали первые три дня ежедневно и затем с интервалом в 48 часов. Лечение проводилось на фоне антибактериальной терапии.
В результате после включения ПО в комплексную терапию клиническое выздоровление и полная элиминация патогенов наступили у 96% больных. Не было отмечено ни одного случая токсических и побочных эффектов от действия суппозиториев. Их применение позволило сократить сроки лечения в 1,5 раза.
Неспецифический кольпит и цервицит. В данном исследовании больные получали свечи каждый день в течение 10 дней в дозе 6 мг. Уже после приема первых двух свечей все больные отмечали исчезновение зуда и жжения, прекращение выделений, явлений дискомфорта. К концу приема препарата эти симптомы исчезали полностью. При кольпоскопии отмечено исчезновение отечности и гиперемии, слизистая влагалища и влагалищной части шейки матки приобрела обычную бледно-розовую окраску. При бактериологическом исследовании перед началом лечения степень обсемененности влагалища достигала 107-109 КОЕ/мл. Среди микробов преобладали золотистый и эпидермальный стафилококк, кишечная палочка, протей, анаэробы. После проведенного лечения суппозиториями микрофлора влагалища была нормализована: количество бактерий составило 103-104/мл. Положительная клиническая динамика совпадала и улучшением показателей как местного, так и системного иммунитета. В первом случае происходило повышение функциональной активности макрофагов влагалища, во втором случае наблюдалось увеличение в крови CD4+Т-хелперов.
Результаты интравагинального применения суппозиториев у ВИЧ-инфицированных женщин с явлениями неспецифических кольпитов и цервицитов оказались весьма убедительными. Эти больные получали по указанной выше схеме свечи с полиоксидонием в сочетании с базисной терапией.
Было установлено, что интравагинальное применение полиоксидония в комплексном лечении ВИЧ-инфицированных больных приводило к существенному снижению вирусной нагрузки крови. На 107 клеток крови количество вируса уменьшалось с 985 геномов до 151. Аналогично уменьшалась и вирусная нагрузка макрофагов слизистой оболочки влагалища: с 344 геномов до 38 геномов на 107 клеток. В контрольной группе женщин, получавших только базисную терапию, снижение вирусной нагрузки на клетки крови было значительно менее выражено, у резидентных макрофагов влагалища практически отсутствовало.
Простатит. В ходе исследования суппозитории применяли в дозе 6 мг ежедневно в течение 10 дней у 15 больных с хроническим хламидийным простатитом. У всех больных после курса лечения полностью исчезали клинические жалобы: прекратились боли и рези в уретре, исчезли боли и дискомфорт в промежности, уретральные выделения, восстановилась эрекция. При контрольном исследовании, проведенном через месяц методом полимеразной цепной реакции, хламидии были выявлены только у одного из 15 больных.
При изучении эффективности лечения простатитов с помощью прямой иммунофлуоресценции через 2 месяца после завершения курса интраректального применения полиоксидония по аналогичной схеме у 30 больных (96 % случаев) была установлена полная элиминация возбудителя из патологического материала. При эхографии простаты отмечалось улучшение ее структуры, происходила нормализация микроскопической картины простаты и улучшение показателей эякулята. При иммунологическом исследовании выявлялось увеличение в периферической крови количества Т-хелперов и IgA.
Таким образом, можно утверждать, что суппозитории с полиоксидонием обладают высокой эффективностью при комплексном лечении урогенитальных инфекций. Учитывая это обстоятельство, а также полное отсутствие побочных эффектов у этой формы препарата, в настоящее время Фармакологический комитет разрешил безрецептурный отпуск полиоксидония в виде ректальных суппозиториев.
Клиническая эффективность инъекционной формы полиоксидония в лечении урогенитальных инфекций. При урогенитальных инфекциях инъекционная форма полиоксидония, так же как и суппозитории, использовалась в трех дозах: 3, 6 и 12 мг. Доза в 3 мг оказалась недостаточно эффективной. Дозы в 12 и 6 мг показали примерно одинаковую эффективность. Поэтому доза в 6 мг может быть признана основной для лечения урогенитальных инфекций с помощью инъекций. Применение полиоксидония в указанной форме хорошо зарекомендовала себя в комплексном лечении хламидийных уретритов, простатитов, цервицитов, сальпингоофоритов, трихоманадного уретрита, генитального герпеса. Эффективность применения полиоксидония может быть подтверждена полным клиническим выздоровлением и исчезновением возбудителей из патологического материала у 95% больных основной группы; в контрольной группе эта доля составила 70-75%. Кроме того, применение полиоксидония в комплексе с другими терапевтическими мероприятиями позволило в два раза сократить сроки лечения, значительно снизить дозу потребляемых антибиотиков, уменьшить частоту отдаленных рецидивов заболевания.
Хламидийные уретрит и простатит. Группа из 17 больных получала препарат в дозе 6 мг внутримышечно: первые 2 инъекции ежедневно, затем 2 раза в неделю; всего курс состоял из 7 инъекций. При культуральном исследовании больных через месяц после окончания лечения у 15 человек хламидии не выявлялись. У 2 больных были обнаружены обычные формы Ch.trachomatis. Как известно, эти формы являются чувствительными к антибиотикам, в связи с чем этот показатель может расцениваться как положительный. При иммунологическом исследовании было обнаружено повышение уровня естественных киллеров (CD16/56+), играющих, как известно, ведущую роль в защите организма от внутриклеточных возбудителей. Наблюдалось также повышение уровня иммуноглобулинов IgA и IgM. Напомним, что IgA играет важную роль в защите слизистых оболочек от инфекционных агентов.
Трихомонадный уретрит. Под наблюдением находилось 45 пациентов, диагноз трихомонадного уретрита у которых был поставлен на основании морфологического исследования соскоба из уретры микроскопическим методом и с помощью ПЦР. 23 человека получали этиотропные химиопрепараты (метронидазол, орнидазол или ниморазол) в комплексе с полиоксидонием (3 раза в неделю внутримышечно по 6 мг), 22 пациента получали только химиопрепараты без полиоксидония. После окончания курса лечения у всех больных первой группы трихомонады в соскобах из уретры не определялись. Клиническое выздоровление отмечалось у 19 человек. После повторного курса лечения выздоровление наступило у 3 человек. Во второй группе после проведенного курса лечения клинический эффект был отмечен только у 13 человек. Повторный курс прошли 9 пациентов, после которого в 5 случаях было достигнуто выздоровление. Таким образом, проведенные клинические наблюдения свидетельствуют об эффективности полиоксидония в комплексном лечении трихомонадных уретритов.
Эндолимфатическое применение полиоксидония при хламидийном простатите. Прямое эндолимфатическое введение ПО осуществляли 12 больным через микрокатетер, установленный в периферический лимфатический сосуд нижней конечности. Препарат вводили через день в дозе 6 мг, курс составлял 5-6 инъекций. В этом случае после окончания курса лечения отмечали значительное улучшение. Элиминация хламидий из простаты происходила в 96% случаев. Существенно улучшалась картина ее секрета. В крови происходило увеличение Т-хелперов (CD4+) и IgA. Вероятно, этот способ введения ПО следует иметь в виду, когда речь идет о запущенных случаях хронического простатита, трудно поддающихся лечению обычными методами.
Отдельные наблюдения практикующих врачей свидетельствуют о возможности применения инъекционной формы полиоксидония и в виде монотерапии. Однако в настоящее время говорить о применении полиоксидония при урогенитальных инфекциях в виде монотерапии преждевременно, для этого требуется дальнейшее накопление фактического материала.
Основная тактика применения полиоксидония. При различных заболеваниях приняты разные дозировки и схемы применения полиоксидония, однако примерную дозировку для взрослых можно сформулировать следующим образом: по 6 мг через 1-2 дня № 7-10. Такая схема рекомендуется для лечения хронических инфекционно-воспалительных процессов различных локализаций, в том числе и урогенитальных инфекций. В зависимости от тяжести патологического процесса число инъекций можно увеличивать до 15. С целью быстрого купирования патологии при острых процессах и септических состояниях первая доза полиоксидония может быть увеличена до 12 мг. В этих случаях возможно также ежедневное введение первых двух доз полиоксидония.
Полиоксидоний хорошо взаимодействует со всеми антимикробными препаратами, интерферонами и их индукторами. Он обладает способностью оказывать усиливающий эффект на действие основных этиотропных средств базисной терапии. Одновременное применение полиоксидония и антимикробного препарата наносит по возбудителю двойной удар, в результате чего и достигается хороший клинический эффект.
Источник
