Пмр на узи мочевого пузыря

Пузырно-мочеточниковый рефлюкс (ПМР) – процесс патологического заброса мочи из мочевого пузыря обратно по мочеточникам в лоханки и чашечки почек. Вызван недостаточностью клапанного механизма мочевых путей. Приводит к учащению воспалительных процессов, повышению почечного давления, нарушению структуры почечной ткани, гибели нефронов с последующим нефросклерозом и высоким риском почечной недостаточности.
Общие сведения
ПМР можно встретить примерно у каждого сотого урологического пациента. Согласно статистике, заболевание чаще проявляется в детском возрасте:
- 60% – дети 0–12 месяцев;
- 25% – 1–3 лет;
- 10-15% – 4–12 лет.
Для более старшего возраста (в том числе для взрослых) показатель составляет не более 4-5 %. В 35-60% случаев ПМР является сопутствующим заболеванием при острых и хронических инфекциях мочевых путей.
Патогенез
В норме анатомия пузырно-мочеточникового соединения исключает возможность обратного тока мочи. Острый угол впадения мочеточников и наличие гладких циркуляторных мышц, выполняющих роль сфинктера, создают надежную антирефлюксную защиту. При нарушении структуры или снижении функциональности гладкомышечного аппарата защита падает, и внутрипузырное давление легко преодолевает барьер уретро-везикулярного соустья, выбрасывая мочу в верхние мочевые пути.
Причины
Основные причины аномальной уродинамики:
- генетические синдромы (Элерса-Данлоса, Гиршпрунга);
- врожденные аномалии структуры мочевыводящих органов – увеличение диаметра отверстий мочеточников, неправильное их положение, укорочение интрамурального отдела, нарушения работы клапанного механизма в верхней части уретры, а также в устьях мочеточников;
- затяжные воспалительные процессы в области треугольника Льето (хронический цистит);
- нейрогенная дисфункция мочевого пузыря – при аномалиях развития ЦНС (спина бифида, липомы спинного мозга и т.п.);
- нарушение режима опорожнения мочевого пузыря – привычка «терпеть до последнего» постепенно приводит к ослаблению гладкой мускулатуры, инфицированию тканей и различным связанным с этим патологиям (рефлюкс, недержание мочи, хронический цистит).
Справка! Формирование мышечной ткани мочевыводящих путей происходит в период с 15 по 20 неделю внутриутробного развития. Если в этот процесс вмешиваются неблагоприятные факторы в виде генетических программ, внешних или внутренних физико-химических факторов, уже на 21—24 неделе у плода могут проявиться различные аномалии. Все они выявляются в первые годы после рождения ребенка. У взрослых людей ПМР встречается крайне редко и является следствием травм, хронических воспалений и неблагоприятных условий жизни
Классификация
По механизму действия ПМР может быть:
- пассивным – заброс мочи происходит при наполнении мочевого пузыря;
- активным – наблюдается при мочеиспускании;
- смешанным, или пассивно-активным.
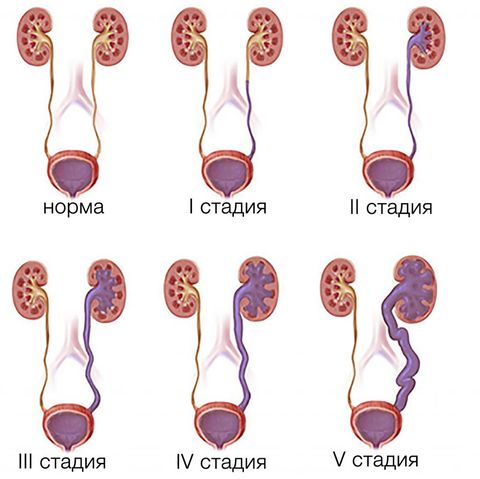
Вне зависимости от причины развития патологии, у ПМР выделяют 5 стадий заболевания:
- 1 стадия: рефлюкс мочи не далее мочеточников, деформация структур не наблюдается;
- 2 стадия: рефлюкс доходит до почек, деформация структур не наблюдается;
- 3 стадия: ПМР с признаками расширения лоханок и чашечек;
- 4 стадия: наличие умеренных признаков расширения в структуре мочеточников, лоханок и чашечек;
- 5 стадия: выраженное расширение всех структур с деформацией канала мочеточника и признаками дисфункции нефронов.
Симптомы ПМР
ПМР лишен характерной клинической картины. Особенно сложно диагностировать заболевание на ранних стадиях, когда симптомы полностью отсутствуют. Основные признаки формируются на 3-й стадии болезни и во многом схожи с симптомами воспалительных патологий. У маленьких детей проявляется по типу пиелонефрита. У детей старшего возраста и взрослых общий симптомокомплекс выглядит следующим образом:
- дискомфорт и боль в области почек при мочеиспускании;
- постоянное ощущение расширения в мочевом пузыре;
- проблемы с мочеиспусканием – частые позывы, прерывистая струя, застой мочи;
- отеки тканей;
- повышенное артериальное давление;
- головная боль, общее ухудшение самочувствия.
Методы диагностики
Основной метод диагностики ПМР – микционная цистография. Она подтверждает факт деформации коллекторной системы почек и мочеточников, определяет форму рефлюкса и степень развития патологии. Дополнительные методы:
- экскреторная урография – определяет тонус верхних мочевых путей;
- УЗИ – выявляет наличие склеротических изменений в тканях;
- цистоскопия – проводится при дифференциальной диагностике для исключения цистита;
- урофлоуметрия и цистометрия – необходима для исследования уродинамики в нижних мочевых путях;
- радиоизотопное обследование – для оценки функциональной активности почек.
Дополнительно врач назначает ряд лабораторных тестов для выявления причины заболевания: общий и биохимический анализ мочи, общий анализ крови, бакпосев, тест на ферменты, иммунограмму и др.
Как проходит лечение
В зависимости от причины и стадии заболевания, задействуют консервативные или хирургические методы. Безоперационное воздействие медикаментами и физиотерапией успешно восстанавливает уродинамику в 60—70% случаев ПМР на 1–3 стадии заболевания. К хирургии в обязательном порядке прибегают при лечении 4–5 стадии патологии, при врожденных аномалиях мочевыводящих путей, а также при отсутствии положительной динамики от консервативной терапии.
Консервативное лечение
Длительность медикаментозно-физиотерапевтического лечения составляет в среднем 6–12 месяцев. Для профилактики рецидивов назначаются курсы фитотерапии. Медикаментозная терапия:
- антибиотики (с учетом чувствительности возбудителя);
- уросептики (нитрофураны, хинолоны, сульфаниламиды), в том числе для внутрипузырных инсталляций;
- противовоспалительные средства, в том числе мембраностабилизирующие препараты;
- иммуностимуляторы;
- витамины и минеральные комплексы;
- средства для профилактики рубцевания почечной ткани.
Наибольшую сложность представляет лечение функциональных расстройств нейрогенной природы. В этом случае большое внимание уделяют методам физиотерапии. Среди них:
- электрофорез;
- ультразвуковое воздействие на область мочевого пузыря;
- электростимуляция;
- рефлексотерапия.
Хирургическое лечение
Главный смысл любых антирефлюксных операций заключается в удлинении внутрипузырного участка мочеточника путем создания искусственного подслизистого тоннеля или смещении положения их отверстий. Хирургическое устранение причин ПМР проводят двумя путями:
- Метод эндоскопии актуален на ранних стадиях ПМР (1–3) при условии сохранения тонуса и сократительной функции сфинктеров мочеточников. В таком случае подслизистую имплантацию гелями выполняют трансуретрально – с помощью цистоскопа. Операция неэффективна при патологическом положении устьев мочеточников за пределами треугольника Льето, при выраженном их расширении. При наличии острого воспалительного процесса операцию не проводят.
- Традиционная пересадка мочеточника методом открытой хирургии или лапароскопии актуальна при диагностировании 4–5 стадии заболевания, а также при рецидивах ПМР после проведения эндоскопии. Во время операции делают резекцию поврежденного отдела мочеточника с последующей имплантацией в новом месте и наращиванием антирефлюксной защиты.
Прогноз и профилактика
Прогноз на будущее зависит от стадии заболевания и степени повреждения почечной паренхимы. По данным статистики хирургическое лечение успешно устраняет ПМР в 85—98% случаев, после чего со временем восстанавливается работы почек (30% случаев) и отмечается общая стабилизация состояния (60% случаев). У маленьких детей эти показатели еще выше.
Во избежание рецидива, следует придерживаться правил профилактики, которые сводятся к своевременной диагностике и лечению инфекционных заболеваний, а также выполнению обязательно бытовых правил здоровья и гигиены:
- не ходить с переполненным мочевым пузырем – терпеть до последнего вредно для его гладкой мускулатуры;
- избегать переохлаждения тазовых органов;
- тщательно соблюдать правила интимной гигиены.
При положительном исходе лечения пациенту показана регулярная диспансеризация в течение 5 лет: первые 2 года – 2 раза в год, затем – 1 раз в год. Дополнительно пациент самостоятельно сдает анализ мочи на стерильность: первое время – ежемесячно, затем – каждые 3 месяца. По истечении срока, при отсутствии обострений пациента снимают с диспансерного учета.
Источник
 Пузырно-мочеточниковый рефлюкс у детей( ПМР )– это обратный ток мочи от мочевого пузыря к мочеточнику и почечной лоханке. Рефлюкс встречается у 1–2% детей, среди детей с пиелонефритом – у 25–40%, и выявляется в 70% случаев в возрасте до 1 года, в 25% случаев – в возрасте 1–3 лет, в 15% случаев – в возрасте 4–12 лет, в более старшем возрасте – в 5% случаев. В течение первого года жизни заболевание значительно чаще выявляется у мальчиков, чем у девочек, в более старшем возрасте отмечается обратное соотношение.
Пузырно-мочеточниковый рефлюкс у детей( ПМР )– это обратный ток мочи от мочевого пузыря к мочеточнику и почечной лоханке. Рефлюкс встречается у 1–2% детей, среди детей с пиелонефритом – у 25–40%, и выявляется в 70% случаев в возрасте до 1 года, в 25% случаев – в возрасте 1–3 лет, в 15% случаев – в возрасте 4–12 лет, в более старшем возрасте – в 5% случаев. В течение первого года жизни заболевание значительно чаще выявляется у мальчиков, чем у девочек, в более старшем возрасте отмечается обратное соотношение.
пузырно мочеточниковый рефлюкс ПМР (пузырно-мочеточниковый рефлюкс ) вызывает нарушение оттока из верхних мочевых путей, что нарушает пассаж мочи и создаёт благоприятные условия для развития воспалительного процесса (пиелонефрит ), рубцеванию почечной паренхимы с развитием рефлюкс-нефропатии, артериальной гипертензии и хронической почечной недостаточности.
Причины ПМР.
Обратный (ретроградный) ток мочи из мочевого пузыря в мочеточник является следствием несостоятельности клапанного механизма уретеро-везикального(пузырно-мочеточникового) сегмента(УВС).
Н.А.Лопаткин выделяет 3 группы теорий развития рефлюкса: первая заявляет главной причиной порок развития пузырно-мочеточникового сегмента, вторая говорит о формировании несостоятельности уретеро-везикального соустья как следствие воспалительного процесса с последующей фибропластической трансформацией, сторонники третьей теории считают главной причиной нарушение нервного аппарата мочеточника.
Выделяют первичный пмр, причиной которого является врожденная аномалия развития – укорочение внутрипузырного отдела мочеточника. Первичный рефлюкс может быть наследственно обусловленным. С ростом и развитием ребенка происходит «дозревание» структур, формирующих клапанный механизм, в связи с чем возможна спонтанная регрессия рефлюкса. Замечено, что чем выше степень рефлюкса – тем меньше вероятность его самостоятельного исчезновения. Несостоятельность клапанного механизма УВС отмечается аномалии расположения устья мочеточника – дистопии, эктопии.
Причины вторичного пмр – повышение внутрипузырного давления (клапан задней уретры, различные варианты дисфункции мочевого пузыря), хронический цистит. Хронический воспалительный процесс приводит к склеротическим изменениям в области уретеровезикального сегмента, укорочению интрамурального отдела мочеточника и зиянию устья. В свою очередь, хронический цистит нередко возникает и поддерживается инфравезикальной обструкцией.
Повреждение почечной паренхимы при ПМР происходит как вследствие повторения (рецидивирования) инфекционного процесса, так и вследствие «гидродинамического удара». Аномальная закладка мочеточника, приводящая к дистопии или эктопии устья, влечет за собой формирование диспластичной почки, что также отражается на ее функции.
Классификация ПМР.
Пузырно-мочеточниковый рефлюкс подразделяется на пассивный, возникающий в фазу наполнения, активный, возникающий в момент мочеиспускания и пассивно-активный или смешанный. Выделяют интермиттирующий пузырно-мочеточниковый рефлюкс, не доказанный рентгенологическими методами, но имеющий характерную клиническую картину – рецидивирующий пиелонефрит, периодическая лейкоцитурия, косвенные ультразвуковые и рентгенологические признаки пузырно-мочеточникового рефлюкса.
Наиболее распространенной является классификация, предложенная P.E.Heikkel и K.V.Parkkulainen в 1966 году, адаптированная в 1985 году International Reflux Study Group. В зависимости от уровня заброса контрастного вещества и степени расширения мочеточника и собирательной системы почки, выявленных при ретроградной цистоуретрографии, выделяют 5 степеней ПМР:
I степень – обратный заброс мочи из мочевого пузыря только в дистальный отдел мочеточника без его расширения;
II степень – заброс мочи в мочеточник, лоханку и чашечки, без дилатации и изменений со стороны форниксов;
III степень – обратный заброс мочи в мочеточник, лоханку и чашечки при незначительной или умеренной дилатации мочеточника и лоханки и склонности к образованию прямого угла форниксами;
IV степень – выраженная дилатация мочеточника, его извилистость, дилатация лоханки и чашечек, огрубленность острого угла форниксов при сохранении сосочковости у большинства чашечек;
V степень – выраженная огрубленность острого угла форниксов и сосочков, дилатация и извилистость мочеточника.
Ряд авторов использует понятие «мегауретер» при диаметре расширенного мочеточника более 7 мм, при наличии рефлюкса говорят о «рефлюксирующем мегауретере».
Клиническая картина. Жалобы, симптомы.
Пузырно-мочеточниковый рефлюкс у детей не имеет специфической клинической картины, течение заболевания у детей, особенно раннего возраста, как правило бессимптомно.
Жалобы обычно возникают при манифестации пиелонефрита. Отмечается повышение температуры до фебрильных цифр, диспептические явления, боли в животе, признаки интоксикации, помутнение мочи. Дети старшего возраста жалуются на боли в поясничной области после мочеиспускания. При бессимптомном течении наличие рефлюкса можно заподозрить при проведении скринингового ультразвукового исследования почек (пре- и постнатально). Показанием к проведению полного комплекса урологического обследования является расширение лоханки (поперечный размер – более 5 мм) и мочеточника, косвенным признаком рефлюкса при УЗИ считается нарастание расширения собирательной системы почки и мочеточника по мере наполнения мочевого пузыря.
Диагностика.
Основным методом диагностики пузырно-мочеточникового рефлюкса у детей является ретроградная цистоуретрография.
Исследование необходимо выполнять не ранее чем через неделю после купирования воспалительного процесса, т.к. воздействие токсинов на мочеточник может исказить истинную картину состояния мочеточников.
Для определения причины пмр, оценки функции почки и выявления склеротических изменений в почечной паренхиме обязательно проведение комплексного обследования, включающего: ультразвуковое исследование почек с допплерографической оценкой показателей внутрипочечного кровотока и мочеточниково-пузырных выбросов, исследование уродинамики нижних мочевых путей (ритм спонтанных мочеиспусканий, цистометрия или видеоцистометрия, урофлоуметрия), также применяются лучевые методы – внутривенная экскреторная урография, динамическая радиоизотопная ренография (технеций-99), статическая радиоизотопная ренография (DMSA).
Лечение.
Основной целью лечения рефлюкса детей является предотвращение развития рефлюкс-нефропатии, для чего необходимо исключить два основных повреждающих фактора – «гидродинамический удар» и рецидивирование инфекционного процесса. Лечение вторичного рефлюкса должно быть направлено на устранение вызвавших его причин.
При любой степени рефлюкса показано проведение консервативных мероприятий, включающих:
– Коррекцию метаболических нарушений в нервно-мышечных структурах мочеточника и мочевого пузыря (элькар, пикамилон, гипербарическая оксигенация, физиотерапевтические процедуры).
– Профилактику и лечение инфекции мочевых путей (уросептики, антибактериальная терапия, иммунокоррекция, фитотерапия).
– Устранение имеющихся нарушений уродинамики на уровне нижних мочевых путей.
Чем меньше частота рецидивов пиелонефрита, тем ниже риск развития рефлюкс-нефропатии, что оправдывает применение антимикробных препаратов у пациентов с ПМР.
После проведённого курса лечения через 6–12 мес. выполняют контрольную цистографию. Эффективность консервативного лечения при I–III степени пузырно-мочеточникового рефлюкса составляет 60–70%, у детей раннего возраста – до 100%.
Показания к оперативному лечению рефлюкса должны определяться с учетом возраста ребенка и причины рефлюкса.
Учитывая возможность спонтанной регрессии рефлюкса у детей первого года жизни необходимо придерживаться максимально консервативной тактики. При высоких степенях рефлюкса, а также неадаптированном мочевом пузыря предпочтительно выполнение эндоскопической коррекции рефлюкса. К оперативному лечению следует прибегать при только при выявлении аномалии положения устья мочеточника (дистопия, эктопия).
У детей старшего возраста возможность спонтанного исчезновения рефлюкса значительно ниже. При первичном рефлюксе предпочтительна эндоскопическая или оперативная коррекция.
Показаниями к оперативному лечению ПМР являются:
– Рецидивирование инфекции мочевых путей несмотря на антимикробную профилактику
– Сохранение рефлюкса после коррекции дисфункций мочевого пузыря
– Неэффективность консервативного лечения (отсутствие роста или прогрессирование сморщивания почки, снижение функции почки)
– Рефлюкс в сочетании с другими аномалиями развития (удвоение мочеточника, дивертикул мочевого пузыря и т.п.)
Проводится путем имплантации какого-либо вещества в подслизистом отделе устья мочеточника с целью усиления пассивного компонента клапанного механизма. Среди преимуществ метода – малая инвазивность и возможность повторных манипуляций в области УВС. Недостатками метода являются невозможность интраоперационной оценки эффективности созданного клапанного механизма, миграция или деградация введенного препарата с течением времени, что может привести к необходимости повторной манипуляции. В качестве имплантируемого вещества предложены различные материалы – ауто- и гетерологичные. Идеального вещества для подслизистой имплантации в нестоящее время не существует, наиболее широкое распространение получили коллаген, уродекс (urodex), вантрис (vantris), каждый из которых, в свою очередь, имеет свои особенности.
Оперативная коррекция рефлюкса. В зависимости от доступа выделяют внутрипузырные, внепузырные и комбинированные методики.
Общим принципом оперативной коррекции является создание клапанного механизма уретеро-везикального соустья за счет формирования подслизистого тоннеля достаточной длины, соотношение между диаметром мочеточника и длиной тоннеля должно быть не менее 1:5. Наиболее распространенными являются операции Политано-Леадбеттера, Коэна, Гленн-Андерсона, Жиль-Вернэ, Лих-Грегуара.
В послеоперационном периоде необходим контроль за размерами почки, собирательной системы и мочеточников, а также проведение антимикробной профилактики. Рентгеновское исследование для оценки эффективности операции проводится через 3–6 месяцев.
При вторичном рефлюксе лечение направлено на устранение факторов, провоцирующих его возникновение.
При наличии клапана задней уретры производится трансуретральная резекция створок клапана с последующим дренированием мочевого пузыря через уретральный катетер и/или цистостому. Решение вопроса о необходимости дальнейшего дренирования проводится после контрольной уретроскопии через 10 дней, при условии сокращения диаметра мочеточников и собирательной системы почек.
При наличии дисфункции нижних мочевых путей лечение осуществляется в зависимости от типа выявленных нарушений.
Прогноз. Исход.
При низких степенях рефлюкса (I–III), отсутствии выраженных изменений со стороны почечной паренхимы и рецидивов пиелонефрита возможно полное излечение без каких-либо последствий.
При образовании участков склероза в почечной паренхиме говорят о развитии рефлюкс-нефропатии.
Рефлюкс IV–V степени в 50–90% сопровождается врожденным повреждением паренхимы почки, связанным с ее дисплазией или вторичным сморщиванием.
По данным последних исследований стерильный рефлюкс не приводит к развитию рефлюкс-нефропатии. Наибольшее повреждение паренхимы почки происходит при первом эпизоде пиелонефрита. При рецидивировании инфекционного процесса вероятность развития сморщивания почки возрастает в геометрической прогрессии. У детей первого года жизни риск развития сморщивания почки значительно выше, чем у детей более старшего возраста.
Всем детям с пузырно-мочеточниковым рефлюксом необходимо динамическое наблюдение уролога и нефролога.
Необходим контроль общего анализа мочи 1 раз в 2-3 недели, общего анализа крови раз в 3 месяца, биохимического анализа крови и мочи (1 раз в 6 месяцев), ультразвуковое исследование почек 1 раз в 3-6 месяцев, радиоизотопное исследование почек 1 раз в год, цистография – после проведения курса терапевтического лечения, через 1 год с целю оценки регрессии рефлюкса. Необходимость антимикробной профилактики у детей с I–III степенью рефлюкса решается в зависимости от изменений в общем и микробиологическом анализе мочи. При IV–V степени антимикробная профилактика должна проводится непрерывно.
Источник
