Пластику мочевого пузыря местными тканями при экстрофии проводят в возрасте
Первичная пластика мочевого пузыря местными тканями при экстрофии у детей
Ю.Э. Рудин, Д.В. Марухненко, Ю.Э. Чекериди
ФГУ “НИИ Урологии Росмедтехнологий”, Детская больница Святого Владимира, Москва
Журнал “Экспериментальная и клиническая урология”, №1, 2010
Экстрофия мочевого пузыря (ЭМП) – одно из самых тяжелых заболеваний. ЭМП представляет собой сочетание ряда пороков, объединенных единой этиологией дефект мочевого пузыря, уретры, незаращение передней брюшной стенки и порочно сформированные наружные половые органы [1, 2, 3, 4]. ЭМП выявляется у одного на 40 000-50 000 новорожденных и приблизительно в 2-3 раза чаще встречается у мальчиков [5, 6]. Задняя стенка мочевого пузыря выпячивается наружу в виде вентральной грыжи, покрытой слизистой оболочкой [6]. В нижней части экстрофированной площадки находятся устья мочеточников, из которых по каплям выделяется моча. Диастаз лонных и седалищных костей обусловлен недоразвитием их медиальных концов [1, 6, 7]. Непосредственный и постоянный контакт верхних мочевых путей с внешней средой через устья мочеточников способствует развитию хронического пиелонефрита [3, 6, 8].
Диагноз ЭМП чаще всего устанавливают сразу после рождения ребенка [9], хотя заподозрить экстрофию мочевого пузыря можно и внутриутробно [1, 6]: при ультразвуковом обследовании плода на разных стадиях беременности врач должен (хотя бы однократно) увидеть наполненный мочевой пузырь. Отсутствие тени мочевого пузыря при серии обследований должно явиться основанием заподозрить диагноз ЭМП [1, 3, 10, 11]. К сожалению, в нашей стране у врачей женских консультаций отсутствует настороженность по выявлению этого тяжелого порока развития на ранних сроках беременности.
Исследованиями F.D. Stephens, J.M. Hutson (2005) установлено, что причиной возникновения ЭМП является давление хвоста эмбриона (tail) на область урогенитальной диафрагмы (место, где происходит соединение зачатков мочевого пузыря, уретры и полового члена) в период закладки органов на 3-4 неделе внутриутробного развития [1, 10].
Первые операции по коррекции экстрофии были выполнены в середине ХIX века. В 1942 году Янг сообщил об успешном закрытии мочевого пузыря у девочки. Шейка мочевого пузыря в последующие сроки была сформирована в трубку, в результате чего девочка оставалась сухой в течение 3-х часов [1]. Однако большинство хирургов, несмотря на успех этого вида вмешательства, в те годы отдавали предпочтение отведению мочи в кишечник [10, 12].
О необходимости выполнения двусторонней остеотомии подвздошных костей впервые сообщил Шульц в 1954 году, благодаря которой (через 2 недели) удавалось закрыть мочевой пузырь. При этом производилось сближение симфиза. Через неделю после удаления катетера из мочевого пузыря пациентка удерживала мочу [13]. Это наблюдение позволило предположить, что сближение лонных костей с двусторонней подвздошной остеотомией способствует наилучшей функции лонной “петли” и соответственно формирует механизм удержания мочи на уровне урогенитальной диафрагмы [5].
В последние годы первичная пластика мочевого пузыря стала распространенным вмешательством, тогда как отведение мочи в кишечник сопровождается высоким процентом послеоперационных осложнений [1, 3]. В то время у детей, которым выполнялась пластика мочевого пузыря местными тканями без сведения лонных костей, вмешательство часто заканчивалось рецидивом заболевания и отсутствием удержания мочи [11, 14, 15].
Экстрофия мочевого пузыря предполагает длительное этапное лечение. Достигнуть полного удержания мочи у большинства пациентов крайне сложно. Поэтому большое значение имеет успешно проведенный первый этап операции (первичная пластика мочевого пузыря местными тканями, а также соединение и удержание вместе лонных костей, формирование шейки мочевого пузыря и соединение порочных мышц уретрального сфинктера). К сожалению, по данным многих авторов [3-6], добиться полного удержания мочи после первого этапа операции не представляется возможным. И только последующие оперативные вмешательства могут способствовать удержанию мочи [1, 7].
МАТЕРИАЛЫ И МЕТОДЫ
За период с 1988 по 2009 гг. в урологическом отделении Детской больницы Святого Владимира были оперированы 93 ребенка с экстрофией мочевого пузыря в возрасте от 1 суток до 16 лет. Мальчиков (67) было в два с половиной раза больше, чем девочек (26). Большинство пациентов (62) поступали в стационар в первую неделю после рождения.
Всем больным с ЭМП проводились лабораторные анализы (общий анализ крови, с определением времени свертываемости и длительности кровотечения, биохимический анализ крови, группа крови и резус фактор, анализ кала, КЩС, общий анализ мочи).
При клиническом осмотре давалась оценка кожным покровам, определялся тургор мягких тканей, оценивались размеры и степень напряжения большого родничка, состояние пуповины. Измерялись размеры пузырной площадки (длина, ширина), определялось расстояние между устьями мочеточников и расстояние до семенного бугорка, оценивалась степень воспалительных изменений слизистой мочевого пузыря, наличие полипозных разрастаний, определялась способность тканей мочевого пузыря к растяжению и погружению в малый таз. Для уменьшения степени выраженности воспаления слизистой мочевого пузыря поверхность слизистой укрывалась тонкой перфорированной пленкой с антибактериальной мазью. Оценивали размеры полового члена у мальчиков измеряли длину и ширину кавернозных тел, наличие вентральной деформации, определяли положение и размер яичек (рисунок 1).
УЗИ органов мочевыделительной системы и брюшной полости проводилось для исключения сочетанных врожденных пороков развития и для измерения расстояния между лонными костями таза.
Рентгеновский снимок костей таза проводили для измерения исходного диастаза лонных костей и для исключения врожденных пороков крестцово-копчиковой области, подвывихов или вывихов головок бедренных костей.
По показаниям проводились дополнительные методы обследования. При выявлении сочетанных пороков развития экскреторная урография выполнялась 5 больным с признаками расширения ЧЛС и мочеточника. Радиоизотопное обследование назначалось для определения функции почек (23 пациентам). УЗ допплеровское исследование кровотока почки (цветовое картирование) проводили 48 детям для оценки почечного кровотока.
Ирригография, колоноскопия, ректороманоскопия выполнялись тем детям, которым предполагалась пересадка мочеточников в толстую кишку, для оценки длины сигмовидной кишки, состояния слизистой и выбора места имплантации мочеточников.
Фистулография выполнялась при наличии ректовагинальных свищей. При обследовании больных с экстрофией мочевого пузыря выявлены различные сочетанные заболевания (таблица 1).

https://bladderexstrophy.ru/pic01/20141126_pic004.jpg
Нами использовались два основных метода коррекции ЭМП: пересадка мочеточников в кишку и первичная пластика мочевого пузыря местными тканями. Для проведения объективной оценки результатов оперативного лечения экстрофии мочевого пузыря были выделены две группы.
В I группу пациентов вошли дети (12 чел.), которым выполняли иссечение площадки мочевого пузыря с пересадкой мочеточников в толстую кишку. Большинство детей этой группы (8 чел., 66%) оперированы по Гудвину (пересадка мочеточников в сигмовидную кишку с антирефлюксной защитой). Пересадка мочеточников в полуотключенный сегмент сигмовидной кишки выполнена 4 больным (34%). Эти оперативные вмешательства выполнялись в период с 1988 по 1998 гг. В последующие годы предпочтение отдавалось первичной пластике мочевого пузыря с остеотомией подвздошных костей.
Основную II группу составили пациенты (81), которым проведена первичная пластика мочевого пузыря местными тканями с пластикой шейки и со сведением костей лонного сочленения. Распределение больных с экстрофией мочевого пузыря в зависимости от возраста, пола и формы порока представлено в таблице 2.

https://bladderexstrophy.ru/pic01/20141126_pic005.jpg
С 1997 по 2009 годы мы стали использовать международный протокол ведения больных с экстрофией мочевого пузыря. Операция первичная пластика мочевого пузыря местными тканями предусматривала проведение следующих этапов:
выделение и мобилизация стенки мочевого пузыря;
формирование шейки пузыря;
дренирование почек уретеростомами;
выведение и фиксация мочеточниковых катетеров и эпицистостомы;
ушивание мочевого пузыря;
сведение и фиксация лонных костей в области лонного сочленения;
ушивание шейки мочевого пузыря;
ушивание дефекта передней брюшной стенки.
Оптимальным сроком для выполнения операции считается возраст 3-5 сутки после рождения ребенка. Чем старше был ребенок, тем сложнее удавалось сопоставить и фиксировать кости таза в области лонного сочленения. Детям старше 14 дней (17 человек, средний возраст 4 мес.) и новорожденным с большим расстоянием между лонными костями более 5 см (6 чел.) для надежного сопоставления лонных костей проводился один из вариантов подвздошной остеотомии. Всего выполнено 23 операции на костях таза.
Задняя вертикальная подвздошная остеотомия была выполнена 3 (13%) больным: подвздошные кости выделяли через задние вертикальные разрезы в проекции крестцово-подвздошного сочленения. Обе пластинки подвздошной кости пересекали долотом от S заднего подвздошного гребня к седалищной вырезке, на 5-7 мм латеральнее крестцово-подвздошного сочленения.
Операция Хиари выполнена 9(39%) детям, а надацетобулярная остеотомия (операция Вильсона) 11(48%) детям, среди них трем новорожденным с большим расстоянием между лонными костями и маленькой площадкой мочевого пузыря. Данные операции обладают рядом преимуществ и более удобны, поскольку и остеотомия, и пластика мочевого пузыря осуществляется в положении ребенка на спине, и его не нужно переворачивать во время выполнения оперативного вмешательства. Иммобилизацию у новорожденных детей осуществляли вытяжением по Блаунту в течение 3-х недель. Детям старше 2-х месяцев накладывали кокситно-гипсовую повязку на 1 мес. Детям старше 1 года фиксацию костей проводили с использованием стержневых аппаратов сроком до 1,5 мес. Ортопедический этап операции выполняли ортопеды-травматологи.
Типичная операция пластики мочевого пузыря местными тканями была выполнена 25 больным (26,8%). На основании накопленного опыта предложена модификация существующей методики: проводили глубокое выделение тканей в области шейки мочевого пузыря с отделением их от лонных костей и пересечением мышц урогенитальной диафрагмы; формировали шейку из ткани мочевого пузыря путем иссечения треугольных лоскутов слизистой оболочки и сшивания их в трубку по методу “двойного запахивания”. Нами предложен также оригинальный шов, соединяющий кости лонного сочленения: вместо внутрикостного шва применяли циркулярный шов вокруг верхней ветви лонной кости. Узел данного шва завязывали снаружи, что предупреждало в дальнейшем стенозирование шейки мочевого пузыря. Данная операция проведена у 56 больных.
Источник
Экстрофия мочевого пузыря это, пожалуй, наиболее тяжелый врожденный порок развития в урологии, при котором отсутствует передняя стенка мочевого пузыря и соответствующая ей передняя брюшная стенка (живота). Вся моча изливается наружу, половой член не имеет уретры, мочеиспускательный канал и головка члена расщеплены по дорсальной поверхности. Кавернозные тела укорочены за счет разошедшихся в стороны лонных костей. Слизистая мочевого пузыря под воздействием памперсов или пеленок подвергается эррозии и кровоточит, далее возникают полипы и признаки булезного воспаления. Некоторые из аномалий по внешнему своему виду вызывают просто шоковое состояние у людей, с ними сталкивающихся. Экстрофия мочевого пузыря встречается довольно редко. В среднем частота порока колеблется от 1 : 10000 до 1 : 50000 новорожденных.
Аномалии группы «экстрофия-эписпадия» представляют собой сочетание ряда пороков, объединенных единой этиологией и наличием по вентральной поверхности дефекта как минимум части мочевого пузыря и уретры. Проявления этой патологии варьируют от головчатой эписпадии до клоакальной экстрофии.
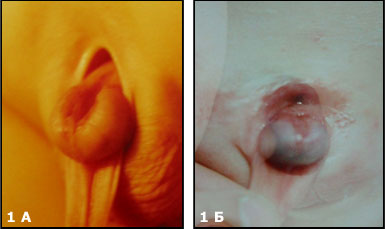
В случае эписпадии (Рис.1 А) наблюдают дефект уретры и в отдельных случаях сфинктера мочевого пузыря.

У больных с частичной экстрофией (Рис.1Б), отсутствует только небольшая часть передней стенки мочевого пузыря,
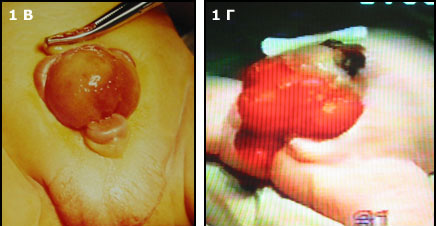
Классическая экстрофия (Рис.1В), когда весь мочевой пузырь расположен снаружи. И наиболее сложная форма экстрофии это клоакальная экстрофия (Рис.1 Г) когда мочевой пузырь представлен двумя округлыми порциями расположенными на расщепленной по передней поверхности толстой кишке, порок сопровождается огромным дефектом передней брюшной стенки и укороченным кишечником.
Открытые наружу мочевой пузырь и деформированные гениталии видны в первый же момент после рождения. И задача бригады, занимающейся лечением экстрофии, – решить, возможно ли обеспечить этому ребенку, здоровому во всех других отношениях, активную продуктивную жизнь, или он будет обречен на уединение, дискомфорт и безисходность.
Последние 3 десятилетия пластика мочевого пузыря стала довольно распространенным вмешательством, особенно в связи с тем, что все более часто появлялись сообщения об осложнениях операций отведения мочи в кишку. Однако, к сожалению, добиться удержания мочи у большинства пациентов с экстрофией мочевого пузыря, остается по-прежнему очень сложной проблемой, решить которую чрезвычайно трудно.
Первичная пластика (закрытие) мочевого пузыря Цели первичного закрытия мочевого пузыря следующие:
1. Ротация безымянных костей для вседения лонных костей и замыкания диафрагмы таза.
2. Закрытие пузыря и смещение его в заднее положение в полость малого таза.
3. Обеспечение свободного выделения мочи через уретру.
4. Мобилизация кавернозных тел от костей таза для первичного удлинения полового члена.
5. Закрытие дефекта передней брюшной стенки.
Мы располагаем опытом лечения новорожденных с экстрофией мочевого пузыря в Больнице Св.Владимира с 1996 г. Успешно оперировано более 130 новорожденных детей. ; Это самый большой опыт по числу наблюдений в России. Число осложнений составило не более 7%. Повторные операции были успешны. У многих детей после первой операции было достигнуто удержание мочи. У большинства удалось достигнуть мочеиспускания порциями и самое главное отмечен рост мочевого пузыря. т Первичное закрытие мочевого пузыря и сведение лонных костей без остеотомии у новорожденных детей с экстрофией мочевого пузыря. (Рис.2) и пластика шейки мочевого пузыря и уретры при тотальной эписпади
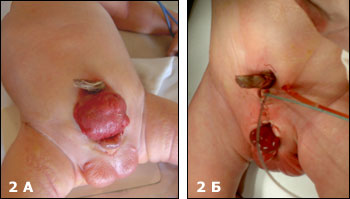 |
| Рис.2 А.Ребенок 4 дней с классической экстрофией мочевого пузыря. Б.Тот больной после операции. |
Первым этапом пластика полового члена, обычно не проводится. Формирование уретры (Рис.3) это следующий последовательный шаг по коррекции данного порока, данную операцию мы выполняем в возрасте 2-3 лет.
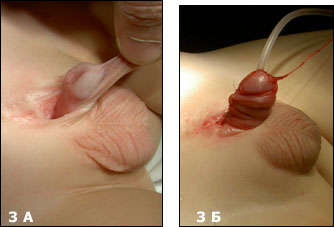 |
| Рис.3 А Ребенок 3 лет с экстрофией мочевого пузыря (после первичной пластики в возрасте 3 дня), Б- тот же ребенок после пластики уретры по Ренсли. |
Пластика шейки мочевого пузыря Этап лечения направленный на создание механизма по удержанию мочи. Важно понимать, что мочевой пузырь является резервуаром для накопления и эвакуации мочи. В случаях, когда исходный размер пузыря невелик, очень трудно сформировать качественный удерживающий мочу механизм, поскольку для этого требуется часть тканей самого мочевого пузыря.Именно поэтому дети с малыми размерами пузырной площадки и микроцистисом. Кроме того для хорошего заживления тканей в послеоперационном периоде после пластики шейки и адекватной работы дренажей необходим достаточный объем мочевого пузыря. По нашим данным необходимо иметь мочевой пузырь 120-150мл. Достигнуть роста мочевого пузыря у детей с микроцистисом и недержанием мочи для выполнения успешной пластики шейки считается одной из пока еще нерешенных проблем экстрофии. Больным с микроцистисом выполняют аугментирующие операции направленные на увеличение емкости мочевого пузыря. соединяя его с сегментом кишки (тонкой или толстой). Операция требует создания сухой стомы (аппендикостомы) – трубки из червеобразного отростка, с помощью которой осуществляют опорожнение мочевого пузыря катетером. В зависимости от емкости резервуара данную катетеризацию необходимо выполнять 4-7 раз в сутки. Кишечные резервуары требуют регулярного (каждый день) промывания, для отмывание слизи, которая может способствовать камнеобразованию и нарушению опорожнения резервуара.
Наиболее сложной задачей считается достижение естественного роста мочевого пузыря у детей с микроцистсисом для сохранения возможности естественного мочеиспускания и качественного удержания мочи. Для этого используется много методов, однако. эффективность их не столь велика. Медикаментозное лечение сопровождается слабым эффектом и нередко сочетается с непереносимостью препаратов. Механические способы растяжения мочевого пузыря в сочетании с отсутсвием удержания мочи – несовершенны и так же мало эффективны. Одним их способов решения данной проблемы стал метод обкалывания мочевого пузыря ботулотоксином. Расслабление стенки пузыря после данных инъекций в сочетании с медикаментозным и механическим растяжение пузыря позволяют достигнуть более значимого эффекта. .
Почему детей с экстрофией мочевого пузыря,оперируют новорожденными? В соответствии с международным протоколом (его придерживаются лидеры в лечении данной патологии Америка, Англия, большинство стран Европы) , коррекцию данного порока целесообразно выполнить в ранние сроки ( первые 2-5 суток после рождения). Столь ранние операции обусловлены возможностью сведения костей лона у больных с экстрофией мочевого пузыря без остеотомии (пересечения подвздошных костей) – пока кости остаются пластичными. Сведение лонных костей обеспечивает лучший эффект удержания мочи, что является наиболее сложной задачей подобных операций. Сведение лонных костей у мальчиков позволяет увеличить длину полового члена. (Рис.4)
Рис. 4 Мобилизация ножек кавернозных тел и сведение лонных костей , позволяют добиться увеличения длины полового члена.
Оперативные вмешательства в более поздние сроки, через 1 мес. и далее требуют проведения той же операции в сочетании с остеотомией по типу Хиари, что значительно травматичнее и сопровождается в несколько раз более сложным и продолжительным восстановительным периодом. Для чего необходима остеотомия? .Последние годы появились публикации о возможности откладывания этих операций на 6-8 мес. Или вообще выполнении первичного закрытия без сведения лонных костей или без остеотомии. Мы согласны, что при рождении ребенка ослабленного, с большим числом сочетанной патологии и очень маленьким размером мочевого пузыря – операцию можно отложить и до 1 года. Почему до 1 года. Необходимо выполнение остеотомии с фиксацией отломков спицами. У грудных детей спицы прорезываются и недостаточно стабильно удерживают отломки. Закрытие пузыря без остеотомии сопряжено с риском большого числа осложнений и самое главное низким косметическим и функциональным результатом. Так по нашим наблюдениям дети, которым сведение лонных костей или остеотомии не выполнями вовсе имеют диастаз лонных костей до 18см.( Рис.5.)
Рис.5. Косметические и функциональные результаты лечения экстрофии у больных без сведения лонных костей значительно хуже.
У мальчиков наблюдается укорочение полового члена, у девочек возможно выпадение матки и влагалища при беременности. Мнение, что сведение лонных костей не позволяет добиться желаемого результата, что лонные кости опять расходятся – неверно. Нужно понимать, что при экстрофии лонные кости недоразвиты и не растут в длину как у детей без данной патологии. У новорожденных детей оперированных в ранние сроки по стандартному протоколу, формируется фиброзный тяж между лонными костями и несмотря на отставание в росте лонных костей расхождение лонного сочленения значительно меньше, чем у детей которым сведение в новорожденном возрасте без остеотомии или в более старшем возрасте с остеотмией не делалось. Расхождение костей у большинства детей не более 3-4см. (Рис. 6)
Рис.6. Расхождение лонных костей после подвздошной остеотомии минимальное
Именно поэтому во всем мире больные с экстрофией мочевого пузыря концентрируются в крупных клиниках, имеющих большой опыт проведения подобных операций. Наш коллектив именно такой. Наша экстрофийная бригада урологи (Рудин Юрий Эдвартович и Марухненко Дмиртий Витальевич) обладают более 20 летним опытом закрытия мочевого пузыря у новорожденных. Это чрезвычайно важно при пузырных площадках малого размера. В нашей команде квалифицированный ортопед Чекериди Юрий Элефтерович, который накопил опыт подвздошных остеотомий при экстрофии более чем у 100 пациентов различного возраста (включая новорожденных) . Данный подход позволяет нам достигать лучших результатов лечения столь тяжелой патологии. В нашей стране нет четкого регламентирования проведения этих операций и зачастую хирурги из регионов обладающие опытом только 1-3 операций пытаются оперировать данных больных. Закрыть пузырь можно, но важно не только укрыть пузырь и погрузить его в область малого таза, но и создать удерживающий мочу механизм, для обеспечения роста пузыря в дальнейшем, для этого целесообразно иметь несколько больший опыт. Кроме того необходимо мобилизовать кавернозные тела полового члена для максимального увеличения его длины. Каждая повторная операция снижает эффективность лечения из-за грубых рубцовых процессов. Обращайтесь к профессионалам с опытом лечения этой сложно и достаточно редкой патологии
Если у Вас в городе или области родятся больные с экстрофией мочевого пузыря вы можете получить консультацию по тактике лечения и возможности проведения операции. Сразу после рождения важно сохранить поверхность слизистой мочевого пузыря от воспаления и булезных разрастаний. Для этого можно успешно использовать полиэтиленовую мягкую пленку (пищевую пленку для упаковки продуктов, она продается в рулонах) . Вырезается из пленки квадрат 12х12мм и делают 4-5 точечных отверстий в центре.для эвакуации мочи. Пленкой с отверстиями укрывают поверхность пузыря и одевают подгузник. Мы имеем колоссальный опыт проведения таких операций. Число осложнений минимально. Важно помнить, что детей желательно оперировать в первые 3-10 дней после рождения. Вы можете направить этих больных (при наличии Российского гражданства и страхового полиса у родителей, граждане других государств могут проходить лечение по хозрасчету) в клинику для дальнейшего лечения только после предварительного согласования с проф. Рудиным Ю.Э. по телефону (499) 164-13-65, 8-905-555-05-39. Не упустите время, проконсультируйтесь со специалистами
rudin761@yandex.ru
Читайте также статью “Первичная пластика мочевого пузыря местными тканями при экстрофии у детей” на сайте Российского независимого интернет-сообщества пациентов с экстрофией мочевого пузыря: https://bladderexstrophy.ru/articles-rudin-pervichnaya-plastika.html
Ю.Э.Рудин, Ю.Ю.Соколов, А.Ю.Рудин, А.С.Кирсанов, Е.В.Карцева. Объем операции при первичном закрытии мочевого пузыря у детей с экстрофией мочевого пузыря.
Ж. Детская Хирургия. 2020. №1, С.21-28 (1560-9510 (); 2412-0677 (Online) (№ 858 из Перечня ВАК)
Ю.Э.Рудин, Ю.Ю. Соколов, А.Ю. Рудин, Д.В. Марухненко, В.И. Руненко, А.С. Кирсанов, Е.В. Карцева, Н.В. Медведева Отсроченное первичное закрытие мочевого пузыря у детей с экстрофией и микроцистисом . Ж.Экспериментальная и клиническая урология. 2020 № 4. С. 146-154. (№ 2250 из Перечня ВАК)
Источник
