Пластика мочевого пузыря осложнения

Варианты резекций; кровоснабжение сегментов мочевого пузыря
Радикальные хирургические вмешательства являются неотъемлемой частью комбинированного лечения злокачественных образований мочевого пузыря.
В настоящее время есть два основных метода:
1) резекция (в том числе трансуретральное удаление опухоли),
2) цистэктомия (тотальная и радикальная).
Органосохраняющие операции, которые мы разрабатывали многие годы, по-прежнему представляют серьезную конкуренцию цистэктомии (Поляничко М.Ф., 1986, 1991, 2000 гг.) особенно при условии использования в комбинированном лечении лучевых и химиотерапевтических компонентов.
В настоящее время мы различаем экономную и расширенную резекцию; последнюю под разделяем в зависимости от объема поражения на: верхнюю, сагиттальную (верхнесагиттальную), нижнюю (нижнесагиттальную) резекции, которые мы производим при новообразованиях (ТЗ-Т4) или больших опухолях категории Т2.
Исследование зон кровоснабжения мочевого пузыря показывает, что a.vesical.sup. кровоснабжает большую часть детрузора (3S). Передненижняя поверхность (1-2S) кровоснабжается a.vesical.inf., а задняя поверхность – a. deferentiales.
Верхняя гемицистэктомия с везикопластикой (чрезбрюшинный доступ)
Удаление значительных участков мочевого пузыря необходимо выполнять из трансперитонеального доступа с удалением паравезикальной клетчатки и лимфоузлов, особенно это касается опухолей 3S (Поляничко М.Ф., 2000). Размеры мочевого пузыря достаточно скромны в сопоставлении с другими органами, поэтому удаление больших сегментов наталкивается на ряд препятствий, обусловленных необходимостью трансплантации мочеточников и замещения различных по размерам пострезекционных дефектов.
Развитие онкоурологии, особенно в той части, которая относится к лечению рака мочевого пузыря, требует анализа отдаленных результатов по количеству и размеру удаляемых участков. В связи с этим нами была предложена схема объемов резекции, которая позволила четче разделить резекции на экономные и расширенные. К расширенным операциям мы отнесли удаление 2-3-х сегментов с уретероцистоанастомозом, лимфоденэктомией или аутопластикой. Эти операции отличаются от экономных резекций доступом, продолжительностью, количеством послеоперационных осложнений и в этом плане могут быть сопоставлены только с цистэктомией.

Пластика мочевого пузыря после расширенных резекций 1
После лапаротомии необходимо обратить особое внимание на заднюю стенку мочевого пузыря, которая может быть вовлечена в опухолевый инфильтрат. В таких случаях мочевой пузырь представляет собой бугристый конгломерат, врастающий в мышцы передней брюшной стенки, к нему часто припаяны петли тонкого и толстого кишечника (рис. 60-61).

Пластика мочевого пузыря после расширенных резекций 2
Подобный «симбиоз» ставит перед оператором непростую задачу – разделить сращения, отделив петли кишечника и определив условно здоровую часть мочевого пузыря. Чтобы не попасть на участок с опухолью, нужно максимально иссечь электроножом весь задний листок брюшины, а затем, отделив боковые отделы мочевого пузыря, не вовлеченные в инфильтрат, вскрыть мочевой пузырь. При необходимости нужно мобилизировать переднюю стенку до самой шейки и у нее вскрыть мочевой пузырь. Обычно при этой локализации опухоли передняя стенка остается интактной. В процессе самой резекции можно сформировать «малый мочевой пузырь». В ряде случаев можно восстановить мочевой пузырь, не прибегая к пластике (рис. 60), но его емкость будет небольшой.
Верхняя чрезбрюшинная гемицистэктомия с лимфаденэктомией при инвазивнбй опухоли (3S)
Мочевой пузырь восстановлен за счет боковых стенок с формированием эпицистостомы. Емкость мочевого пузыря – 50-60 мл.
Верхняя гемицистэктомия.
Пунктиром обозначена линия рассечения париетальной брюшины.
Часть пузыря с удаленной с обеих сторон тазовой клетчаткой и лимфоузлами.
Разрабатывая в течение многих лет альтернативные методы реконструкции, мы убедились в возможности (при использовании принципов каркасной регенерации) восстановления мочевого пузыря после удаления обширных его участков.
Создание каркаса и условий для регенерации после верхней гемицистэктомии осуществлялось в трех основных вариантах:
1. Формирование единого перитонеального лоскута для аутопластики.
2. Использование части боковых стенок, остатков брюшины и мышц передней брюшной стенки, сигмовидной кишки и передней брюшной стенки.
3. Использование изолированного кишечного сегмента.
Рассмотрим каждый из вариантов в отдельности.
Первый вариант везикопластики брюшиной
Успех аутопластики в первом варианте зависит от размеров оставшейся брюшины. Неровные края следует подровнять, а затем их сшить с внутренней поверхностью, используя атравматическую нить.
Этот этап операции следует выполнять с особой тщательностью, так как толщина брюшины составляет примерно 1-2 мм. Лучше формировать лоскут, вворачивая внутрь края, а затем сзади дополнить первую линию тонким узловым швом. После окончания этого этапа лоскут поворачиваем кпереди до уровня пирамидальных мышц, к которым он фиксируется непрерывно узловой атравматической кетгутовой нитью. В просвет вновь образованного резервуара вводится через уретру катетер Фоли и наполняется до 50 мл, мочеточники интубируются гонкими полихлорвиниловыми трубками, которые выводятся наружу вместе с надлобковым дренажем. После контроля на герметизм брюшная полость ушивается с оставлением дренажа.
В формируемую полость введен катетер Фоли. Продолжено сшивание оставшейся брюшины. Мочеточниковые дренажи выведены через мышцы передней брюшной стенки.
После введения надлобкового дренажа непосредственно в образованный «мочевой пузырь» листок брюшины фиксирован к прямым и пирамидальным мышцам.

Пластика мочевого пузыря после расширенных резекций 3

Второй вариант везикопластики – брыжжейкой, мышцами, сегментом кишки
При резекции с аутопластикой необходимо оставшиеся фрагменты мочевого пузыря тут же фиксировать к нормальным подлежащим тканям: шейку мочевого пузыря – к пирамидальным мышцам и надкостнице лобковых костей; внизу, при других вариантах резекции, – к апоневрозу Денонвилье или фасциальным элементам мышц таза.
Наиболее сложный и трудноосуществимый вариант аутопластики возникает при почти полном иссечении инфильтрированной брюшины и возникновении громадного дефекта мочевого пузыря.
После операции такого объема мы имеем малый таз, в глубине которого расположен trigonum Lietaudii и небольшая часть передней стенки, уходящая полоской к шейке мочевого пузыря. Вначале интубируем мочеточниковые устья. Затем непрерывным кетгутовым швом анастомозируем полуокружность тригонального отдела мочевого пузыря с брыжейкой сигмовидной кишки. Изнутри брыжейку укрепляем переходной складкой брюшины пузырно-ректального заворота с переходом на боковую стенку таза, формируя искусственную полость.
Далее расправляем кишку и брыжейку таким образом, чтобы она закрывала всю предполагаемую заднюю стенку, фиксируя ее к боковым листкам париетальной брюшины и к мышцам. Открыта только передняя стенка нормируемой полости. Перед ее закрытием в полость вводим катетер Фоли и наполняем его до нужных размеров (25-30 мм). Надлобковый дренаж устанавливаем через оставшуюся часть передней стенки мочевого пузыря или через мышцы, строго следя за тем, чтобы он не соприкасался со стенкой кишки.
Второй вариант везикопластики с использованием остатков брюшины и брыжейки сигмовидной кишки.




Третий вариант везикопластики мышцей брюшной стенки



Источник
Очеленко В.А.
Введение. Качественным этапом развития оперативной урологии стало экспериментальное обоснование и практическое применение различных сегментов желудочно-кишечного тракта (ЖКТ) для реконструкции мочевых путей. В настоящее время для замещения мочеточника и мочевого пузыря (МП) предложено и используется на практике более 80 различных вариантов реконструктивно-восстановительных операций [1,2].
Вначале с целью реконструкции обширных поражений верхних мочевыводящих путей (ВМП) поиск различных сегментов ЖКТ был в первую очередь направлен на восстановление адекватного оттока мочи из почек. С появлением разнообразных и многочисленных методов пластики мочеточника и МП появилась возможность сравнить их преимущества и недостатки. Наиболее физиологичными считаются способы ортотопической реконструкции мочевыводящих путей из различных сегментов ЖКТ, т.к. они позволяют восстановить естественное мочеиспускание через уретру и добиться наиболее полной медицинской и социально-психологической адаптации. По мнению E. Skinner [3], качество жизни (КЖ) является одной из основных движущих сил развития методов континентного отведения мочи.
При выборе способа реконструкции ВМП необходимо учитывать показания и противопоказания, вытекающие из преимуществ и недостатков того или иного способа, а также социальные и психологические последствия лечения для пациента, как представителя общества, в котором физическое здоровье и внешний вид являются одними из атрибутов профессиональной и частной жизни. Существует фактор качества жизни, который в современных условиях необходимо обязательно учитывать. К появлению многочисленных методов деривации мочи привело желание пациента быть социально адаптированным [4, 5].
Различные варианты реконструкции ВМП были многократно исследованы в плане эффективности и возникающих осложнений, однако в их сравнительную характеристику не были включены критерии качества жизни. В результате хирург выбирал метод, который имел минимальное количество осложнений, не учитывая, что он может губительно отразиться на качестве жизни данного пациента. При отборе больных для реконструкции мочевыводящих путей следует учитывать не только мнение хирурга, основанное на объективных критериях, но и интересы пациента, который вправе сделать самостоятельный выбор. В настоящее время результаты оперативного лечения оцениваются не только с точки зрения оперативной техники, сложности и объёма хирургического вмешательства. Определяющими показателями являются характер, частота осложнений, а также послеоперационная летальность и выживаемость. Последняя рассматривается с позиций физической и социально-психологической адаптации пациента в семье и обществе.
Основным показателем, который отражает состояние здоровья человека и позволяет получить ценную информацию об его индивидуальной реакции на болезнь и проводимое лечение является качество жизни, которое как термин было введено лишь в начале 80-х годов. Под понятием «качество жизни» (HRQOL) понимают интегральную характеристику физического, психологического, эмоционального, социального и духовного благополучия человека, основанную на его субъективном восприятии [6, 7].
Существует определенная зависимость между КЖ и различными осложнениями, возникающими в послеоперационном периоде. Однако в повседневной жизни пациенты чаще обращают внимание на неудобства, связанные с функциональными нарушениями и не замечают латентно протекающие осложнения (обструкция ВМП, рефлюкс и др.), которые сопровождаются ухудшением функции почки и в конечном счете могут стать серьезной угрозой для их жизни. Сегодня КЖ постепенно становится определяющим фактором при выборе хирургической тактики и требует дальнейшего изучения [8].
Материал и методы. С 1995 по 2012 г. было опрошено 298 пациентов (спустя 3 и более мес.) после замещения мочеточника и МП различными сегментами ЖКТ: 47- с интестинальной пластикой мочеточника (ИМП); 43 – с аугментационной цистопластикой (АЦП); 29 – с уретеросигмоанастомозом (УСА) и 179 – с ортотопическим мочевым пузырём после радикальной цистэктомии (РЦ). Мужчин среди них было 240 (80,5%), женщин -58 (19,5%). Возраст больных колебался от 18 до 82 лет и в среднем составил 67,2±9,5 лет. Показаниями к восстановлению мочевыводящих путей различными отделами желудочно-кишечного тракта были: протяженные стриктуры мочеточников, рак мочевого пузыря, микроцистис различного генеза и другие заболевания мочевыводящих путей. У 2 больных была произведена трансформация гетеротопического резервуара в ортотопический неоцистис.
Для оценки качества жизни использовали опросники, которые заполнялись пациентами и в процессе расшифровки позволяли получить интегрально-цифровую характеристику состояния здоровья больного. Методологическими основами любого опросника являются специфичность, многомерность характеристик качества жизни, возможность заполнения его больными и применимость к различным культурам. К современным версиям опросников, отвечающим этим требованиям, относятся: европейский – 2 EORTC QLQ-C30 (Quality of Life Questionnary-Core 30 of European Organisation for Re and Treatment Cancer) и американский – 4 FACT-G (al Assessment of Cancer Therapy-General) [9], включающие ряд вопросов и состоящие из нескольких функциональных шкал, к которым может быть добавлен модуль – дополнительные специфические вопросы [10]. Данный метод прост, надёжен, экономичен и информативен.
Исследование качества жизни пациентов производилось на основании опросника, состоящего из 34-х вопросов, и заполнения ими специальных карт. Вопросы делились на: 1) общие, характеризующие общее благосостояние, адаптацию в обществе и семье, умственный и эмоциональный статус, 2) определяющие, свидетельствующие о воздействии болезни на жизнедеятельность человека, – прежде всего, в виде осложнений деривации мочи и рецидивов заболевания, и 3) специальные, касающиеся особенностей жизни у лиц с суправезикальной деривацией мочи. При составлении опросных карт обязательно учитывались специфические особенности жизни пациентов после замещения мочевыводящих органов различными отделами ЖКТ и старались, чтобы они отвечали международным требованиям, а именно, были бы: 1) универсальными, 2) надёжными, т.е. способными при одних и тех же условиях давать одинаковые результаты при повторных исследованиях, 3) чувствительными к клинически значимым изменениям состояния здоровья каждого пациента, 4) воспроизводимыми, 5) простыми в использовании, 6) стандартизированными едиными вариантами вопросов и ответов для всех, 7) оценочными. С этой целью применялась специальная шкала в баллах от «0» наихудшей (наименьшей) до «5» – наилучшей (наивысшей) характеристики для данного явления (показателя), которую выбирал сам больной.
Результаты и их обсуждение. Количественная оценка общих показателей качества жизни представлена в табл.1.
Таблица 1. Общие показатели качества жизни у больных после замещения мочеточника и мочевого пузыря различными сегментами ЖКТ
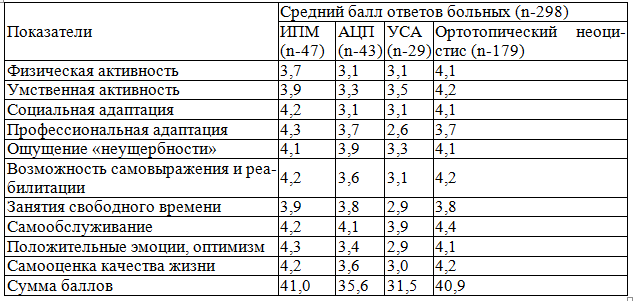
В данной таблице отсутствуют критерии, которые влияют на качество жизни, но не связаны со способом реконструкции ВМП. Имеются в виду: семейное положение, наличие родственников и друзей или одиночество; материально-жилищные условия; физическая и материальная поддержка или её отсутствие; психологическая и духовная поддержка или её отсутствие. Несмотря на известную долю субъективизма, наилучшую оценку своему состоянию дали пациенты, которые после реконструктивно-восстановительных операций имели возможность контролировать и осуществлять мочеиспускание через уретру. Непривычное и нефизиологическое для больных отведение мочи через анус негативно отражается практически на всех общих показателях качества их жизни. Невысокую оценку своему состоянию дают больные после АЦП, которые после операции ожидают полного восстановления утраченной функции МП. Больные раком мочевого пузыря, осведомленные о своем заболевании и альтернативных методах отведения мочи, воспринимают ортотопический артифициальный МП с большим оптимизмом и дают высокую самооценку качества своей жизни.
Не менее важное влияние на жизнедеятельность человека оказывают течение основного и сопутствующих заболеваний, а также осложнения, связанные с хирургическим вмешательством и способом отведения мочи. В табл. 2 приведена взаимосвязь между качеством жизни пациентов с отведением мочи в сегменты ЖКТ и болезненными состояниями, возникающими в результате рецидивов злокачественного процесса, сопутствующих заболеваний и осложнений, связанных с особенностями суправезикальной деривации мочи.
Таблица 2. Показатели, определяющие воздействие заболеваний (осложнений) на качество жизни у больных после замещения мочеточника и мочевого пузыря различными сегментами ЖКТ
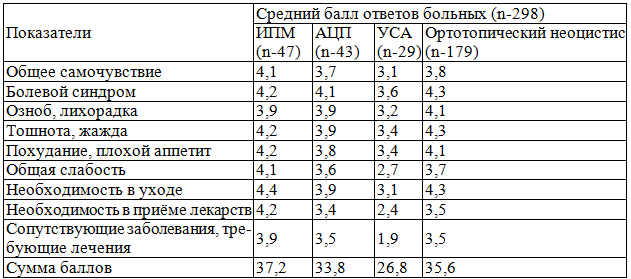
Развитие ранних и поздних осложнений существенно отражалось на КЖ пациентов, которые нуждались в постороннем уходе, постоянном медицинском наблюдении, лекарственной и хирургической коррекции. Показателями осложнённого течения послеоперационного периода в отдалённые сроки являлись: неудовлетворительное общее самочувствие, ознобы, повышения температуры тела, тошнота и жажда, прогрессирующая общая слабость, похудание, плохой аппетит и сон, болевой синдром. Сопутствующие заболевания негативно влияли на общее самочувствие пациентов и требовали дополнительного лечения. При опросе больных отсутствие перечисленных показателей оценивалось высшим баллом, а их наличие по степени тяжести – низшим.
Лучшие показатели качества жизни были получены у пациентов с интестинальной пластикой мочеточника (ов) и ортотопическим МП, имеющих минимальное количество послеоперационных осложнений. Наиболее часто проблемы, связанные с деривацией мочи, возникали у больных с пересадкой мочеточников в сигмовидную кишку, о чем свидетельствует низкие показатели уровня их жизни. Невысокие показатели качества жизни после АЦП по сравнению с ортотопическим МП объясняются отсутствием у этих пациентов злокачественного процесса и, соответственно, более требовательными отношением к результатам реконструктивных операций. С другой стороны в эту группу вошел наиболее тяжелый контингент больных, страдающих туберкулезом мочевой системы и имеющих высокий риск послеоперационных осложнений, которые в конечном счете, развивались в большинстве случаев.
Специальные вопросы касались специфических особенностей жизни, которые возникают у пациентов с деривацией мочи в сегменты ЖКТ. Главным образом, они затрагивали проблемы, связанные с актом мочеиспускания. Минимальный балл соответствовал наихудшим, а максимальный – наилучшим результатам – см. табл. 3.
Таблица 3. Специальные показатели качества жизни у больных после замещения мочеточника и МП различными сегментами ЖКТ
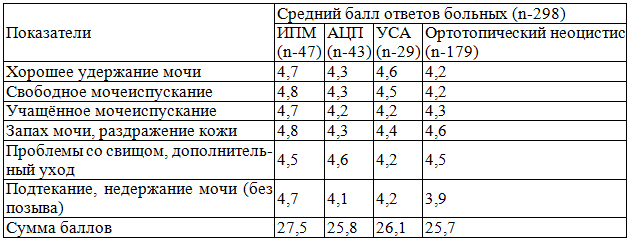
Кишечная пластика мочеточника приводила к увеличению емкости МП и улучшению его уродинамических показателей. Поэтому неудивительно, что качество их жизни оказалось наилучшим. Практически одинаковые результаты были получены при аугментационной и ортотопической цистопластике после РЦ, которые оказались хуже по сравнению с различными вариантами УСА. Т.е. лучшее качество жизни и наименьшее количество проблем, связанных с актом мочеиспускания, отмечали пациенты с анальным отведением мочи.
Для определения общего уровня жизни прооперированных больных на основании полученных ответов суммировали средние баллы всех показателей качества жизни. Сумма баллов от 0 до 45 соответствовала низкому, от 46 до 90 среднему и от 91 до 135 высокому КЖ. Из приведённой табл. 4 видно, что из 298 опрошенных пациентов 6,7% имели низкий, 56,7% – средний и 36,6% – высокий уровень жизни. Подсчет суммы средних баллов основных показателей качества жизни показал, что при правильном отборе больных использование сегментов ЖКТ для отведения мочи позволяет добиться удовлетворительного уровня жизни (табл. 5).
Таблица 4. Общий уровень жизни больных с различными методами отведения мочи (n-298)
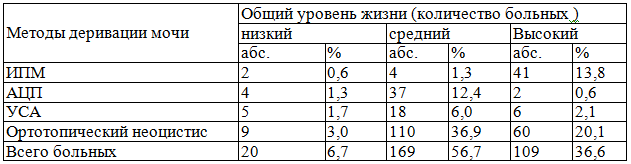
Таблица 5. Средние показатели качества и общего уровня жизни больных с различными вариантами отведения мочи в сегменты ЖКТ
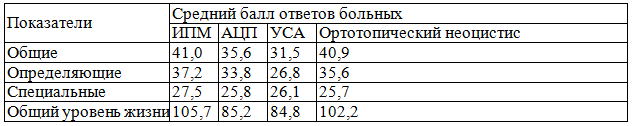
Таким образом, наилучшие показатели качества и общего уровня жизни были получены у больных с кишечной пластикой мочеточника. При сравнении различных вариантов замещения МП с точки зрения социально-психологической и медицинской адаптации качество жизни оказалось лучше при создании ортотопических искусственных резервуаров с восстановлением физиологического мочеиспускания по уретре. В то же время ответы на специальные вопросы, касающиеся акта мочеиспускания, показали преимущества анального отведения мочи. В результате проведенного опроса всех больных 92,7% из них отмечали удовлетворительный уровень жизни.
Заключение. Наилучшие показатели качества и общего уровня жизни были получены у больных с кишечной пластикой мочеточника. При сравнении различных вариантов замещения МП с точки зрения социально-психологической и медицинской адаптации качество жизни оказалось лучше при создании ортотопических искусственных резервуаров с восстановлением физиологического мочеиспускания по уретре. Качество жизни больных после замещения мочевыводящих органов сегментами ЖКТ главным образом зависит от характера, частоты осложнений и степени удержания мочи, а у онкологических пациентов от распространенности, инвазии злокачественного процесса и радикальности хирургического лечения. Отношение пациентов к различным методам отведения мочи и результатам реконструктивно-восстановительных операций не всегда совпадает с мнением хирурга, т.к. целый ряд осложнений (хроническая почечная недостаточность, метаболический ацидоз, уретеральные стрикуры, рефлюкс и др.), представляющие реальную угрозу их жизни, протекают бессимптомно и существенно не отражаются на субъективной оценке качества жизни. Выбор метола лечения оперирующего врача основан на клинической эффективности метода с учетом индивидуальных особенностей конкретного пациента. Самого больного в первую очередь интересует качество жизни после операции.
Рациональное использование сегментов ЖКТ в восстановительной хирургии мочевыводящих органов позволяет добиться удовлетворительных функциональных результатов у большинства оперированных больных.
Источник
