Пикамилон при гиперактивном мочевом пузыре
Нейрогенные дисфункции мочевого пузыря (НДМП) являются одной из актуальных проблем детской урологии, что связано с значительным ростом количества пациентов данного профиля [1–5, 7, 8]. Наряду с расстройствами мочеиспускания, которые приводят к значительному снижению качества жизни ребенка, проявляющемуся социальной изоляцией, снижением уровня самооценки, конфликтам в семье, детском саду, школе, это заболевание может стать причиной развития вторичных изменений со стороны мочевыводящей системы — рецидивирующего хронического цистита, пиелонефрита, пузырно-мочеточникового рефлюкса, уретерогидронефроза, приводящих к нефросклерозу, артериальной гипертензии и хронической почечной недостаточности. Это и обуславливает постоянный поиск путей улучшения лечения данной патологии [1–6, 8, 10].
В свете новых патогенетических аспектов формирования дисфункции мочевого пузыря, роли сложнейших биологических процессов и, в частности, «гипоксии» детрузора, в настоящее время широко применяется лечение препаратом Пикамилон (натриевая соль N-никотил-гамма-аминомасляной кислоты) — амидным производным никотиновой кислоты и гамма-аминомасляной кислоты, обладающим ноотропным, антигипоксическим и антиоксидантным эффектом. Однако использование только этого препарата не всегда оказывает положительный эффект. Способность нормализовать детрузорно-сфинктерные отношения у ряда производных нейромедиаторных кислот (Глицин, Пирацетам, Тауфон) является многообещающим в терапии НДМП. Именно результатам применения ряда таких аминокислот посвящена данная работа [3, 5, 9, 10].
Материалы и методы
Мы проанализировали особенности клинических проявлений, уродинамических показателей в зависимости от вида терапии нейрогенной дисфункции мочевого пузыря, в частности, гиперрефлекторного типа, у 185 детей в возрасте от 3 до 15 лет, из них 84 мальчика и 101 девочка.
Соотношение полов (1:1,5) в нашем исследовании подчеркивает определенное неблагоприятное влияние эстрогенов на уродинамику верхних и нижних отделов мочевых путей. Известно, что гиперрефлексия у девочек с нестабильным мочевым пузырем сопровождается нарастанием эстрогенной насыщенности, обусловливающей повышение чувствительности М-холинорецепторов к ацетилхолину [2]. Это объясняет преобладание детей женского пола в совокупной группе больных с расстройствами мочеиспускания функциональной природы.
Всем детям проводили обследование, включающее клинические и биохимические анализы мочи и крови, бактериологическое исследование мочи, ультразвуковое исследование почек и мочевого пузыря, урофлоуметрию и ретроградную цистометрию.
Все дети были разделены на V групп, каждая из которых состояла из 37 детей обоего пола:
- I группа — группа сравнения, получала антихолинергетики, седативные препараты, витаминотерапию и физиолечение.
Четыре испытуемые группы получали различные аминокислотные препараты внутрь:
- II группа — Пирацетам, из расчета 50 мг/кг/сут в три приема, перорально, после еды;
- III группа — Пикамилон (никотиноил-гамма-аминомасляная кислота), из расчета 5 мг/кг/сут в три приема, перорально, после еды;
- IV группа — Тауфон (таурин), из расчета 50 мг/кг/сут в три приема, перорально, до еды;
- V группа — Глицин, из расчета 50 мг/кг/сутки в три приема, перорально, до еды.
В комплексе с аминокислотами назначались витамины группы В, РР, А и Е в возрастных дозировках, антихолинергетики (Беллатаминал), седативные препараты (растительного происхождения — валериана и пустырник) и физиопроцедуры. Курс лечения составил 1–1,5 месяца.
Учитывая, что таурин, глицин и производные гамма-аминомасляной кислоты являются тормозными аминокислотами, они назначались детям с гиперрефлекторной формой нейрогенной дисфункции.
Результаты и обсуждение
Нейромедиаторные аминокислоты широко используются в педиатрии, но нами обнаружены их новые свойства, а именно — способность оказывать определенное влияние на детрузорно-сфинктерные отношения с уменьшением степени выраженности или полным прекращением расстройств акта мочеиспускания как днем, так и ночью. Наиболее стабильно обратному развитию подвергались симптомы, отражающие выпадение резервуарной функции мочевого пузыря, — поллакиурия, императивные позывы, императивное недержание мочи и энурез. Согласно данным суточного режима спонтанных мочеиспусканий, до лечения и в группе сравнения и во всех испытуемых группах частота мочеиспусканий была 9,7 (при норме от 4 до 5 раз в сутки); минимальный эффективный объем мочевого пузыря 34,4 мл (при норме от 46 до 68 мл); эффективный средний объем 103,4 мл (при норме 140–192 мл); максимальный объем 133,6 мл (при норме 191–325 мл). Эти показатели свидетельствовали о наличии гиперрефлекторного мочевого пузыря (табл. 1).
После проведенного лечения в группе сравнения, получавшей традиционное лечение, частота мочеиспусканий осталась прежней. В группах, получавших то же лечение в комплексе с аминокислотами, произошла существенная положительная динамика. Так, частота мочеиспусканий уменьшилась до 5,0. Увеличился также эффективный объем мочевого пузыря (минимальный, средний, максимальный), что представлено в табл. 1. По результатам суточного ритма спонтанных мочеиспусканий можно судить об аналогичном действии всех препаратов, наименее выраженном при применении пирацетама.
По данным урофлоуметрии и ретроградной цистометрии (табл. 2 и 3) видно, что клиническому улучшению функции мочевого пузыря соответствовали увеличение порога его чувствительности и рефлекторной возбудимости, то есть возрастание способности к накоплению и удержанию мочи (резервуарная функция). В не меньшей степени действие медиаторных аминокислот затрагивало адаптационную способность детрузора.
По данным урофлоуметрии, до лечения у всех детей с нейрогенной дисфункцией мочевого пузыря общий объем мочи и средняя скорость эвакуации были меньше нормы. Так, средняя скорость в группе сравнения составляла 6,4 мл/с; в группе, получавшей аминокислоты, — 4,7 мл/с (при норме 9,7 мл/с). Общий объем эвакуации в группе сравнения составил 105,1 мл, в испытуемой группе — 86,7 мл (табл. 2).
После лечения у детей, получавших медиаторные аминокислоты, происходило увеличение общего объема эвакуации от 92 мл до 130 мл, а средней ее скорости от 7,7 до 9,4 мл/с. В группе сравнения эти изменения отсутствовали (табл. 2).
По эффективности воздействия на эти показатели препараты распределились следующим образом: Тауфон > Пикамилон ≥ Глицин > Пирацетам, то есть наименее действенным был Пирацетам.
При анализе результатов ретроградной цистометрии у больных с гиперрефлекторным мочевым пузырем до лечения аминокислотами отмечается уменьшение порога чувствительности — первый позыв на мочеиспускание, рефлекс и опорожнение мочевого пузыря происходят при меньшем его объеме, отмечается повышение внутрипузырного сопротивления за счет гипертонуса детрузора. Vmax — объем мочевого пузыря до лечения — был в среднем равен 113,0 мл (норма 225,0 мл). Vn — объем мочевого пузыря при первом позыве до лечения — в среднем составил 37 мл (норма 125 мл). T — тонус детрузора до лечения — в среднем был 7,5 (при норме 2,9–4,0) (табл. 3).
После лечения аминокислотами у детей во II–V группах отмечено увеличение порога чувствительности — первый позыв на мочеиспускание, рефлекс и опорожнение мочевого пузыря происходили при большем его объеме, нормализовался тонус детрузора. После лечения: Vmax — восстанавливался до 188 мл. Vn — в среднем составил 99 мл. T — тонус детрузора после лечения — в среднем 3,0. У детей в группе сравнения достоверных изменений нет (табл. 3).
По воздействию на порог чувствительности позыва к мочеиспусканию препараты были приблизительно равными, за исключением Пирацетама: (Тауфон = Глицин = Пикамилон) > Пирацетам.
При контрольном обследовании детей с нейрогенной дисфункцией мочевого пузыря через 6 месяцев после лечения у детей, получавших аминокислоты, сохранялись нормальные показатели уродинамики. В группе сравнения достоверных изменений показателей, сравнительно с исходными, не отмечено.
При изучении ритма спонтанных мочеиспусканий: урежение частоты мочеиспускания и сохранение увеличенного объема мочевого пузыря через 6 месяцев после окончания лечения выражено только в IV и V группах, получавших Тауфон и Глицин.
При проведенной в катамнезе урофлоуметрии только у детей IV группы, получавших Тауфон, по двум показателям сохраняется достоверное увеличение средней скорости эвакуации и увеличение общего объема мочи, в остальных группах достоверных различий с исходными данными нет.
Через 6 месяцев после окончания лечения по данным ретроградной цистометрии у детей III, IV, V групп отмечаются достоверные различия по всем трем показателям: сохраняется увеличение максимального объема мочевого пузыря, увеличение объема при первом позыве и нормализация тонуса детрузора.
Учитывая результаты проведенного обследования, можно сделать вывод, что производные ГАМК, Тауфон и Глицин оказывают положительное влияние на уродинамику нижних мочевых путей как на центральном, так и на периферическом уровне [9–11].
Литература
- Вишневский Е. Л., Лоран О. Б., Вишневский А. Е. Клиническая оценка расстройств мочеиспускания. М.: ТЕРРА, 2001. 96 с.
- Державин В. М., Вишневский Е. Л., Абдурахманов Х. И. Роль эстрогенов в патогенезе нейрогенной дисфункции мочевого пузыря гиперрефлекторного типа и пузырно-мочеточникового рефлюкса у детей // Педиатрия. 1990. № 4. С. 10–14.
- Джавад-Заде М. Д., Державин В. М., Вишневский Е. Л. и др. Нейрогенные дисфункции мочевого пузыря. М.: Медицина. 1989. 383 с.
- Кириллов В. И., Киреева Н. Г. Нейрогенные дисфункции мочевого пузыря у детей // РМЖ. 1998. Т. 6, № 9. С. 587–593.
- Кольбе О. Б., Сафонов А. Б., Сазонов А. Н. и др. Современные аспекты клиники, диагностики и лечения нейрогенных дисфункций мочевого пузыря // Педиатрия. 2000. № 4. С. 34–39.
- Лопаткин Н. А., Пугачев А. Г. Детская урология. М.: Медицина. 1986. 490 с.
- Маркова И. В., Неженцев М. В., Папаян А. В. Лечение заболеваний почек у детей. СПб: Сотис. 1994. 389 с.
- Марушкин Д. В., Артюхина С. В. Нейрогенные дисфункции мочевого пузыря. Уч. пособие. Волгоград, 1996. 18 с.
- Марушкин Д. В., Петров В. И., Папаян А. В. Результаты применения пикамилона в терапии недержания мочи у детей // Материалы Российской конференции «Пикамилон — в лечебной практике». М., 1994. С. 96–100.
- Папаян А. В., Марушкин Д. В. Ночное недержание мочи у детей. Уч. пособие. Волгоград, 1996. 19 с.
- Трошкин В. М., Радаева Т. М., Куркина С. А. Расстройства мочеиспускания у детей (Уч. пособие). Нижний Новгород, 2000. 24 с.
С. Н. Зоркин*, доктор медицинских наук, профессор
О. И. Маслова*, доктор медицинских наук, профессор
С. В. Артюхина**, доктор медицинских наук
С. А. Борисова*
*НЦЗД РАМН, Москва
**Центр патологии мочеиспускания, Волгоград
Контактная информация об авторах для переписки: zorkin@nczd.ru
Источник
Комментарии
Е.Л. ВИШНЕВСКИЙ, И.С. БЕЛОУСОВА
ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава»
Международным обществом по вопросам удержания мочи в 2004 году для описания расстройств мочеиспускания рекомендован к использованию новый термин – синдром гиперактивного мочевого пузыря (ГАМП), характеризующийся поллакиурией, императивными позывами и императивными недержаниями мочи различной степени выраженности, часто – в сочетании с энурезом.
В отечественной литературе для обозначения данного состояния традиционно использовался термин «нейрогенная дисфункция мочевого пузыря», в рамках которого в зависимости от состояния резервуарной пузырной функции выделялось три варианта патологии: гипер-, нормо- и гипорефлекторный мочевой пузырь.
В КАКОМ ВОЗРАСТЕ СИМПТОМОКОМПЛЕКС ГАМП У ДЕТЕЙ СТОИТ СЧИТАТЬ ЗАБОЛЕВАНИЕМ?
К 4 годам большинство детей имеют волевой контроль основных функций мочевого пузыря и формируют «зрелый тип мочеиспускания», характеризующийся:
полным удержанием мочи днем и ночью;
- умением задерживать и прерывать при необходимости акт мочеиспускания;
- умением опорожнять мочевой пузырь без предшествующего позыва на мочеиспускание;
- поведенческие реакции, сопровождающие акт мочеиспускания – стремление к уединению при появлении позыва и пр.
В норме дети 3-4 лет опорожняют мочевой пузырь 5-8 раз во время бодрствования; средний эффективный объем мочевого пузыря колеблется от 80 до 150 мл.
Таким образом, о формировании симптомо-комплекса ГАМП можно говорить, если у ребенка 4 лет и старше число мочеиспусканий и эффективный объем мочевого пузыря выходят за рамки нормативных показателей, мочеиспускание неконтролируемо в той или иной степени.
Очевидно, что в силу негативного влияния ГАМП на качество жизни и риска присоединения микробно-воспалительных заболеваний мочевой системы нарушения мочеиспускания подлежат ранней диагностике и лечению.
ПРИНЦИПЫ ЛЕЧЕНИЯ ГАМП
С 1870 года единственными хорошо изученными и эффективными средствами медикаментозного лечения данной патологии являются препараты на основе атропина – М-холинобло-каторы. И в настоящий момент М-холинобло-каторы (оксибутинина гидрохлорид, толтеро-дина тартрат) остаются препаратами первого ряда в лечении симптомов гиперактивного мочевого пузыря (Международное общество по вопросам удержания мочи, 2000).
М-холиноблокаторы демонстрируют высокую эффективность при подавлении неконтролируемых сокращений детрузора. Однако наряду с этим им свойственна высокая частота появления системных побочных эффектов: общая атропинизация (40-65%) и нарушения со стороны центральной нервной системы (10-15%), которые становятся главным ограничением при лечении. При этом частота возникновения побочных эффектов у детей в 4 раза превосходит таковую у взрослых. Из-за выраженности побочных эффектов терапию вынуждены прекращать 10-30% пациентов.
Все вышеперечисленное диктует необходимость поиска новых этиопатогенетических методов лечения гиперактивного мочевого пузыря у детей.
В последние годы детально изучается влияние гипоксии на функцию мочевого пузыря. Нарушения кровоснабжения мочевого пузыря, тканевая гипоксия и сопряженные нарушения биоэнергетики детрузора признаны важнейшими патогенетическими звеньями расстройств мочеиспускания. Объясним интерес к средствам оптимального фармакологического воздействия на них.
Основным средством метаболической терапии, широко используемым при лечении расстройств мочеиспускания, является препарат из группы ноотропных средств – Пикамилон.
Ранее было показано, что у большинства детей симптомокомплекс ГАМП разворачивается на измененном биоэнергетическом фоне (на фоне политканевой митохон-дриальной дисфункции), оказывающем заметное влияние на формирование и клинические проявления расстройств мочеиспускания. Это явилось основанием для использования в лечении данной патологии препарата L-карнити-на (Элькар®).
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
При анализе имеющихся разрозненных данных об эффективности использования различных метаболических препаратов возникают практические вопросы. Какова их сравнительная клиническая эффективность у детей с ГАМП? У какой категории пациентов использование изучаемых фармакологических средств является наиболее обоснованным и эффективным?
Нами была проведена сравнительная оценка клинической эффективности Элькара и Пи-камилона в режиме монотерапии у детей с ГАМП различной степени тяжести
Обследовано 77 детей с ГАМП в возрасте от 4 до 15 лет. Максимальное количество дисфункций приходилось на дошкольный возраст. Клиническая картина заболевания характеризовалась поллакиурией, императивными позывами и императивными недержаниями мочи различной степени выраженности, часто в сочетании с энурезом.
Использованы общепринятые лабораторные и рентген-урологические методы обследования. Учитывая вариабельность клинической картины, для объективизации оценки расстройств мочеиспускания использовалась квали-метрическая Таблица оценки расстройств мочеиспускания, составленная на основании рекомендаций Международного комитета по удержанию мочи у детей с учетом возрастных нормативов (табл.1). Результатом заполнения таблицы являлся суммарный балл расстройств мочеиспускания, определенный в качестве главного объективного критерия для оценки выраженности клинической симптоматики и эффективности терапии.
Таблица 1
Ф.И.О.________________________________________________________________________№и/б
Дата рождения__________________________________________________________________Пол
| ТАБЛИЦА ОЦЕНКИ МОЧЕИСПУСКАНИЯ (для детей от 4 до 15 лет) | ||||
| Параметр | Балл | |||
| 1. Позыв на мочеиспускание | Нормальный Императивный — не каждый день Императивный — каждый день 1 раз Императивный — каждый день неск. раз | 0 1 3 5 | ||
| 2. Императивное недержание мочи | Нет Не каждый день Каждый день — 1 раз Каждый день — несколько раз | 0 1 3 5 | ||
| 3. Непроизвольное мочеиспускание во время сна | Нет Несколько раз в месяц Несколько раз в неделю Каждую ночь — 1 раз Каждую ночь — несколько раз Во время дневного сна | 0 1 3 5 7 7 | ||
| 4. Ритм спонтанных мочеиспусканий | А. Число м/и в сутки: | |||
| 1-2 3-4 5-6 7-8 9-10 11-12 13-14 15-16 17-18 19-20 Более 21 | 6 3 2 4 6 8 10 12 14 | |||
| Б. Средний эффективный объем мочевого пузыря, мл | Возраст, лет | |||
До 50 мл 51-75 76—100 101—125 126-150 151—175 176—200 201—250 251-300 Более 300 Ср. эффективный объем, мл | 4-7 4 3 2 1 1 2 3 | 8-11 5 4 3 2 1 1 2 | 12-15 6 5 4 3 2 1 1 | |
| Диурез с 1800 до 600 в % от суточного | До 40% 41—50% 51—60% 61—70% Более 71% | 0 3 6 9 12 | ||
| Суммарный балл | ||||
В зависимости от степени выраженности расстройств мочеиспускания, определенных по квалиметрическим таблицам, для анализаклинических наблюдений было выделено 3 группы больных:
- 1 группа – легкая степень расстройств мочеиспускания, суммарный балл 2-10.
- 2 группа – средняя степень расстройств, суммарный балл 11-20.
- 3 группа – тяжелая степень расстройств мочеиспускания, суммарный балл 21-30.
Курс терапии L-карнитином (Элькар®, компания «Пик-Фарма», Россия) получили 43 ребенка. 34 пациентам проведено лечение вазоактив-ным препаратом Пикамилоном. Распределение детей случайное.
Общая оценка эффективности терапии проводилась на основании рекомендаций Международного общества по удержании мочи у детей (1998 г.) по динамике эпизодов недержаний мочи и/или энуреза. Ответ на лечение считался полным в случае исчезновения более чем 90% эпизодов недержания мочи; частичным (улучшение) – при снижении числа эпизодов недержаний мочи на 50-90%; уменьшение числа эпизодов недержаний мочи менее чем на 50% расценивалось как отсутствие ответа (резистентность).
Проведенный по окончанию месячного курса терапии анализ динамики исходных клинических показателей расстройств мочеиспускания показал, что терапевтическая эффективность Элькара составила 84%, тогда как эффективность Пикамилона составила 80%. Более чем в половине наблюдений ответ на терапию Элькаром носил частичный характер и заключался в уменьшении количества эпизодов недержания мочи на 50-90%
У пациентов, получавших Элькар, было зарегистрировано достоверное снижение суммарного балла расстройств мочеиспускания с 13,8 до 6,3, т.е. на 56% от исходного, что не отличалось от регрессии клинической симптоматики на фоне приема Пикамилона.
На фоне терапии Элькаром наиболее стабильно обратному развитию подвергались дневные симптомы ГАМП, в то время как энурез являлся стойким и медленно поддающимся обратному развитию симптомом – его редукция отмечена только в половине наблюдений.
Во всех немногочисленных случаях исчезновения энуреза достигнутый эффект был нестойким. У 4 детей на фоне уменьшения дневных симптомов расстройств мочеиспускания ночная продукция мочи и кратность энуреза увеличились.
Эффективность терапии Элькаром зависела от исходной степени выраженности расстройств мочеиспускания. Так, при легкой и средней степени тяжести расстройств эффективность терапии составила 81 и 93% соответственно, при тяжелой степени – не превышала 66%. Во всех трех группах в большинстве наблюдений отмечался частичный ответ на терапию.
У детей с исходно сниженной емкостью мочевого пузыря Элькар оказывал позитивное влияние на резервуарную функцию: при легкой и средней степени тяжести расстройств мочеиспускания среднеэффектив-ный объем мочевого пузыря увеличился на треть (31 и 29%), а при тяжелой – более чем на половину.
Примечательно, что при тяжелой степени расстройств увеличение резервуарной способности мочевого пузыря на фоне приема Элькара было более существенным по сравнению с Пикамилоном. В то время как влияние Пикамилона на резервуарную функцию было гораздо более значимым у детей со средней степенью нарушений.
У пациентов с исходно увеличенным сред-неэффективным объемом мочевого пузыря вне зависимости от исходной степени тяжести расстройств Элькар влияния на резервуарную функцию не оказывал. Практически все дети остались резистентыми к терапии.
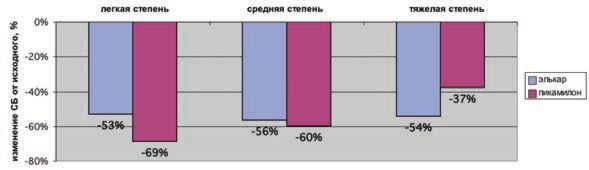
Обратная динамика симптомов расстройств мочеиспускания на фоне приема Элькара в целом схожа с показателями, достигнутыми на фоне приема Пикамилона. Исключение составили дети с исходно тяжелой степенью расстройств, у которых улучшение клинической симптоматики на фоне приема Элькара было более существенным (рис. 1).
Рисунок 1 
Изменение суммарного балла расстройств мочеиспускания (по Таблицам расстройств мочеиспускания) от исходного у детей с ГАМПразличной степени тяжести на фоне терапии элькаром и пикамилоном.
Примечание: СБ — суммарный балл по таблицам расстройств мочеиспускания.
Рисунок 2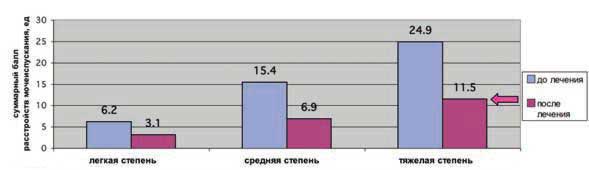
Суммарный балл расстройств мочеиспускания (по Таблицам расстройств мочеиспускания) у детей с ГАМП различной степени тяжести до и после терапии элькаром
Обратная динамика симптомов расстройств мочеиспускания на фоне терапии Элькаром была практически одинаковой у детей с различной исходной тяжестью расстройств и составляла 53-56% от базового показателя. Однако, учитывая различный стартовый уровень выраженности клинических проявлений, достигнутые на фоне лечения показатели принципиально различались. Так, у детей с исходно умеренной степенью расстройств мочеиспускания произошло их уменьшение до легкой степени, пациенты с тяжелой степенью расстройств к моменту окончания лечения сохраняли нарушения средней степени (рис.2).
Таким образом, проведенное исследование показало, что у детей с гиперактивным мочевым пузырем препарат Элькар в режиме монотерапии демонстрирует высокую клиническую эффективность, сопоставимую с действием Пикамилона – традиционного метаболического средства, используемого при лечении изучаемой патологии. Оба препарата имеют хорошую переносимость.
Элькар оказывает более выраженное позитивное влияние на дневные симптомы расстройств мочеиспускания, отражающие выпадение резерву-арной функции (поллакиурия, императивные позывы, императивное недержание мочи).
Применение Элькара в режиме монотерапии в лечении детей с гиперактивным мочевым пузырем является оправданным в случае исходной выраженности расстройств мочеиспускания легкой (0-10 баллов) и средней (11-20 баллов) степени при сохранной или сниженной резервуарной функции.
У детей с тяжелой выраженностью симптомов (более 21 балла) терапия Элькаром оказывает достоверное позитивное действие на изучаемые клинические параметры расстройств мочеиспускания, однако достигнутый при этом эффект не является достаточным для их нормализации. Исходя из полученных данных, можно ожидать, что у данной категории пациентов включение Элькара в комбинированную терапию позволит улучшить результаты лечения.
Данные клинических исследований позволяют применять обоснованный дифференцированный подход к лечению детей с ГАМП и оптимизировать лечебную тактику.
Сведения об авторах: Евгений Леонидович Вишневский, руководитель отдела урологии и нейроурологии ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава», профессор, д-р мед. наук
Ирина Станиславовна Белоусова, сотрудник отдела урологии и нейроурологии, ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава», канд. мед. наук
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
