Обострение хронического пиелонефрита и мочекаменной болезни
Актуальность. Заболеваемость мочекаменной болезнью в современном мире неуклонно растет. Воспаление и фиброз как его исход способствуют образованию камней в почках.
Материал и методы. Исследование проведено в два этапа. На первом этапе с целью выявления предпосылок к литогенезу сравнивалась концентрация общего кальция и фосфора в сыворотке крови у 12 пациентов с хроническим неспецифическим пиелонефритом и 17 пациентов с урогенитальным туберкулезом. На втором этапе изучалась эффективность Блемарена в комплексном лечении больных хроническим пиелонефритом и уратурией, для чего было сформировано две группы по 19 человек в каждой. В основной группе дополнительно к стандартной терапии назначался Блемарен.
Результаты. Длительный инфекционно-воспалительный процесс в почках независимо от этиологии приводит к повышению экскреции оксалатов, причем наиболее выраженно при хроническом неспецифическом пиелонефрите (р < 0,05). Экскреция мочевой кислоты, не имевшая достоверных отличий исходно в обеих группах (4,97 и 5,19 ммоль/сут), статистически значимо увеличилась у больных урогенитальным туберкулезом через три месяца приема противотуберкулезных препаратов.
Выводы. Следствием хронического инфекционно-воспалительного процесса в почках становятся нарушение минерального обмена, увеличение экскреции уратов и оксалатов. Обнаружение в моче больного хроническим пиелонефритом этих солей является показанием к назначению курса Блемарена до стойкой нормализации рН мочи и растворения солей. Включение в комплекс лечения цитратной смеси не только способствует ожидаемому исчезновению уратурии, но и снижает выраженность болевого синдрома.
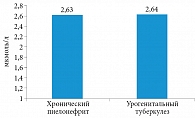
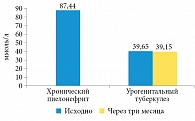
Рис. 1. Концентрация общего кальция в сыворотке крови у больных хроническим неспецифическим пиелонефритом и урогенитальным туберкулезом
Рис. 2. Концентрация альбумина в сыворотке крови у больных хроническим неспецифическим пиелонефритом и урогенитальным туберкулезом
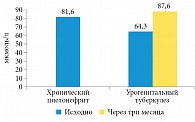
Рис. 3. Суточная экскреция оксалатов у больных хроническим неспецифическим пиелонефритом и урогенитальным туберкулезом

Рис. 4. Суточная экскреция мочевой кислоты у больных хроническим неспецифическим пиелонефритом и урогенитальным туберкулезом

Рис. 3. Суточная экскреция фосфатов у больных хроническим неспецифическим пиелонефритом и урогенитальным туберкулезом

Характеристика пациентов с хроническим пиелонефритом в стадии обострения и уратурией, принявших участие в исследовании (n = 38)
Введение
Распространенность мочекаменной болезни (МКБ) в современном мире неуклонно растет, что в значительной мере обусловлено кардинальными изменениями питания и поведения человека [1]. МКБ причиняет значительные моральные страдания, а также положительно коррелирует с заболеваниями сердечно-сосудистой системы, в частности ишемической болезнью сердца [2]. Кроме того, МКБ, в том числе в анамнезе, существенно повышает риск развития инфаркта миокарда и инсульта, что показано в канадском когортном исследовании, охватившем более трех миллионов пациентов [3].
Воспаление и фиброз как его исход способствуют образованию камней в почках [4, 5]. Различные нарушения метаболизма выявлены у 91,5% больных нефролитиазом. Среди них преобладала гиперурикемия (21,1%), у каждого десятого были обнаружены гипоцитратемия и низкая кислотность мочи [6]. Некоторые исследователи рассматривают камни почек как ренальное отражение классического метаболического синдрома [7].
Материал и методы
Исследование проведено в два этапа. На первом этапе с целью выявления предпосылок к литогенезу у пациентов с хроническим инфекционно-воспалительным процессом в почках различной этиологии (12 больных хроническим неспецифическим пиелонефритом и 17 больных урогенитальным туберкулезом) оценивалась концентрация общего кальция и фосфора в сыворотке крови. На втором этапе с целью определения эффективности Блемарена в комплексном лечении больных хроническим пиелонефритом сформировано две группы по 19 пациентов в каждой. У всех больных наряду с хроническим пиелонефритом также имела место уратурия в общем анализе мочи. В основной группе дополнительно к стандартной терапии по поводу обострения хронического пиелонефрита пациенты принимали Блемарен в виде шипучих таблеток, растворенных в 200 мл воды комнатной температуры, под контролем рН мочи в течение месяца. Группу сравнения набирали путем ретроспективного анализа историй болезни. В этой группе проводилось стандартное лечение, включающее антибиотик в соответствии с чувствительностью выделенного возбудителя.
Критерии включения:
- пациенты обоего пола старше 18 лет;
- диагноз «обострение хронического пиелонефрита»;
- как минимум два рецидива за последние полгода или три в течение года, предшествовавшего включению в исследование;
- наличие в моче уратов.
Эффективность лечения определяли по следующим критериям: срок нормализации или улучшения анализов мочи, уменьшение интенсивности боли по Визуальной аналоговой шкале, прекращение роста уропатогенов. Эффективность лечения оценивали через десять и 30 дней от начала терапии.
Статистическая обработка результатов проведена на персональном компьютере с помощью пакетов статистических программ Microsoft Excel 2007 и istica for Windows 6.0. Значимость различий (p) оценивали, используя t-критерий Стьюдента и критерий Манна – Уитни. Частоты признаков сравнивали с помощью критерия хи-квадрат Пирсона. Статистически значимыми считали различия при р
Результаты
Первый этап
Средняя концентрация общего кальция в сыворотке крови у больных хроническим неспецифическим пиелонефритом и нелеченых больных урогенитальным туберкулезом достоверных различий не имела (рис. 1). Однако у больных урогенитальным туберкулезом в сравнении с больными хроническим пиелонефритом наблюдалась тенденция к гипоальбуминемии, что косвенным образом свидетельствовало о повышении уровня ионизированного кальция в сыворотке крови (рис. 2).
При сравнении суточной экскреции ряда камнеобразующих элементов (оксалатов, мочевой кислоты и фосфатов) у больных урогенитальным туберкулезом и хроническим неспецифическим пиелонефритом выяснилось, что длительный инфекционно-воспалительный процесс в почках независимо от этиологии приводит к повышению экскреции оксалатов, причем наиболее выраженно при хроническом неспецифическом пиелонефрите (р
Оказалось, что более высокий уровень экскреции фосфатов характерен для больных хроническим пиелонефритом. У больных урогенитальным туберкулезом уровень экскреции фосфатов был в два раза ниже, чем у больных хроническим пиелонефритом, и прием противотуберкулезных препаратов не повлиял на этот параметр (рис. 5). Вместе с тем ни в одной группе не зафиксированы уреазопродуцирующая флора в моче и рН мочи > 7,0.
Таким образом, у больных туберкулезом мочевой системы выявлено увеличение суточной экскреции оксалатов и мочевой кислоты в процессе терапии. Оксалурия может быть связана с длительным приемом антибактериальных препаратов. Гиперурикозурия не только способствует формированию солей мочевой кислоты, но и повышает сатурацию мочи, благоприятствуя образованию кальциево-оксалатных конкрементов. Изменение суточной экскреции камнеобразующих элементов у больных туберкулезом может быть фактором риска формирования конкрементов в мочевой системе. Остается актуальным поиск эффективной профилактики камнеобразования.
Второй этап
Группы пациентов, включенных в исследование, по основным показателям были сопоставимы (таблица).
При оценке эффективности непосредственных результатов лечения сразу по завершении основного курса антибактериальной терапии статистически значимых различий по снижению бактериурии и лейкоцитурии в обеих группах не обнаружено. У 12 (63,1%) пациентов основной группы и 11 (57,9%) больных группы сравнения полностью нормализовались или значительно улучшились показатели мочи (уменьшились признаки воспаления). Рост патогенных микроорганизмов в моче прекратился у 16 (84,2%) пациентов основной и 16 (84,2%) пациентов контрольной группы. Однако интенсивность боли статистически значимо снизилась только в основной группе, где пациенты оценили ее в среднем в 3,4 ± 0,8 балла, в то время как в группе сравнения этот показатель составил 5,4 ± 0,5 балла (p
Уратурия прекратилась у 13 (68,4%) больных основной группы и двоих (10,5%) пациентов группы сравнения. Оксалурия исчезла у всех пациентов основной группы и по-прежнему наблюдалась у трех (15,8%) пациентов группы сравнения.
При контрольном обследовании через месяц установлено, что в основной группе умеренная лейкоцитурия сохранялась у двух (10,5%) пациентов, а у 17 (89,5%) признаки воспаления в моче исчезли. В группе сравнения нормальное число лейкоцитов в моче отмечено у 16 (84,2%) пациентов, а у трех (15,8%) по-прежнему выявлялась лейкоцитурия. Рост уропатогенов в диагностически значимом титре имел место у трех пациентов в каждой группе. Оксалурия не обнаружена ни у одного пациента основной группы, однако оксалаты по-прежнему визуализировались в моче одного пациента группы сравнения. Соли мочевой кислоты в моче отсутствовали у всех пациентов основной группы, в то время как в группе сравнения уратурия сохранялась у 15 (78,9%) пациентов.
Обсуждение результатов
Мочекислые камни занимают небольшую долю в структуре уролитиаза – не более 15-20% [8]. Они могут образовываться как из эндогенных источников de novo за счет синтеза и катаболизма нуклеиновых кислот, так и экзогенным путем из-за особенностей диеты. В частности избыточное поступление с пищей животных белков (не только мяса, но и рыбы) способствует формированию уратных конкрементов [9, 10].
Уратный литиаз потенциально может быть излечен консервативно, без инвазивных вмешательств. К факторам риска образования уратов относятся гиперурикемия, гиперурикозурия, олигурия, низкий рН мочи. Гиперурикемия является показанием к назначению ингибитора ксантиноксидазы аллопуринола. Этот фермент катализирует превращение гипоксантина в ксантин и далее в мочевую кислоту – конечный продукт пуринового обмена [8].
Уратные камни успешно поддаются литолизу и in vitro, и in vivo на фоне приема Блемарена, представляющего собой смесь сухой лимонной кислоты, гидрокарбоната калия и цитрата натрия [11, 12]. Многие исследователи подчеркивают, что комбинированное применение цитрата натрия и ингибиторов ксантиноксидазы эффективнее при уратном уролитиазе [13]. А у больных тубулоинтерстициальным нефритом в сочетании с уратным уролитиазом подобная комбинация не только приводила к хемолизу камней, но и улучшала почечную функцию [13]. Предположительно зафиксированный более выраженный эффект ослабления интенсивности боли у больных хроническим неспецифическим пиелонефритом на фоне приема Блемарена объясняется минимизацией повреждающего действия солей на паренхиму почек.
Обнаружено, что при кальций-оксалатной форме МКБ гиперурикемия способствует появлению кристаллов оксалата кальция в моче [14]. Установлена целесообразность назначения Блемарена перед дистанционной ударно-волновой литотрипсией, поскольку прием этого препарата приводит к уменьшению размеров конкрементов и снижению их плотности. В результате у 86,7% больных уратным уролитиазом, получавших в предоперационном периоде курс Блемарена, дезинтеграция камня почки была проведена за один сеанс, а в контрольной группе, где операцию выполняли без предшествующего уролитолиза, этот показатель был существенно ниже – 65,5% [15]. Подтверждена высокая эффективность Блемарена, особенно в сочетании с аллопуринолом, в метафилактике мочекислых камней почек [16].
Гипоцитратемия сегодня рассматривается как ведущий пункт нарушения обмена веществ у больных кальций-оксалатными камнями и встречается у 60% таких больных [1]. Мочекислые камни формируются в кислой среде, поэтому необходимо употреблять в пищу фрукты и овощи, избегая, однако, избытка шпината, грибов, аспарагуса, зеленого горошка [17]. Сладкая кукуруза тоже должна быть исключена, поскольку способствует гиперурикемии [1]. Сок дыни, апельсина, лимона, лайма повышает уровень цитратов в крови и снижает риск образования камней [1]. Употребление в пищу свежих фруктовых соков предотвращает образование камней не только благодаря увеличению объема мочи, но и за счет высокого содержания в них калия и лимонной кислоты. Цитраты профилактируют образование мочевых камней двумя путями. Во-первых, они связывают кальций, что снижает сатурацию мочи. Во-вторых, связывают кристаллы оксалата кальция и тем самым способствуют прекращению их роста [18]. Ведущий фактор патогенеза мочекислых камней – низкий рН мочи. Поэтому цитрат калия, нормализующий кислотность мочи, – основополагающий компонент в лечении больных мочекислым уролитиазом [17].
Проспективные рандомизированные контролируемые исследования показали, что прием калия цитрата уменьшает вероятность формирования кальций-оксалатных камней [19]. При этом был отмечен пролонгированный эффект от цитратной смеси, сохранявшийся до трех лет [20].
Накоплен значительный опыт применения Блемарена у больных уратным уролитиазом. В исследовании С.Н. Калининой и соавт. у 58,3% больных с камнями мочеточников достигнут полный литолиз на фоне цитратной терапии Блемареном [21]. Аналогичные результаты получены П.В. Глыбочко и соавт.: двухмесячный курс цитратной терапии завершился полным растворением уратных камней мочеточников у 72% пациентов [22].
В Российской Федерации, особенно в Сибири и на Дальнем Востоке, наблюдается неблагополучная эпидемическая ситуация по туберкулезу [23]. Туберкулезный очаг воспаления может заживать посредством имбибирования солями кальция, во фтизиатрии существует понятие «туберкулезные очаги в фазе обызвествления». Подобный очаг обызвествления в почке ошибочно может быть диагностирован как МКБ. Выполнение литотрипсии в этом случае чревато фатальными последствиями. Если урогенитальный туберкулез сочетается с хроническим пиелонефритом и МКБ, что бывает нередко, то отсутствие эффекта от стандартной антибактериальной терапии объясняют резистентностью уропатогенов [24].
В стандартную полихимиотерапию туберкулеза входит пиразинамид, который может вызывать такой побочный эффект, как повышение уровня мочевой кислоты в плазме крови. В проводимом исследовании у больных урогенитальным туберкулезом через три месяца приема противотуберкулезных препаратов статистически значимо выросла экскреция мочевой кислоты. Выявленная закономерность служит основанием для введения в комплекс лечения больных туберкулезом цитратных смесей, например Блемарена. Исследование показало, что длительный инфекционно-воспалительный процесс в почках независимо от этиологии приводит к повышению экскреции оксалатов, причем при хроническом неспецифическом пиелонефрите выраженнее, чем при урогенитальном туберкулезе. Не вызывает сомнения, что МКБ может осложниться вторичным пиелонефритом, резистентным к стандартной терапии за счет формирования биопленок на поверхности конкремента. Однако этот процесс обоюдно-направленный – хронический пиелонефрит любой этиологии также способствует формированию кристаллов солей, что усугубляет воспалительный процесс и усиливает интенсивность боли. Установленный факт позволяет рекомендовать литолитическую терапию пациентам с пиелонефритом.
Выводы
Хронический инфекционно-воспалительный процесс в почках приводит к нарушению минерального обмена, увеличивает экскрецию уратов и оксалатов. Обнаружение в моче больного хроническим пиелонефритом этих солей является показанием к назначению курса Блемарена до стойкой нормализации рН мочи и растворения солей. Включение в комплекс лечения цитратной смеси не только способствует ожидаемому исчезновению уратурии, но и снижает выраженность болевого синдрома.
Источник
Патогенез хронического пиелонефрита
Механизм развития хронического пиелонефрита связан с проникновением возбудителей в почечно-лоханочную систему и интерстициальную ткань. В результате этого развивается первичная атака в виде острого пиелонефрита.
Неадекватная антибиотикотерапия, несоблюдение пациентом всех врачебных рекомендаций приводят к тому, что часть бактерий переходит в неактивную форму, но остаётся в почках. В дальнейшем любой провоцирующий фактор приводит к их активизации и повторному воспалению.
Частое воспаление в почках становится причиной изменения структуры почечной ткани – отмирают канальцы и нефроны, они замещаются нефункциональной соединительной тканью.
Массивное воспаление и частые рецидивы приближают развитие почечной недостаточности.
Классификация и стадии развития хронического пиелонефрита
Ключевой критерий классификации хронического пиелонефрита – первичность поражения почек. На основании этого признака выделяют:
- Первичный хронический пиелонефрит – формируется в интактной, то есть не затронутой иным патологическим процессом, почке.
- Вторичный хронический пиелонефрит – развивается на фоне патологических состояний, которые нарушают уродинамику.
По распространённости пиелонефрит бывает одно- и двусторонним, а также тотальным (захватывает всю почку) и сегментарным – поражена лишь часть почки.
По преобладанию того или иного симптома различают гипертоническую, азотемическую и анемическую разновидности пиелонефрита.
В зависимости от выраженности воспаления хронический пиелонефрит имеет три фазы:
- Активное воспаление – характеризуется максимальными воспалительными изменениями в ткани почек и связанными с этим симптомами.
- Латентное воспаление – проявляется минимальными симптомами.
- Ремиссия или клиническое выздоровление – проявляется отсутствием какой-либо симптоматики и нормальными показателями лабораторных исследований.
Гистологическое исследование почек пациентов позволило определить стадии хронического пиелонефрита.
На I стадии (a) в почках отмечается выраженная инфильтрация интерстиция почки лейкоцитами, а также незначительные атрофические процессы, затрагивающие собирательные канальцы.
II стадия (b) характеризуется гиалинизацией (химическими изменениями) части клубочков, начинающимся разрастанием соединительной ткани.
На III стадии (c) гиалинизирована львиная доля клубочков, склерозирована значительная часть почечной ткани, а также многие мелкие кровеносные сосуды.
На IV стадии (d) отмечаются выраженные рубцово-склеротические изменения интерстиция, что проявляется сморщиванием почки – её поверхность приобретает мелкобугристый характер.
Осложнения хронического пиелонефрита
Прогрессирование хронического пиелонефрита сопровождается нефросклерозом, то есть происходит замещение нормальной почечной ткани соединительной, которая не способна выполнять фильтрационную функцию. Рано или поздно этот процесс приводит к формированию хронической почечной недостаточности.
В периоды обострения высок риск развития гнойно-септических осложнений:
- паранефрит;
- урогенный сепсис;
- инфекционно-токсический шок;
- перитонит (при распространении инфекции на брюшную полость).
Перечисленные осложнения значительно ухудшают прогноз для пациентов, страдающих хроническим пиелонефритом. Тяжёлые формы осложнений нередко приводят к летальному исходу.[2][6][7]
Хронический пиелонефрит является одной из причин нефрогенной артериальной гипертензии: при одностороннем поражении она развивается у 35-36% пациентов, при двустороннем – у 43%.[6]
Диагностика хронического пиелонефрита
Постановка диагноза начинается со сбора анамнеза пациента и проведения физикального обследования. Заподозрить хронический пиелонефрит помогают типичные жалобы, перечисленные выше.[1][3][4] При физикальном обследовании определяются следующие признаки:
- болезненность при пальпации в поясничной области;
- положительный симптом поколачивания;
- положительный симптом Пастернацкого;
- полиурия.
Подтвердить диагноз помогают лабораторные и инструментальные методы диагностики.
Лабораторная диагностика
Стандартный алгоритм обследования пациентов с хроническим пиелонефритом включает:
- общий анализ мочи;
- бактериологическое и бактериоскопическое исследование мочи;
- общий анализ крови;
- биохимию крови.
В моче определяется лейкоцитурия (преимущественно за счёт нейтрофилов), протеинурия, цилиндрурия, микрогематурия. Выраженность патологических изменений варьируется в зависимости от активности воспаления:
- в стадии активного воспаления количество лейкоцитов может достигать нескольких десятков в поле зрения;
- в стадии латентного – ограничивается 5-10 лейкоцитами или вообще отсутствует.
Клинически значимым минимальным уровнем лейкоцитурии считают показатель в 104 КОЕ/мл.
Для определения скрытой лейкоцитурии применяют пирогеналовый или преднизолоновый тесты – исследуют мочу через некоторое время после введения соответствующих препаратов.[1][4]
Бактериологическое исследование мочи имеет важное значение для диагностики конкретного возбудителя и исследования его чувствительности к антибиотикам. Это помогает выбрать рациональный режим антибиотикотерапии.
В общем анализе крови при хроническом пиелонефрите отмечаются изменения, характерные для системного воспаления: лейкоцитоз со сдвигом лейкоформулы влево, увеличение СОЭ.
Изменения биохимических параметров крови на ранней стадии заболевания могут отсутствовать, в других случаях определяется повышение уровня мочевины и креатинина.
С целью оценки функционального состояния почек проводятся пробы Реберга и Зимницкого.
Инструментальные методы диагностики
В обязательном порядке выполняется УЗИ почек и всей мочевыводящей системы. Ультразвуковое исследование позволяет выявить отёк почечной паренхимы в период обострения, а также деформацию и сморщивание почек при хроническом течении. Расширение чашечно-лоханочной системы свидетельствует о нарушении оттока мочи, что является одним из важнейших провоцирующих факторов пиелонефрита.
Допплерография почечных сосудов позволяет уточнить степень угнетения кровотока в почках.[2][8]
Высокотехнологичные методы диагностики, такие как КТ или МРТ, назначаются для выявления заболеваний, способствующих возникновению хронического пиелонефрита:
- аномалий развития почек;
- мочекаменной болезни;
- опухолей.
Хромоцистоскопия, урография и некоторые другие исследования чаще всего выполняются в ходе дифференциальной диагностики. Биопсия, как самостоятельное исследование, при описываемой патологии значения не имеет. Она проводится лишь для решения вопроса о назначении иммуносупрессивной терапии при других диффузных поражениях почечной ткани.
Лечение хронического пиелонефрита
Лечебные мероприятия при хроническом пиелонефрите включают как медикаментозные средства, так и немедикаментозные способы терапии. Объём и тактика лечения определяются национальным стандартом, разработанным Российским обществом урологов и утверждённым Минздравом.
Немедикаментозная терапия
Пациентам с хроническим пиелонефритом рекомендуется потреблять достаточное количество жидкости, чтобы поддерживать диурез (объём мочи) на адекватном уровне. В день следует выпивать не менее двух литров жидкости. Предпочтение отдаётся витаминизированным ягодно-травяным отварам с мочегонным эффектом (брусничный, клюквенный морс или чай). Исключение – больные с артериальной гипертонией, так как у этой категории пациентов количество жидкости следует ограничивать до одного литра в сутки.
Необходимо избегать воздействия любых провоцирующих факторов, в период обострения предписан охранительный режим.[1][3]
Медикаментозная терапия
Эпизоды обострения хронического пиелонефрита в обязательном порядке требуют назначения антибиотиков. Для повышения эффективности антибиотикотерапии требуется выделение культуры возбудителя с определением чувствительности к разным группам препаратов. Учитывая высокий риск наличия нефросклероза и почечной недостаточности, дозу антибактериального препарата рассчитывают, опираясь на показатели пробы Реберга.[5][8][9]
При неосложнённом пиелонефрите лёгкой и средней тяжести чаще всего используется монотерапия одним препаратом. Антибиотик принимают перорально курсом 10-14 дней. В качестве средств эмпирической антибиотикотерапии (до определения возбудителя и исследования его чувствительности) применяют фторхинолоны («Ципрофлоксацин», «Левофлоксацин») или цефалоспорины III поколения («Цефиксим» и аналоги).[5][8][9]
При тяжёлом течении рецидива хронического пиелонефрита антибиотики назначаются парентерально – в виде внутримышечных или внутривенных инъекций. При точно установленном возбудителе возможно назначение защищённых бета-лактамов («Амоксиклав»), аминогликозидов или карбапенемов.
Хирургическое лечение хронического пиелонефрита
Операции при пиелонефрите проводятся в случае наличия абсолютных показаний, к которым относятся:
- камни в почках или в мочеточниках, препятствующие нормальному пассажу мочи – проводят литоэкстракцию (литотрипсию) или накладывают нефростому;
- выраженный односторонний пиелонефрит, при котором пострадавшая почка не функционирует, являясь лишь источником инфекции. В этом случае проводят нефрэктомию – удаление почки;
- гнойные осложнения – абсцесс почки, апостематозный нефрит и другие.
В состав комплексной терапии пиелонефрита включают метаболические средства, витамины и антигистаминные препараты. Обязательно проводится симптоматическое лечение: при гипертонии назначают гипотензивные средства, при анемии – железосодержащие средства и фолиевую кислоту.[3][6]
В период стойкой ремиссии допускается использование физиотерапевтических методов лечения: электрофореза, СМТ-терапии, гальванотерапии.
Прогноз. Профилактика
Латентное течение пиелонефрита никак не препятствует повседневной деятельности – пациенты долгое время сохраняют трудоспособность.
Частые рецидивы становятся причиной временной нетрудоспособности, а в тяжёлых случаях развивается инвалидизация из-за хронической почечной недостаточности. Сроки её развития весьма вариабельны и во многом зависят от своевременности и качества проводимого лечения, а также приверженности пациента. Однако даже терминальная стадия хронической почечной недостаточности в настоящее время не является абсолютным приговором для больных хроническим пиелонефритом. В случае её развития решается вопрос о переводе человека на программируемый аппаратный гемодиализ.[2][3]
Предупреждение развития хронического пиелонефрита заключается в активной и, главное, своевременной терапии острых инфекций мочеполового тракта. Также должны быть выявлены и ликвидированы другие возможные очаги хронического инфицирования:
- инфекция ЛОР-органов;
- вылечены кариозные зубы;
- проведена санация ротовой полости;
- женщины обследуются на предмет хронических инфекций половой системы (сальпингита и др.);
- мужчин обследуют на простатит.
С точки зрения профилактики очень важно избегать воздействия провоцирующих факторов: переохлаждения, половых инфекций.
Пациентам с сопутствующими хроническими заболеваниями следует уделить внимание их лечению. Особое внимание должно быть уделено нарушениям углеводного обмена – обязательно проводится полная коррекция сахарного диабета.[3]
Список литературы
- Тареева И.Е. Нефрология: руководство для врачей. – М.: Медицина, 2000.
- Шулутко Б.И. Нефрология 2002. Современное состояние проблемы. – СПб.: Ренкор, 2002.
- Урология. Национальное руководство / под ред. Н.А. Лопаткина. – М.: ГЭОТАР-Медиа, 2009. – 1024 с.
- Аль-Шукри С.Х., Ткачук. Урология : учебник. – 2011. – 480 с.
- Лопаткин Н.А., Аполихин О.И., Пушкарь Д.Ю. и др. Антимикробная терапия и профилактика инфекций почек, мочевыводящих путей и мужских половых органов / Российские национальные рекомендации. – М., 2014.
- Франц М., Хорл У. Наиболее частые ошибки диагностики и ведения инфекции мочевых путей (ИМП) // Нефрология и диализ. – 2000. – Т. 2, № 4.
- Klahr S. Obstructive nephropathy // Kidney Int. – 1998. – Vol. 54. – P. 286-300.
- Naber K.G., Bergman B., Bishop M.C. et al. Guidelines on Urinary and Male Genital Tract Infections. – London, 2000. – P. 71.
- Scholar E.M., Pratt W.B. The Antimicrobial Drugs. – Oxford, 2000.
Источник
