Нервы поясница мочевой пузырь
Статья посвящена проблеме нейрогенных расстройств мочеиспускания при травме позвоночника и спинного мозга
Путь пациента с осложненной травмой позвоночника, т. е. сопровождающейся повреждением спинного мозга, начинается с нейрохирургического оперативного вмешательства и продолжается многоэтапной реабилитацией, направленной на коррекцию сопутствующих осложнений и восстановление утраченных функций организма [1]. Для таких больных есть специфический термин – «спинальные».
Одним из тяжелейших последствий травмы спинного мозга является расстройство произвольного мочеиспускания, обусловленное нарушением проводимости спинномозговых путей. По данным М.Р. Касаткина, подобное осложнение встречается в 92,1% случаев закрытых повреждений спинного мозга [2]. Патогенез изменений функции нижних мочевых путей при травме спинного мозга, проявляющийся в утрате рефлекторной деятельности, сложен и многообразен [3].
Механизм нормального мочеиспускания и характер его расстройства у спинальных пациентов напрямую связаны с особенностями физиологии этой области. Периферическую иннервацию нижних мочевых путей осуществляют тазовый нерв, представляющий парасимпатическую нервную систему, гипогастральный нерв, реализующий симпатическую регуляцию, и пудендальный соматический нерв. Афферентную информацию несут волокна всех трех нервов – вегетативных от детрузора (гладкой мышцы мочевого пузыря) и уретры и полового нерва от тканей промежности. Первичным анализатором для парасимпатического тазового нерва являются нейроны сакрального центра мочеиспускания, расположенного на уровне S2‒S4 сегментов спинного мозга. Здесь же, в анатомическом соседстве, находится ядро Онуфа, представляющее собой скопление нервных клеток, аксоны которых образуют пудендальный нерв [4]. Симпатическая афферентная иннервация, опосредованная гипогастральным нервом, являющимся частью подчревного и поясничного сплетения, осуществляется через пограничный симпатический ствол и вставочные интернейроны боковых рогов спинного мозга на уровне его Th10‒L2 сегментов. Эти же нервы несут и эфферентные сигналы к иннервируемым органам. Регулирующие структуры спинного мозга связаны с вышерасположенными центрами иннервации проекционно, а также с помощью нейрогуморальных и рефлекторных механизмов [5]. Однако следует отметить, что концепции регуляции функции нижних мочевых путей в норме и патологии являются в большей степени эмпирическими, и единого понимания этого вопроса на сегодняшний день нет.
Клиническая картина
Врачу-неврологу, курирующему пациента с осложненной травмой позвоночника, необходимо оценить уровень и степень повреждения спинного мозга и учесть посттравматические сроки. Клиническая картина в острый и ранний периоды после получения травмы обусловлена спинальным шоком, что проявляется арефлексией и задержкой мочи. По мере восстановления можно наблюдать активизацию рефлекторной деятельности и формирование «в сухом остатке» нейрогенного расстройства мочеиспускания. При повреждении спинного мозга на уровне сакрального центра мочеиспускания и периферических нервных волокон развивается атония или гипотония детрузора, при этом за счет интактности симпатических структур иннервации внутренний уретральный сфинктер сохраняет сократительную способность. Таким образом, нарушается взаимосвязь симпатических и парасимпатических влияний [6]. Клинически наблюдается нейрогенная задержка мочеиспускания с элементами парадоксальной ишурии (выделения мочи по каплям на фоне переполненного мочевого пузыря). При локализации травмы выше сакрального центра и ядра Онуфа повреждаются проводниковые нервные волокна, осуществляющие взаимосвязь регулирующих структур, однако сами центры иннервации могут быть интактны. В этом случае и детрузор, и внутренний сфинктер уретры способны к циклическому сокращению и расслаблению, но рассогласованность в работе приводит не к нормальному акту мочеиспускания, а к детрузорно-сфинктерной диссинергии. Поражение на уровне нижнегрудного и верхнепоясничного отделов позвоночника, вовлекающее симпатические регулирующие структуры, вызывает нарушение сократительной способности внутреннего сфинктера уретры и недержание мочи. Травма спинного мозга на уровне шейного и верхнегрудного отделов позвоночника ведет к прерыванию взаимосвязи спинальных и стволовых, а также кортикальных структур регуляции. В ситуации, когда центры иннервации спинного мозга и нервные проводники между ними сохраняют свою анатомическую целостность, клинически может сформироваться автономный процесс мочеиспускания, а также гиперактивность мочевого пузыря. В этом случае накопление и выделение мочи происходят рефлекторно, в т. ч. с участием аксон-рефлексов, без контроля центров, отвечающих за произвольную составляющую физиологического процесса [7].
Описанные клинические нарушения достаточно вариабельны и зависят от характера и тяжести повреждения, а также сроков, прошедших с момента травмы, поэтому можно наблюдать переход одной формы нейрогенного расстройства мочеиспускания в другую.
Невролог, понимая обусловленность клинической картины уровнем поражения спинного мозга, определяет тактику ведения спинального пациента и дальнейший прогноз. Осуществление адекватной коррекции урологических осложнений лежит, несомненно, в междисциплинарной плоскости. В связи с этим нейроурологическая практика, а вернее, четкое и скоординированное взаимодействие невролога и уролога способно обеспечить квалифицированную и своевременную помощь. И если врач-невролог сосредоточен на повреждении спинного мозга и нарушении иннервации, то уролог контролирует непосредственное функциональное состояние нижних мочевых путей и коррекцию сопутствующих воспалительных и нефротических осложнений. Отсюда вытекает необходимость тесной взаимосвязи специалистов для полноценной коррекции нейрогенных расстройств мочеиспускания.
В представлении уролога, оказывающего специализированную помощь пациентам с неврологическими расстройствами, процесс мочеиспускания выглядит несколько сложнее, чем простой циклический акт, состоящий из чередования фаз накопления и выведения мочи, обеспеченный двумя основными функциями мочевого пузыря: резервуарной и эвакуаторной. Функционально этот процесс определяется синергией детрузора с гладкомышечным сфинктером уретры и мышцами тазового дна, включающими наружный уретральный сфинктер.
Физиологически мочевой пузырь, природой созданный резервуар для сбора мочи, обладает способностью к полному опорожнению в подходящее время и в удобном для совершения акта мочеиспускания месте согласно социально-поведенческим нормам. Эта крайне важная способность реализуется в результате сложной регуляции с участием центральной и периферической нервных систем. Фундаментально акт мочеиспускания – это спинальный рефлекс, обеспечиваемый работой центров головного мозга, реализация и подавление этого рефлекса находятся под волевым контролем. Возможность произвольного управления делает функцию нижних мочевых путей уникальной по сравнению, например, с сердечно-сосудистой системой, и в то же время более уязвимой при неврологических заболеваниях [8]. Таким образом, основными функциями нижних мочевых путей являются накопление мочи в мочевом пузыре, длящееся относительно продолжительное время, и мочеиспускание, занимающее в норме несколько секунд. Реципрокные отношения – расслабление/напряжение детрузора, закрытие уретрального сфинктера и сокращение/расслабление детрузора, открытие уретрального сфинктера – обеспечивают скоординированность процессов накопления и удаления мочи и находятся под нейромедиаторным контролем [9].
Нейрогенная дисфункция нижних мочевых путей является следствием патологии центральной нервной системы или периферических нервных окончаний ‒ отделов нервной системы, выполняющих контроль над актом мочеиспускания. В этом состоит главное отличие рассматриваемого нарушения от нарушений нижних мочевых путей ненейрогенной этиологии, развивающихся вследствие поражения непосредственно мочеполовой системы.
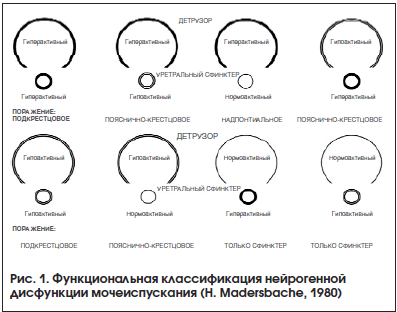
В урологическом сообществе длительное время основной опорой для определения формы нейрогенного расстройства мочеиспускания являлась классификация, предложенная профессором Г. Мадерсбахером в 1980 г. и рекомендуемая Европейской ассоциацией урологов (рис. 1) [10]. В ней автор выделяет 8 основных форм нейрогенных расстройств мочеиспускания в зависимости от состояния детрузора и внутреннего сфинктера уретры. Подразумевается, что указанные структуры могут быть в гипертонусе, гипотонусе и в нормальном состоянии. Однако сложность в постановке диагноза и категоричность в выборе одной из 8 форм нарушений мочеиспускания сегодня заставляют говорить о пересмотре форм расстройств мочеиспускания. С клинической точки зрения все возможные виды нарушений мочеиспускания рассмотреть в рамках одной из существующих классификаций невозможно. В определении поражения у пациента наиболее часто специалисты основываются на преобладающем нарушении эвакуаторной или резервуарной функции мочевого пузыря, различных видах детрузорно-сфинктерной диссинергии и уродинамических показателях максимального детрузорного давления в точке утечки. При этом важность знания о максимальном детрузорном давлении и максимальном давлении в точке утечки делает необходимым проведение специализированного уродинамического исследования практически каждому пациенту с нарушениями мочеиспускания на фоне неврологического заболевания.
Лечение
Основными задачами урологической помощи на всех этапах нейрореабилитации являются:
1) сохранение и обеспечение функции верхних мочевыводящих путей;
2) независимость регуляции функции нижних мочевыводящих путей;
3) улучшение качества жизни.
С практической точки зрения важны борьба с вторичными осложнениями нейрогенной дисфункции мочеиспускания, а также их профилактика. К таким осложнениям относятся манифестация инфекции мочевыводящих путей (исключая бессимптомную бактериурию), уролитиаз, микроцистис, гидронефротическая трансформация и почечная недостаточность, стриктура уретры и т. д. [11].
Наименьшего риска осложнений со стороны верхних мочевыводящих путей следует ожидать при сохранении резервуарной функции мочевого пузыря с низким внутрипузырным давлением, например при гипотонии детрузора, его достаточной функциональной емкости и нормальном состоянии поперечно-полосатого сфинктера уретры или его гипотонии. В этом случае к хорошим результатам коррекции, в т. ч. улучшению качества жизни спинального пациента, приводит адекватное дренирование нижних мочевых путей, при этом следует руководствоваться международными стандартами и отечественными клиническими рекомендациями. При нарушении функции опорожнения мочевого пузыря вследствие повреждения позвоночника и спинного мозга методом выбора является асептическая периодическая катетеризация. Она подразумевает использование одноразового стерильного лубрицированного катетера. Процедура выполняется самостоятельно или с посторонней помощью каждые 4‒6 ч [12].
Иные методы дренирования мочевого пузыря, такие как приемы Креде или Вальсальвы, длительное использование постоянного мочевого катетера, должны быть строго обоснованы, т. к. несут значительные риски развития вторичных нейрогенных осложнений работы мочевого пузыря, достигающих 34% [13].
Периодическая катетеризация 4‒6 раз в сутки при условии отсутствия выраженных нарушений со стороны верхних мочевыводящих путей, шокового состояния, гнойно-инфекционных процессов в уретре и мочевом пузыре может быть назначена любым специалистом, курирующим пациента. Вопрос о том, когда переводить пациента на периодическую катетеризацию для постоянного уретрального дренажа, находится в стадии обсуждения сообщества специалистов по нейроурологии [14]. Формальных ограничений и четких рекомендаций по срокам нет, однако считается, что при отсутствии противопоказаний и достаточной укомплектованности отделения средним и младшим медицинским персоналом следует избавлять пациента от постоянных дренажей как можно раньше.
Гиперактивный мочевой пузырь, встречающийся на фоне детрузорно-сфинктерной диссинергии и без нее, является другой формой нейрогенного расстройства мочеиспускания вследствие травмы позвоночника и спинного мозга. Если такой тип нарушения клинически проявляется недержанием мочи, то он не несет значительного риска осложнений со стороны верхних мочевыводящих путей. К проблемам нейрогенного гиперактивного мочевого пузыря следует отнести снижение качества жизни.
Детрузорно-сфинктерная диссинергия характеризуется тем, что в момент напряжения мочевого пузыря для его опорожнения происходят различные по силе и продолжительности сокращения внутреннего и наружного сфинктеров уретры, обеспечивающих функцию удержания. В норме сокращения детрузора синхронны с расслаблением этих сфинктеров, что способствует свободному выведению мочи по уретре. Нарушение функции опорожнения в сочетании с высоким внутрипузырным давлением ‒ наиболее опасная форма нейрогенной дисфункции мочеиспускания из-за развития пузырно-мочеточникового рефлюкса, а также возможности структурных повреждений самого мочевого пузыря. В этом случае перед урологом стоят две основные задачи: 1) подавление высокого внутрипузырного давления, 2) обеспечение оттока мочи по уретре.
Для подавления детрузорной гиперактивности в качестве первой линии терапии применяются антихолинергические средства, в дополнение к которым можно назначать препараты из группы бета-3-адреномиметиков [15]. Вторая линия лечения включает инъекционное введение в стенку мочевого пузыря 200 ЕД ботулинического нейропептида. Надо понимать, что терапия направлена на создание низкого внутрипузырного давления в мочевом пузыре, необходимого для нормальной работы верхних мочевых путей. Одним из результатов купирования гиперактивности, особенно при сохранении нормального или повышенного тонуса поперечно-полосатого сфинктера уретры, будет увеличение количества остаточной мочи или отсутствие мочевыделения. Поэтому крайне важно объяснить пациенту необходимость проведения указанной терапии с назначением периодической катетеризации мочевого пузыря.
При своевременной коррекции нарушений мочеиспускания у спинальных пациентов, применении рекомендованного метода отведения мочи, компенсации избыточного внутрипузырного давления вследствие гиперактивности детрузора или детрузорно-сфинктерной диссинергии удается избежать многих вторичных осложнений.
В комплексной программе реабилитационного лечения пациентов с травмой позвоночника и спинного мозга используются методики немедикаментозной коррекции, показавшие различный терапевтический потенциал в ходе исследований. В частности, применение электростимуляции мочевого пузыря с помощью имплантируемых электродов в работе А.В. Лившица и соавт. показало, что создать управляемый акт мочеиспускания невозможно, т. к. возбуждение детрузора распространяется на внутренний сфинктер уретры, моделируя детрузорно-сфинктерную диссинергию [16]. Несмотря на то что исследователи представили некоторые положительные результаты, методика не нашла клинического применения в связи с высокой инвазивностью и риском вторичных осложнений.
Применение электростимуляции переменным пульсирующим током по лонно-сакральной методике и электрофореза с прозерином на передней брюшной стенке в проекции мочевого пузыря в настоящий момент представляется несостоятельным вследствие особенностей физиологии нижних мочевых путей и неучастия мышц живота в акте мочеиспускания.
Перспективно использование современных методик: сакральной инвазивной электронейростимуляции с помощью имплантируемых электродов и ритмической периферической магнитной стимуляции в области сакрального центра мочеиспускания и крестцовых корешков [17, 18]. В настоящее время механизм действия магнитной стимуляции на физиологию нижних мочевых путей остается неясным. Многоступенчатость и сложность нервной регуляции процесса удержания мочи и акта мочеиспускания предполагают возможность вовлечения различных структур в ответ на внешнее воздействие. Клинические и уродинамические эффекты магнитной стимуляции, вероятно, связаны с восстановлением интеграции регуляторных рефлексов, при этом наблюдается эффект нейромодуляции, когда происходит изменение активности (торможение или возбуждение) структур центральной, периферической и вегетативной нервных систем [19, 20].
Нейрогенное нарушение мочеиспускания, обусловленное травмой позвоночника и спинного мозга, клинически чрезвычайно гетерогенно вследствие вариабельности уровня и степени тяжести поражения [21, 22]. Этот аспект диктует необходимость индивидуального диагностического подхода, выбора адекватного метода коррекции работы нижних мочевых путей. Реабилитационный путь спинального пациента в настоящее время невозможно представить без тесного сотрудничества невролога и уролога. Совместный современный подход специалистов к проблеме урологических осложнений травмы спинного мозга обеспечивает пациенту верное понимание собственного состояния и адекватную прогностическую оценку, а также возможность социальной адаптации и повышения качества жизни [23, 24].
Источник
Нейрогенный мочевой пузырь – это дисфункция мочевого пузыря, обусловленная врожденной или приобретенной патологией нервной системы. В зависимости от состояния детрузора дифференцируют гипер- и гипорефлекторный тип патологии. Заболевание может проявляться поллакиурией, недержанием мочи или ее патологической задержкой. Диагностика синдрома заключается в полном невролого-урологическом обследовании (анализы, урография, УЗИ почек и мочевого пузыря, урофлоурометрия, цистография и цистоскопия, сфинктерометрия, рентгенография и МРТ позвоночника, МРТ головного мозга и пр.). Лечение может включать немедикаментозную и лекарственную терапию, катетеризацию мочевого пузыря, оперативное вмешательство.
Общие сведения
Нейрогенный мочевой пузырь – достаточно распространенное состояние в клинической урологии, связанное с невозможностью осуществления произвольно-рефлекторного накопления и выделения мочи из-за органического и функционального поражения нервных центров и путей, регулирующих данный процесс. Расстройства мочеиспускания имеют социальный аспект, поскольку могут ограничивать физическую и психическую активность человека, создавать проблему его социальной адаптации в обществе.
Патология часто сопровождается миофасциальным синдромом, синдромом тазовой венозной конгестии (венозного застоя). Более чем в 30% случаев наблюдается развитие вторичных воспалительно-дистрофических изменений со стороны мочевыделительной системы: пузырно-мочеточникового рефлюкса, хронического цистита, пиелонефрита и уретерогидронефроза, приводящих к артериальной гипертензии, нефросклерозу и хронической почечной недостаточности, что может грозить ранней инвалидизацией.
Нейрогенный мочевой пузырь
Причины
Сбой, происходящий на любом этапе сложной многоуровневой регуляции процесса мочеиспускания, может привести к развитию одного из многочисленных клинических вариантов нейрогенного мочевого пузыря. У взрослых синдром связан с повреждением головного и спинного мозга (при инсульте, сдавлении, хирургическом вмешательстве, переломе позвоночника), а также с воспалительно-дегенеративными и опухолевыми заболеваниями нервной системы – энцефалитом, рассеянным энцефаломиелитом, полинейропатией, полирадикулоневритом, туберкуломой, холестеатомой и т. д.
Нейрогенный мочевой пузырь у детей может иметь место при врожденных дефектах развития ЦНС, позвоночника и мочевыделительных органов, после перенесенной родовой травмы. Недержание мочи может быть вызвано снижением растяжимости и емкости мочевого пузыря вследствие цистита или неврологических заболеваний.
Классификация
Выделяют гиперрефлекторный нейрогенный мочевой пузырь, проявляющийся в фазу накопления гиперактивностью детрузора (при надсегментарных поражениях нервной системы) и гипорефлекторный – со сниженной активностью детрузора в фазу выделения (при поражении сегментарно-периферического аппарата регуляции мочеиспускания). Синдром может иметь в основе рассинхронизацию деятельности детрузора и сфинктера мочевого пузыря (внутренняя и наружная детрузорно-сфинктерная диссинергия).
Симптомы
Синдром нейрогенного мочевого пузыря может иметь постоянные, периодические или эпизодические проявления, а многообразие его клинических вариантов определяется различием уровня, характера, степени тяжести и стадии поражения нервной системы. Типичными для гиперактивного варианта патологии являются поллакиурия, в т. ч. никтурия, императивные позывы и недержание мочи. Преобладание тонуса детрузора ведет к значительному повышению внутрипузырного давления при малом количестве мочи, что при слабости сфинктеров вызывает императивные позывы и учащенное мочеиспускание.
Гиперактивный тип синдрома характеризуется спастическим состоянием и опорожнением при накоплении менее 250 мл мочи; отсутствием или малым объемом остаточной мочи, затруднением произвольного начала и самого акта мочеиспускания; появлением вегетативных симптомов (потливости, подъема артериального давления, усиления спастики) перед микцией в отсутствии позывов; возможностью спровоцировать мочеиспускание раздражением области бедра и над лобком. При наличии ряда неврологических нарушений может возникать неконтролируемое стремительное выделение большого объема мочи – «церебральный незаторможенный мочевой пузырь».
Относительное преобладание тонуса сфинктеров при детрузорно-сфинктерной диссинергии выражается полной задержкой мочи, мочеиспусканием при натуживании, наличием остаточной мочи. Гипоактивный нейрогенный мочевой пузырь проявляется снижением или отсутствием сократительной активности и опорожнения при полном и даже переполненном пузыре в фазу выделения.
Из-за гипотонии детрузора нет повышения внутрипузырного давления, необходимого для преодоления сопротивления сфинктера, что ведет к полной задержке или вялому мочеиспусканию, натуживанию во время микции, наличию большого (до 400 мл) объема остаточной мочи и сохранению ощущения наполненности пузыря. При гипотоничном растянутом мочевом пузыре возможно недержание мочи (парадоксальная ишурия), когда при переполнении органа происходит механическое растяжение внутреннего сфинктера и неконтролируемое выделение мочи каплями или небольшими порциями наружу.
Осложнения
Денервация вызывает развитие выраженных трофических нарушений и осложнений в виде интерстициального цистита, приводящего к склерозированию и сморщиванию мочевого пузыря. В мочевыводящих путях могут формироваться камни, нарушающие отток мочи, провоцирующие развитие инфекции. В случае спазма сфинктера может возникать пузырно-мочеточниковый рефлюкс (обратный заброс мочи в мочеточники и почки, приводящий к воспалению). Синдром часто сопровождается функциональными невротическими расстройствами, которые в дальнейшем могут стать определяющими.
Диагностика
Для диагностики необходимо провести тщательный сбор анамнеза, лабораторное и инструментальное обследование. В опросе родителей ребенка с нейрогенным мочевым пузырем выясняют, как протекали роды, имеется ли наследственная предрасположенность к заболеванию. Для исключения воспалительных заболеваний мочевыделительной системы выполняют анализ крови и мочи – общий, по Нечипоренко, функциональную пробу Зимницкого, биохимическое исследование мочи и крови.
Основными методами инструментальной диагностики синдрома являются УЗИ почек и мочевого пузыря, цистоскопия, МРТ, рентгенологическое исследование мочевыводящих путей (обычная и микционная уретроцистография, экскреторная урография, восходящая пиелография, радиоизотопная ренография), уродинамические исследования (цистометрия, сфинктерометрия, профилометрия, урофлоуметрия).
При отсутствии заболеваний со стороны мочевыделительной системы проводят неврологическое обследование для выявления патологии головного и спинного мозга с применением электроэнцефалографии, КТ, МРТ, рентгенографии черепа и позвоночника. Осуществляется дифференциальная диагностика с гипертрофией простаты, стрессовым недержанием мочи у пожилых людей. При невозможности установить причину заболевания говорят о нейрогенном мочевом пузыре с неясной этиологией (идиопатическом).
Лечение нейрогенного мочевого пузыря
Терапия проводится совместно врачом-урологом и неврологом; ее план зависит от установленной причины, типа, степени выраженности дисфункции мочевого пузыря, сопутствующей патологии (осложнений), эффективности ранее проведенного лечения. Применяют немедикаментозное, медикаментозное и хирургическое лечение, начиная с менее травматичных и более безопасных лечебных мероприятий.
Гиперактивный вариант лучше поддается лечению. Используют лекарственные средства, снижающие тонус мышц мочевого пузыря, активизирующие органное кровообращение и устраняющие гипоксию: антихолинергические препараты (гиосцин, пропантелин, оксибутинин), трициклические антидепрессанты (имипрамин), антагонисты кальция (нифедипин), альфа-адреноблокаторы (фентоламин, феноксибензамин).
В последнее время довольно перспективным в лечении гиперрефлексии, детрузорно-сфинктерной диссенергии и инфравезикальной обструкции считают применение инъекций ботулотоксина в стенку мочевого пузыря или уретры, внутрипузырное введение капсаицина и резинфератоксина. В дополнение назначают препараты на основе янтарной кислоты, L-карнитин, гопантеновая кислота, N-никотиноил-гамма-аминобутировая кислота, коферментные формы витаминов, обладающие антигипоксическим и антиоксидантным действием.
Параллельно применяют немедикаментозные методы лечения нейрогенного мочевого пузыря: лечебную физкультуру (специальные упражнения для тазовых мышц), физиотерапию (электростимуляцию, лазеротерапию, гипербарическую оксигенацию, диадинамотерапию, тепловые аппликации, ультразвук), тренировку мочевого пузыря, нормализацию режима питья и сна, психотерапию.
Гипоактивный вариант болезни труднее поддается терапии. Имеющиеся застойные явления в мочевом пузыре создают риск присоединения инфекции, развития вторичных поражений мочевой системы. В лечении нейрогенного синдрома с признаками гипотонии важно обеспечение регулярного и полного опорожнения мочевого пузыря (с помощью принудительных мочеиспусканий, наружной компрессии (прием Креде), методами физиотерапии, тренировки мышц мочевого пузыря и тазового дна, периодической или постоянной катетеризацией).
В качестве медикаментозной терапии применяют непрямые и М-холиномиметики (бетанехол хлорид, дистигмина бромид, ацеклидин, галантамин), позволяющие усиливать моторику мочевого пузыря, снижать его эффективный объем и количество остаточной мочи. Индивидуально назначают альфа-адреноблокаторы (феноксибензамин – при внутренней детрузорно-сфинктерной диссинергии, диазепам и баклофен – при внешней детрузорно-сфинктерной диссинергии), альфа-симпатомиметики (мидодрин и имипрамин – в случае недержания мочи при напряжении).
При медикаментозной терапии нейрогенного мочевого пузыря для профилактики мочевых инфекций необходимы контроль количества остаточной мочи и прием антибактериальных препаратов (нитрофуранов, сульфаниламидов), особенно пациентам с пузырно-мочеточниковым рефлюксом.
Хирургическое эндоскопическое вмешательство при гипотонии органа заключается в трансуретральной воронкообразной резекции шейки мочевого пузыря, обеспечивающей в дальнейшем возможность опорожнения слабым нажатием снаружи. При гиперрефлекторном варианте (со спастикой тазового дна и детрузорно-сфинктерной диссинергией) проводят надрез наружного сфинктера, что снижает напор мочеиспускания, а в последующем – гиперреактивность детрузора, увеличивая вместимость пузыря.
Также возможно оперативное увеличение мочевого пузыря (с использованием пластики тканей), ликвидация пузырно-мочеточникового рефлюкса, постановка цистостомического дренажа для опорожнения мочевого пузыря. Патогенетическое лечение синдрома нейрогенного мочевого пузыря позволяет уменьшить риск повреждения мочевыделительных органов и необходимость оперативного вмешательства в будущем.
Источник
