Муциновый слой мочевого пузыря
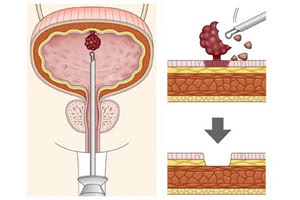
Опухолью мочевого пузыря называют доброкачественное новообразование, возникающее на его стенках. Наиболее часто патологические процессы происходят на задней и боковых стенках пузыря, шейке, в мочепузырном треугольнике (треугольник Льето), изменяя количественный и качественный состав клеток эпителия слизистых оболочек.
Доброкачественная опухоль мочевого пузыря, как правило, локализуясь на определённом участке поверхностей, изменяет его клетки, в результате чего образуются полипы, аденомы, эндометриоз, феохромоцитомы (фиброепителиомы), лейомиомы, рабдомиомы, невриномы и папилломы в мочевом пузыре, где преимущественно располагаются все опухоли мочевыделительной системы. Мужское население от 50 до 70 лет заболевает опухолевыми болезнями мочевого пузыря в 4 раза чаще, чем женское.
Эпителиального происхождения доброкачественные опухоли встречаются у 95-98% больных в виде папиллом и полипов, которые при озлокачествлениипроцесса могут перейти в разные виды рака мочевого пузыря и аденокарциному (90-96% от всех опухолей мочевого пузыря). Папиллома мочевого пузыря, невзирая на её морфологически доброкачественнуюструктуру, определяется как предраковая опухоль, потому как имеет склонность к частым рецидивами перерождению в злокачественную.
Доброкачественные опухоли мочевого пузыря отличаются отсутствием метастазирования, поражения здоровых тканей вокруг и продолжением роста после оперативного удаления. Самую большую распространенность среди мужчин после 45 лет получила аденома, хотя за последние десятки лет она значительно «помолодела».
Неэпителиального происхождения (из соединительной ткани) опухоли мочевого пузыря в виде фибром, миом, гемангиом, фибросарком — очень редко встречающиеся новообразования, хотя саркомы, дающие лимфогенные и гематогенные метастазы на ранних стадиях, определяются гораздо чаще.

Классификация опухолей мочевого пузыря
Доброкачественныеопухоли делятся на группы эпителиальногои неэпителиальногопроисхождения. К эпителиальным условно доброкачественным опухолям относятся:
- Папилломы, представляющие собой многочисленные длинные разветвленные ворсинки со множеством кровеносных сосудов, которые определяются как потенциально злокачественные, т.к. склонны к малигнизированию.
- Аденома (гиперплазия) предстательной железы, образующаяся из клеток слизистой мочевого пузыря или стромальной составляющей предстательной железы. Она имеет узелки, которые при увеличении размеров сдавливают мочевыводящий канал, мешая процессу мочеотделения.
- Эндометриозмочевого пузыря — это опухоль, являющаяся итогом гормональных нарушений, когда имеется избыток эстрогенов и дефицит прогестерона, с губчатой структурой из разнокалиберных кист на стенке, выпирающих в пузырь, на фоне повышенной отечности и гиперемии околослизистого пространства. Эндометриоз зависим от менструального цикла, имеет склонность к озлокачествлению клеток.
- Полипы — это выступающие над слизистым слоем мочевого пузыря патологические разрастания тканей.
- Феохромоцитома — нейроэндокринная опухоль в мышечном слое шейки, образовавшаяся из клеток хромаффинной ткани, выделяющей переизбыток катехоламинов.
- Типичная фиброэпителиома — нежное ворсистое новообразование на ножке, которое может размножиться.
- Атипичная фиброэпителиома — ворсинчатое образование с более грубыми ворсинками на более толстой ножке, с умеренно отечной и гиперемированной слизистой оболочкой вокруг. При объединении с папилломатозом она опасна перерождением в злокачественную опухоль.
К неэпителиальным доброкачественным опухолям мочевого пузыря относятся фибромы, миомы, фибромиксомы, гемангиомы, липомы, лимфангиомы, опухоль Абрикосова (зернистоклеточная опухоль), невриномы, встречающиеся в урологической практике относительно нечасто.
Прогноз и профилактика доброкачественных опухолей мочевого пузыря
В основной практике полипы и папилломы продолжительное время могут никак себя не проявлять, поэтому их обнаружение и лечение на запущенных стадиях озлокачествления редко даёт положительные результаты. Чтобы избежать усложнений заболевания, люди из группы риска должны периодически обследоваться, избавляться от провоцирующих опухолеобразование болезней, вести здоровый образ жизни и находиться под наблюдением врача. Послеоперационный период при неосложненных новообразованиях длится недолго, и возврат к нормальной полноценной жизни равен практически 100%.
Причины развития доброкачественных опухолей мочевого пузыря
Этиология развития опухолей мочевого пузыря окончательно не определена, однако, исходя из известных факторов, определяются следующие:
- анилиновые красители, особенно их производные — ароматические амины с их конечными метаболитами (бензидином, нафтиламином и др.), обладающие канцерогенным действием на работников лакокрасочных, бумажных, химических и резиновых производств;
- различные канцерогены окружающей среды, попадая в организм и выводясь с мочой, приобретают патологическое влияние на уротелий при застое мочи;
- курение и стаз мочи являются толчковым механизмом к образованию опухолей мочевого пузыря, когда ортоаминофенолы (продукты конечного обмена аминокислоты триптофана) вызывают разрастание клеток эпителия мочевыводящего тракта;
- возраст и пол больного, анатомические особенности строения мужской мочевыводящей системы, морфологические отличия слизистой пожилых людей, часто приводящие к застою мочи;
- наличие и частота воспалительных заболеваний уретры и мочевого пузыря, таких как шеечный цистит, простатит, мочекаменная болезнь, лейкоплакия, изъязвления мочевого пузыря;
- нарушения гормонального фона, снижение активности Т-системы иммунитета;
- паразитарные инвазии типа бильгарциоза, шистомоза и другие.
Кроме этого, существует обсуждаемая тема в мировой медицине о вирусном происхождении новообразований в мочевом пузыре.
Симптомы доброкачественных опухолей мочевого пузыря
Доброкачественная опухоль мочевого пузыря, симптомы которой обычно никак не проявляются, обнаруживается, как правило, случайно. Основные и наиболее выраженные симптомы доброкачественных опухолей:
- гематурия различных типов выраженности (микро-, макрогематурия, тотальная, терминальная): главный симптом при любой доброкачественной опухоли — это наличие крови и её сгустков в мочевой жидкости на различных этапах мочеиспускания у большинства пациентов, что отличает виды и стадии опухоли;
- дизурия — затрудненное мочеиспускание, наблюдаемое у трети пациентов с частотой, увеличивающейся в результате ухудшения состояния больного;
- вторичный цистит и восходящий пиелонефрит как результат распада новообразования;
- различной выраженности дискомфорт, жжение или болезненность при мочеиспускании;
- докучающие позывы к мочеиспусканию;
- недержание мочи у мужчин и женщин;
- ложные позывы к дефекации, боль, распространяющаяся в промежность, прямую кишку, крестец при опухоли шейки мочевого пузыря;
- нарушение опорожнения мочевого пузыря при сжимании устьев мочеточников опухолями приводит к проявлению признаков хронической почечной недостаточности, пиелонефроза и уретерогидронефроза;
- болевые ощущения, рези внизу живота, локализующиеся в лобковой, а затем и в паховой области.
Иногда, вследствие перекручивания полипа или папилломы пузыря, происходит острое нарушение кровообращения, ведущее к инфаркту новообразования, что сопровождается усилением гематурии. Доброкачественные опухоли мочевого пузыря являются катализаторами рецидивов воспалительных заболеваний мочевыводящих путей — циститов, восходящих уретеропиелонефритов.
Опасность перерождения доброкачественных тканей папиллом мочевого пузыря в злокачественные наиболее велика у заядлых курильщиков. Папилломы мочевого пузыря имеют склонность к повторному прорастанию с непредсказуемой периодикой, с каждым рецидивом становясь более злокачественными, чем прежде удаленные опухоли.
Обнаружили симптомы данного заболевания?
Звоните
Наши специалисты проконсультируют Вас!
Диагностика доброкачественных опухолей мочевого пузыря

Чтобы выявить и достоверно определить наличие, тип и стадию опухоли мочевого пузыря, необходимо провести комплексную диагностику пациента всеми доступными в настоящее время методами. Особенно следует отметить следующие.
Бимануальная пальпация (ручное исследование) — обязательное исследование, однако маленькие опухоли, выросшие вовнутрь, как правило, не пальпируются, а новообразование, которое удалось пальпировать, указывает на распространившееся проникающее поражение мочевого пузыря.
Ряд клинических и биохимических анализов крови и мочи через определённые этапы времени, позволяющие провести точную оценку развития заболевания.
Рентгенологическое исследование пузыря с введением контрастного вещества (экскреторная урография) в полость пузыря для определения дефекта наполнения его мочевой жидкостью и определения состояния его слизистой оболочки. Иногда это исследование проводят в условиях двойного контрастирования, вводя кислород в мочевой пузырь и окружающую его клетчатку, чтобы уточнить степень инфильтрации стенки пузыря и распространения её на окружающие участки.
Эндоскопическое исследование полости пузыря (цистоскопия) предоставляет его внутреннюю картину, помогает с достаточной точностью определить вид опухоли, её характеристики и площадь поражения с обязательным получением тканей и мочи для бактериологического анализа.
Цитологический анализ мочевой жидкости с целью выявления атипичных клеток проводится в случаях, когда нет возможности произвести биопсию на гистологию.
Трансуретральная пункционная биопсия тканей опухоли для определения их гистологии выполняется как отдельная процедура или при трансуретральной резекции мочевого пузыря.
УЗИ (ультразвуковое исследование) пузыря и органов малого таза выявит новообразование, его вид, размеры, экспозицию и широту распространенности.
Использование магнитно-резонансной и компьютерной томография почек с введением контрастного вещества позволит обнаружить опухоль пузыря, степень её прорастания в стенки и соседние органы, развитие метастазов в регионарных лимфатических узлах.
Экскреторная томография с введением контрастных веществ в вену позволит осуществить контроль над их выходом из почек и последующим выводом из организма.
Лечение доброкачественных опухолей мочевого пузыря
Хирургическое удаление является обязательным при диагностике доброкачественных новообразований методом трансуретральной резекции, эндоскопии, электро- или лазерной коагуляции опухоли. Также предписывается полное удаления мочевого пузыря в случае значительного вовлечения его и уретры в опухолевый процесс.
Лекарственное лечение обычно бывает направлено на укрепления местного и общего иммунитета.
Противовоспалительная, противопаразитарная и противовирусная терапия назначается при необходимости.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом
или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Источник
Хронические воспалительные заболевания нижних мочевых путей у женщин чрезвычайно распространены и являются частой причиной обращения пациенток к урологу, гинекологу, терапевту и врачам других специальностей. Расстройства мочеиспускания являются причиной ежегодного обращения к врачу около 3 млн женщин в США. В России заболеваемость циститом составляет 15-20 тыс. на 1 млн человек, около 20-25% женщин переносят цистит в той или иной форме, а примерно 10% пациенток страдают хроническим циститом [1].
[1]. В России примерно 10% женщин страдают хроническим циститом
Для инфекций нижних мочевых путей (НИМП) характерно рецидивирование. Установлено, что у 50% женщин после эпизода цистита в течение года развивается рецидив, у 27% молодых женщин рецидив развивается в течение 6 месяцев после первого эпизода цистита, причем у 50% больных рецидивы отмечаются более 3 раз в год. Такая высокая частота рецидивирования объясняется следующими факторами:
– анатомо-физиологическими особенностями женского организма (короткая и широкая уретра, близость к естественным резервуарам инфекции – анусу, влагалищу), возможными аномалиями расположения наружного отверстия уретры;
– частыми сопутствующими гинекологическими заболеваниями – воспалительными процессами во влагалище, гормональными нарушениями, приводящими к нарушению биоценоза влагалища и колонизации в нем патогенной микрофлоры
– генетической предрасположенностью;
– способностью грамотрицательных микроорганизмов, вызывающих инфекционный процесс в уретре и мочевом пузыре, к адгезии к клеткам эпителия, вследствие наличия фимбрий и ворсин;
– частой ко-инфекцией атипичными микроорганизмами (уреаплазмой, хламидиями, микоплазмой и др.), приводящей к стойким морфологическим перестройкам уротелия
Мочевой пузырь у здоровых женщин обладает защитными механизмами, препятствующими бактериальной инвазии. В норме переходный эпителий мочевого пузыря (уротелий) выделяет на поверхность гликозаминогликановую (мукополисахаридную) субстанцию (рис. 1), препятствующую адгезии бактерий, миграции компонентов мочи в подслизистый слой. Разрушение слоя муцина приводит к усилению миграции ионов калия в интерстиций. В ряде работ показано, что миграция ионов калия в интрестиций приводит к деполяризации сенсорных нервных окончаний, спазму гладкой мускулатуры, повреждению кровеносных и лимфатических сосудов. Нормальный уровень калия в моче колеблется в пределах 20-150 ммоль/л, в случае повреждения муцинового слоя этой концентрации достаточно, чтобы вызвать стойкую дизурию.
Нередко при обследовании женщин со стойкой дизурией в общем анализе мочи и посеве мочи отсутствуют патологические изменения. Пациентки проходят множество неэффективных курсов общего и местного лечения, нередко у них предполагают наличие интерстициального цистита и даже психические заболевания. Однако известно, что при обследовании пациенток со стойкой дизурией, интерстициальный цистит обнаруживается лишь у 3,6 % пациенток.
По данным разных авторов при цистоскопии у 63,6–100% пациенток со стойкой дизурией, хронической тазовой болью обнаруживается лейкоплакия с расположением в шейке мочевого пузыря и мочепузырном треугольнике [10]. В то же время лейкоплакия до настоящего времени является наиболее неизученным заболеванием слизистой оболочки мочевого пузыря. В свете современных исследований лейкоплакия представляет собой патологический процесс, который характеризуется нарушением основных функций многослойного плоского эпителия: отсутствием гликогенообразования и возникновением ороговения – которые в норме отсутствуют [12].
Лейкоплакией принято называть белесоватые пятна на видимых слизистых оболочках (полости рта, мочевых органов, шейки матки и др). При морфологическом исследовании участков лейкоплакии обнаруживается метаплазия переходного эпителия в многослойный плоский, иногда с ороговением. С момента первого описания лейкоплакии мочевого пузыря были предложены разнообразные теории ее возникновения. Среди причин называли дефекты эмбрионального развития, инфекции (туберкулез, сифилис), гиповитаминоз витамина А, но в настоящее время эти теории опровергнуты. Долгое время была принята теория возникновения лейкоплакии мочевого пузыря вследствии воспаления, в пользу которой высказывался П.А. Герцен (1910). Однако в работах зарубежных морфологов показано, что метаплазия эпителия сопровождается отеком подлежащей ткани и вазодилятацией, но не выраженным воспалением. По аналогии с лейкоплакией других локализаций, лейкоплакию мочевого пузыря многие авторы рассматривали как предраковое состояние. Между тем не имеется ни одного достоверного случая перехода плоскоклеточной метаплазии уротелия в рак.
Бесспорна роль урогенитальных инфекций (Ch. trachomatis, U. urealiticum, N.gonorrhoeae, M. genitalium, T.vaginalis, H. simplex I, II) в этиологии уретритов, циститов у женщин [3, 9, 10]. Однако под воздействием возбудителей урогенитальных инфекций, в отличие от неспецифических патогенов (E. coli и др.), происходит не обычное воспалительное повреждение тканей мочевого тракта. В ответ на урогенитальные инфекции в уротелии обнаруживаются различные формы дистрофического повреждения с исходом в плоскоклеточную метаплазию чаще без ороговения. В зоне плоскоклеточной метаплазии (лейкоплакии) наблюдается разрушение муцинового слоя, разобщение и десквамация клеток поверхностного слоя. Показано, что у пациенток со стойкой дизурией и ургентностью с или без бактериурии при цистоскопии с биопсией выявлялась плоскоклеточная метаплазия с разной выраженностью подслизистого фиброза. Интересно, что при выраженной степени морфологических изменений, бактерии отсутствовали [13, 14, 15].
Инфекция является причинным фактором повреждения уротелия и формированием метаплазии, в то время как дальнейшая альтерация происходит вне зависимости от инфекции, приводя к стойкой дизурии. У пациенток с лейкоплакией имеется повышенная проницаемость эпителия, невозможна адаптивная перестройка уротелия при физиологическом наполнении мочевого пузыря, что приводит к диффузии компонентов мочи в интерстиций и развитию учащенного, болезненного мочеиспускания, болей над лоном, в уретре и т.д [16]. Длительно протекающие инфекции, особенно на фоне заболеваний, передающихся половым путем (Chlamidia trachomatis, Ureaplasma urealiticum, N.gonorrhoeae, Mycoplasma hominis, T. vaginalis, Herpes simplex I,II) приводят к выраженным морфологическим изменениям уротелия, так называемым поствоспалительным изменениям уротелия.Наиболее часто развивается лейкоплакия мочевого пузыря, реже формируются псевдополипы.
На кафедре урологии и хирургической андрологии РМАПО был разработан алгоритм обследования и лечения пациенток со стойкой дизурией, вызванной лейкоплакией мочевого пузыря.
В план обследования пациенток со стойкой дизурией должны входить:
1. Тщательно собранный анамнез:
Особенности течения рецидивирующих инфекций мочевых путей, протекающих после перенесенных или на фоне инфекций, передающихся половым путем:
a) длительность заболевания более 2 лет;
b) наличие поллакиурии вне периода обострения до 11-14 раз в сутки;
c) постоянные выраженные боли над лоном, в области уретры, влагалища, которые приводили к сексуальной и социальной дезадаптации;
d) неэффективность традиционной антибактериальной терапии.
2. Общий анализ мочи.
3.Посев мочи на флору и чувствительность к антибиотикам
4.Осмотр в «зеркалах» для исключения анатомических изменений, с проведением пробы O’Donnel.
5.Осмотр гинекологом.
6.Обследование на наличие инфекций, передающихся половым путем (ИППП), 2 методами из 2 локусов (цервикальный канал и уретра).
7. Ультразвуковое исследование органов мочевой и половой системы,
8.Цистоскопия с биопсией и морфологическим исследованием биоптата.
Аномалии расположения наружного отверстия уретры. Часто у пациенток с указанной патологией манифестация мочевой инфекции происходит в детском возрасте: развиваются вагиниты, рецидивирующие хронические уретриты, циститы. После начала половой жизни после полового акта отмечается значительное усиление симптомов . При влагалищном осмотре определяется вагинализация уретры, уретро-гименальные спайки, положительным оказывается тест O’Donnel. Ретроградное инфицирование нижних мочевых путей приводит к формированию и поддержанию хронического воспалительного процесса в уретре, мочевом пузыре и стойкой дизурии [6].
При обнаружении изменений в общем анализе мочи и росте флоры в посеве мочи следует назначить курс антибактериальной терапии с учетом данных антибиотикограммы. При наличии ИППП препаратами выбора являются макролиды(джозамицин, азитромицин, мидекамицин), тетрациклины (доксициклин), фторхинолоны (моксифлоксацин, левофлоксацин, офлоксацин). При выявлении генитального герпеса проводится противовирусная терапия (ацикловиром, валацикловиром, фамцикловиром) [4, 7, 8].
После лечения или в случае отсутствия патологических изменений в анализах у всех пациенток с длительностью заболевания более двух лет обязательно проводят уретроцистоскопию с биопсией мочевого пузыря. Это необходимо для уточнения локализации поражения мочевого пузыря и определения степени диспластических процессов в зоне шейки мочевого пузыря и мочепузырного треугольника,исключения заболеваний мочевого пузыря и уретры, протекающих со сходной клинической симптоматикой (опухоли, туберкулеза, эндометриоза и т.д). Лейкоплакия при рецидивирущих инфекциях в основном локализуется в задней уретре, шейке мочевого пузыря и мочепузырном треугольнике, иногда в зоне шейки мочевого пузыря обнаруживаются псевдополипы (рис. 2).
Несмотря на то, что эндоскопическая картина лейкоплакии мочевого пузыря весьма характерна, необходимо гистологическое подтверждение диагноза. Дифференциальный диагноз следует проводить с плоскоклеточной папилломой и, в редких случаях, с раком мочевого пузыря.
После морфологического подтверждения диагноза возможно проведение лечения.
Лечение лейкоплакии мочевого пузыря должно быть комплексным. Наиболее эффективным лечением лейкоплакии является курс внутрипузырной терапии. Однако до ее начала обязательно проводится лечение неспецифической и специфической инфекции мочевых путей.
[1]. Наиболее эффективным лечением лейкоплакии является курс внутрипузырной терапии
Выбор антибактериального препарата при рецидивирующих инфекциях должен производиться на основе данных микробиологического исследования. Антибактериальная терапия должна быть длительной (до 7-10 дней). Выбор препарата производят с учётом выделенного возбудителя и антибиотикограммы. Необходимо назначение антибиотиков с бактерицидным действием. Препаратами первой линии терапии неосложненных инфекций нижних мочевых путей, в случае исключения наличия ИППП, являются такие препараты как фосфомицин-трометамол, фторхинолоны (норфлоксацин), нитрофурантоин.При обнаружении ИППП препаратами выбора являются макролиды (джозамицин, азитромицин, мидекамицин), тетрациклины (доксициклин), фторхинолоны (моксифлоксацин, левофлоксацин, офлоксацин). При выявлении генитального герпеса проводится противовирусная терапия (ацикловиром, валацикловиром, фамцикловиром). После окончания курса терапии необходимо проведение культурального контроля.
Альтернативным подходом в лечении инфекций мочевых путей является стимуляция собственных иммунных механизмов пациента, направленных против патогенной флоры, с помощью орального назначения иммунотерапевтических препаратов. Одним из таких препаратов является уро-ваксом − лиофилизированный белковый экстракт, полученный путем фракционирования щелочного гидролизата наиболее распространенных уропатогенных штаммов E. coli. Препарат применяется по 1 капсуле в сутки натощак в течение 3 месяцев, затем по 1 капсуле в сутки натощак в течение 10 дней каждого месяца в течение 3 месяцев. Мы рекомендуем прием препарата после проведения специфической терапии.
Заслуживает внимания применение бактериофагов в лечении хронических рецидивирующих ИМП, что особенно актуально для пациентов с поливалентной аллергией к антибактериальным препаратам или наличием полирезистентных возбудителей. Несмотря на отсутствие плацебо-контролируемых исследований применения бактериофагов, клиническая эффективность указанных препаратов не вызывает сомнений. Перед назначением лечения обязателен посев мочи с определением чувствительности возбудителя к бактериофагам. В стандартной схеме бактериофаги применяются по 20 мл х 3 раза в день за 40 минут до еды в течение 2 недель.
[2]. Перед назначением лечения обязателен посев мочи с определением чувствительности возбудителя к бактериофагам
[3]. После проведения курса противовоспалительной терапии необходимо местное лечение лейкоплакии мочевого пузыря, направленной на восстановлении муцинового слоя
После проведения курса противовоспалительной терапии необходимо местное лечение лейкоплакии мочевого пузыря, направленной на восстановлении муцинового слоя.Наиболее целесообразны инстилляции природных или синтетических аналогов гликозаминогликанов в мочевой пузырь (гепарина, гиалуроновой кислоты, хондроитина сульфата, пентозанполисульфата и др.). Под воздействием инстилляций аналогов ГАГ происходит восстановление муцинового слоя, регрессия плоскоклеточной метаплазии. Используется схема терапии, подобная лечению интерстициального цистита, при котором также обнаруживают дефекты муцинового слоя [18]. Наиболее доступным и эффективным препаратом для лечения лейкоплакии мочевого пузыря является гепарин, который вводят внутрипузырно в виде раствора: гепарин – 25 тысяч единиц – 5 мл, 2 % раствор лидокаина – 2 мл, 0,9 % раствор натрия хлорида – 13 мл; инстилляции проводят 2-3 раза в неделю в течение 3 месяцев. Для профилактики обострений инфекции инстилляции целесообразно проводить на фоне приема уроантисептиков, препаратом выбора может являться растительный препарат канефрон, назначаемый на весь курс инстилляций по 2 драже 3 раза в день или по 50 капель 3 раза в день. После окончания лечения проводится контрольная уретроцистоскопия.
[4]. Наиболее доступным и эффективным препаратом для лечения лейкоплакии мочевого пузыря является гепарин, который вводят внутрипузырно в виде раствора. Инстилляции проводят 2-3 раза в неделю в течение 3 месяцев
При наличии псевдополипоза шейки мочевого пузыря или неэффективности консервативной терапии лейкоплакии показано хирургическое лечение в объеме трансуретральной электровапоризации или электрорезекции пседополипов, лейкоплакии [7,15].
Пациенткам, у которых стойкая дизурия развилась и поддерживается на фоне «вагинализации» наружного отверстия уретры, показана операция транспозиция уретры, рассечение уретро-гименальных спаек после проведения лечения лейкоплакии мочевого пузыря.
На рис. 4 представлены обобщенные данные о патогенезе и лечении лейкоплакии мочевого пузыря у женщин.
В основе успешного лечения расстройств мочеиспускания лежит проведение тщательной дифференциальной диагностики заболеваний, которые приводят к дизурии. Лечение расстройств мочеиспукания в большинстве случаев должно быть комплексным, воздействующим на различные звенья патогенеза болезни.
Литература
1. Лоран О.Б., Зайцев А.В., Годунов Б.Н., Каприн А.Д., Давидьянц А.А. //Урол. и нефрол. – 1997. – №6. – С.7-14.
2. Загребина О.С.Этиологическое значение Ureaplasma urealiticum в развитии воспалительных процессов половых и мочевых органов у женщин: Дисс. … канд. мед. наук – М., 2001. – С. 8-20, 130-136.
3. Parsons C. Lowell. //Contemp.urol. – 2003. – Feb. – P.22-31.
4. Перепанова Т.С, Кудрявцев Ю.В., Хазан П.Л // Consilium Medicum Прил.Урология. – 2002. – С.5-9.
5. Астапов А.И. Трансуретральная электровапоризация в комплексном лечении женщин страдающих хроническим циститом: Дисс. … канд. мед. наук – М., 2003
6. Гвоздев М.Ю. Транспозиция дистального отедла уретры в оперативном лечении и сексуальной реабилитации женщин, страдающих хроническим циститом: Дисс. … канд. мед. наук – М., 2000. – С.18.
7. Страчунский Л.С., Рафальский В.В., Сехин С.В., Абрарова Э.Р //Урология. – 2002. – №2. – С.8-14.
8. Яковлев С.В. //Consilium medicum. – 2001. – Т.3. – №7. – С.300-306.
9. Косова И.В. Роль урогенитальных инфекций в этиологии циститов и необструкутивных пиелонефритов у женщин: Дисс. … канд. мед. наук – М., 2005.
10. Burkhard FC, Blick N, Studer UE “Urinary urgency, and chronic urethral and/or pelvic pain in females. Can doxycycline help?” //J Urology, 2004
11. Patelli E, Mantovani F, Catanzaro M, Pisani E “Urgency-frequency syndrome in women: interstitial cystitis and correlated syndromes” //Arch Ital Urol Androl. – 1999; Dec; 71(5): 317-20.
12. Смирнов Д.С. «Особенности диагностики и лечения больных с лейкоплакией мочевого пузыря» Авт. дисс. – СПб, 2007.
13. Okamura K, Ito K, Suzuki Y, Shimoji T «Histological study of cases of bladder cancer and chronic cystitis with difficulty in cystoscopic diagnosis» Hinyokika Kiyo. – 1984; Apr; 30(4): 459-65.
14. Vitoratos N, Gregoriou O, Papadias C, Liapis A, Zourlas PA. «Sexually transmitted diseases in women with urethral syndrome» //Int J Gynaecol Obstet. – 1988; Oct; 27(2): 177-80.
15. Murakami S, Igarashi T, Takahara M, Yamanishi T, Shimazaki J, Shigematsu H. «Squamous metaplasia of the trigone in women with recurrent cystitis syndrome» //Hinyokika Kiyo. – 1985; Feb; 31(2): 301-7.
16. Sideri M, De Virgiliis G, Rainoldi R, Ferrari A, Remotti G. Junctional pattern in the squamous metaplasia of the female trigone. A freeze-fracture study. //J Urol. 1983 Feb;129(2):280-3.
17. Зайцев А.В. Диагностика и лечение интерстициального цистита у женщин: Дисс.док.мед.наук. – М.,1999.
Рисунки смотрите в приложении
Источник
