Мочевой пузырь болезнь при травме
Травма мочевого пузыря — это нарушение целостности стенки органа, вызванное механической травмой, воздействием химических веществ, редко – давлением мочи при некоторых заболеваниях. Проявляется болью в животе, припухлостью и синюшностью кожи над лоном, учащенными ложными позывами к мочеиспусканию, снижением или отсутствием диуреза, макрогематурией, подтеканием мочи из раневого отверстия, нарастанием симптоматики травматического шока. Диагностируется с помощью ретроградной цистографии, катетеризации, УЗИ, КТ, МРТ мочевого пузыря, общего анализа мочи, лапароскопии. В легких случаях возможно консервативное ведение с установкой катетера, при внутрибрюшинных и крупных внебрюшинных разрывах выполняется реконструктивная пластика органа.
Общие сведения
В структуре общего травматизма механические повреждения мочевого пузыря составляют от 0,4 до 15% (в России — от 1 до 7%). В последние годы отмечается более частое травмирование органа, что связано с усилением интенсивности транспортного сообщения, износом автопарка, увеличением количества тяжелых техногенных катастроф и локальных военных конфликтов.
Пик травматизации наблюдается в 21-50-летнем возрасте, около 75% пострадавших — мужчины. Особенностью травм является преимущественно сочетанный характер поражения (в 100% открытых ранений и в 85% тупых травм кроме мочевого пузыря повреждаются кости таза, позвоночник, другие органы). Актуальность своевременной диагностики и экстренных лечебных мероприятий обусловлена неблагоприятным прогнозом – в соответствии с оценочными шкалами 31,4% пострадавших относятся к категории тяжелых, 49,2% — крайне тяжелых больных, уровень смертности превышает 25%.

Травма мочевого пузыря
Причины
У большинства пациентов травматическое повреждение мочевого пузыря связано с воздействием на его стенку внешних механических факторов различного происхождения. В редких случаях травма обусловлена влиянием агрессивных химических веществ, инсталлированных в мочевой пузырь, или наличием заболеваний, препятствующих мочеиспусканию. Причинами травм являются:
- Дорожно-транспортные происшествия. Более чем в четверти случаев мочевой пузырь травмируется во время ДТП. Повреждение возникает при прямом ударе в проекцию органа, сильном сдавлении в транспортном средстве, ранении осколками тазовых костей, конструктивными элементами автомобиля, предметами окружающей среды.
- Ятрогенные факторы. 22-23% пациентов получают травму во время медицинских манипуляций. Стенка органа может повреждаться при его катетеризации, бужировании уретры, выполнении операций — трансуретральных вмешательств, кесарева сечения, экстирпации матки, миомэктомии, аденомэктомии, резекции толстой кишки и др.
- Бытовой и производственный травматизм. В 10% случаев повреждение происходит из-за падения с высоты на твердый предмет. При наличии предпосылок (переполнении мочой, рубцовых изменениях и др.) возможен разрыв органа из-за резкого сотрясения тела при прыжке. У 4,2% пострадавших травма возникает под действием производственных факторов.
- Насильственные действия. Целостность мочевого пузыря может нарушаться при тупых ударах в живот, ранении ножом или другими острыми предметами в драках, при криминальных абортах. В военное время в 3-4 раза увеличивается количество огнестрельных травм и открытых ранений органа осколками взрывных боеприпасов.
- Урологические заболевания. Крайне редко самопроизвольный разрыв мочевого пузыря отмечается у пациентов, которые страдают заболеваниями, нарушающими мочеиспускание, — аденомой и раком простаты, стенозом уровезикальной шейки, стриктурами уретры. Чаще урологическая патология играет роль предрасполагающего фактора, усиливая растяжение органа.
Риск возникновения наиболее тяжелых повреждений — частичных или полных разрывов — зависит не только от силы травматического воздействия, но и от места его приложения, направления, внезапности. Вероятность получения травмы существенно возрастает при алкогольном опьянении, которое способствует переполнению мочевого пузыря из-за притупления позывов к мочеиспусканию и провоцирует травмоопасное поведение. Предполагающими факторами также являются опухолевые поражения, фиброзные изменения стенки органа после перенесенных операций, лучевой терапии, воспалительных заболеваний.
Патогенез
Механизм травмы мочевого пузыря зависит от типа факторов, вызвавших повреждение. При тупом ударе в надлобковую область, противоударе о крестец, сдавлении резко повышается внутрипузырное давление, усиливается нагрузка на мочепузырную стенку. Возникновение гидродинамического эффекта способствует внутрибрюшинному разрыву органа на участке наименее развитой мускулатуры (обычно по задней стенке пузыря возле его верхушки).
Рана обычно рваная, с неровными краями. При меньшей силе механического воздействия удар вызывает закрытые повреждения (ушибы, кровоизлияния в стенку). Аналогичный патогенез характерен при наличии урологических заболеваний с нарушением пассажа мочи. Значительное смещение пузыря при механических травмах приводит к резкому натяжению поддерживающих боковых и пузырно-простатических связок с внебрюшинным разрывом мягко-эластичной стенки органа. Сильный удар способен вызвать разрыв связок, мочепузырных кровеносных сосудов, отрыв шейки.
При закрытых и открытых повреждениях везикальных оболочек острыми предметами, инструментами, осколками костей происходит поверхностное, глубокое надсечение или сквозное рассечение стенки. Рана при этом обычно линейная. Сочетание с гидродинамическим ударом при огнестрельных и оскольчатых ранениях приводит к дополнительным радиальным надрывам круглого раневого отверстия.
Классификация
Критериями систематизации травматических повреждений являются степень тяжести, возможное сообщение с окружающей средой, расположение разрыва по отношению к брюшине, сочетание с травмами других органов. Такой подход позволяет спрогнозировать течение патологического процесса и вероятные осложнения, выбрать оптимальную тактику ведения пациента. В зависимости от тяжести повреждения мочепузырной стенки травмы могут быть глухими (ушиб, поверхностное ранение наружной оболочки, надрыв слизистой) или сквозными (полный разрыв, отрыв шейки). В свою очередь, сквозные повреждения разделяют на три группы:
- Интраперитонеальные разрывы. Наблюдаются более чем у 60% пострадавших. Обычно обусловлены прямыми ударами в переполненный мочевой пузырь. Из-за истечения мочи в брюшную полость быстро осложняются перитонитом.
- Экстраперитонеальные разрывы. Возникают в 28% случаев. Чаще провоцируются избыточным натяжением поддерживающего связочного аппарата. Травмированный мочевой пузырь не сообщается с брюшной полостью, моча истекает в малый таз.
- Комбинированные разрывы. Наблюдаются у 10% пострадавших. Множественное повреждение стенки органа обычно сочетается с переломами тазовых костей. Сообщение между мочевым пузырем, брюшной и тазовой полостями обуславливает особую тяжесть патологии.
До 90% травм мирного времени являются закрытыми, благодаря сохранению целостности кожи поврежденный мочевой пузырь не сообщается с внешней средой. В военный период, при насильственных действиях с использованием холодного и огнестрельного оружия возрастает частота открытых травм, при которых нарушается целостность кожи, возникает сообщение между оболочками или полостью органа и окружающей средой. По наблюдениям специалистов в сферах травматологии и клинической урологии, сочетанные повреждения превалируют над изолированными. У 40-42% пациентов выявляются переломы костей таза, у 4-10% — разрывы кишечника, у 8-10% — травмы других внутренних органов.
Симптомы
Важная клиническая особенность данного повреждения — частое преобладание общей симптоматики над локальной. Из-за выраженного болевого синдрома и кровотечения у пострадавших нарастают признаки гемодинамических нарушений, у 20,3% наблюдается травматический шок: снижается уровень АД, ускоряется частота сердечных сокращений, кожные покровы бледнеют, покрываются липким холодным потом, возникает слабость, головокружение, оглушенность, спутанность, а затем и потеря сознания.
Из-за раздражения брюшины мочой пациенты с интраперитонеальными разрывами ощущают интенсивную боль в надлонной области, в нижней части брюшной полости, которая впоследствии распространяется на весь живот, сопровождается тошнотой, рвотой, задержкой газов и стула, напряжением брюшной мускулатуры. Специфические симптомы травмы мочепузырной стенки — боль и локальные изменения области повреждения, дизурия. При открытых ранениях на передней стенке живота, реже — в зоне промежности выявляется зияющая рана, из которой может истекать моча.
Для закрытых внебрюшинных травм характерно образование болезненной припухлости над лобком, в паху, синюшный цвет кожных покровов из-за их пропитывания кровью. Пострадавшие испытывают частые ложные позывы к мочеиспусканию со значительным уменьшением либо полным отсутствием диуреза, выделением капель крови из мочеиспускательного отверстия. При сохранении мочевыделения у пациентов с надрывами слизистой моча окрашена кровью.
Осложнения
Летальность при травматических повреждениях мочевого пузыря, особенно открытых и сочетанных, достигает 25% и более. Причинами смерти обычно являются запущенные формы перитонита, болевой, инфекционно-токсический, геморрагический шок, сепсис. Сквозные травмы стенки мочевого пузыря быстро осложняются вовлечением в процесс других органов. Анатомические особенности паравезикальной, забрюшинной клетчатки, фасциальных пространств способствуют мочевой инфильтрации, распространению затеков, образованию урогематом.
При внутрибрюшинном разрыве возникает уроасцит. Вторичное инфицирование приводит к формированию абсцессов, флегмон. У 28,3% пациентов развивается мочевой перитонит, у 8,1% — уросепсис. Восходящее распространение инфекции провоцирует начало острого пиелонефрита. В 30% случаев при сочетании травмы пузыря с повреждениями других органов наблюдается ДВС-синдром. В отдаленном периоде у больных иногда формируются мочевые свищи, наблюдается недержание мочи.
Диагностика
С учетом серьезности прогноза всем пациентам с подозрением на травму мочевого пузыря назначают комплексное обследование, позволяющее выявить разрывы мочепузырной стенки, определить их особенности и количество, обнаружить возможное повреждение смежных органов. Рекомендованными методами лабораторной и инструментальной диагностики являются:
- Общий анализ мочи. Исследование удается провести только при сохраненном мочеиспускании. Объем разовой порции зачастую уменьшен. В анализе в большом количестве присутствуют эритроциты, подтверждающие наличие кровотечения.
- УЗИ. По данным эхографии мочевого пузыря, орган обычно уменьшен в объеме, рядом с ним определяются скопления крови. Исследование дополняют УЗИ почек, при проведении которого обнаруживаются признаки постренального нарушения оттока мочи, и УЗИ брюшной полости для выявления свободной жидкости.
- Рентген. Ретроградная цистография считается «золотым стандартом» диагностики этого вида травм. Разрывы органа проявляются затеками рентгеноконтрастного вещества в пузырно-прямокишечную ямку, околопузырную клетчатку, область крыльев подвздошной кости, полость брюшины.
- Томография мочевого пузыря. С помощью КТ удаётся получить трехмерное изображение поврежденного органа, в ходе МРТ он изучается послойно. Результаты томографии позволяют точно оценить повреждения, объем урогематом, выявить сочетанные травмы.
- Диагностическая лапароскопия. Осмотр мочевого пузыря через лапароскоп дает возможность определить особенности травмированной стенки, обнаружить затеки мочи, крови. При выполнении лапароскопии визуализируются повреждения соседних органов.
Большое диагностическое значение играет катетеризация мочевого пузыря, дополненная вливанием в него жидкости (проба Зельдовича). О наличии разрывов свидетельствует отсутствие мочевыделения через катетер или поступление небольшого количества мочи с кровью. Жидкость, введенная в травмированный орган, обратно выделяется слабой струей и не в полном объеме. При интраперитонеальных разрывах возможно отхождение в 2-3 раза большего объема жидкости, что обусловлено проникновением катетера в брюшную полость и выделением ранее попавшей в нее мочи.
Экскреторную урографию назначают с осторожностью, чтобы не спровоцировать развитие контраст-индуцированной нефропатии на фоне шоковых изменений гемодинамики. Цистоскопия обычно не проводится из-за риска занесения инфекции. В общем анализе крови определяются признаки анемии — эритропения, снижение уровня гемоглобина, возможен умеренный лейкоцитоз и повышение СОЭ.
Дифференциальная диагностика проводится с повреждением заднего отдела уретры, травмами печени, селезенки, различных отделов кишечника, разрывами сосудов брыжейки. Кроме врача-уролога пациента осматривает травматолог, хирург, анестезиолог-реаниматолог, терапевт, по показаниям — проктолог, гинеколог, кардиолог, гастроэнтеролог, невропатолог, нейрохирург.
Лечение травмы мочевого пузыря
Пострадавшего срочно госпитализируют в травматологическое или урологическое отделение, переводят на строгий постельный режим. Консервативное ведение в виде катетеризации (обычно на 3-5 суток до прекращения макрогематурии) возможно только при контузии мочевого пузыря, надрывах слизистой при грубых медицинских манипуляциях, небольших экстраперитонеальных разрывах с сохраненной уровезикальной шейкой. Остальным пострадавшим показано экстренное проведение реконструктивного хирургического вмешательства с дренированием брюшной или тазовой полостей.
На этапе предоперационной подготовки назначаются гемостатические, антибактериальные, противовоспалительные, анальгезирующие препараты, средства для стабилизации гемодинамики. Объем операции зависит от особенностей повреждения. При внутрибрюшинных разрывах мочевой пузырь перед ушиванием раны экстраперитонизируют для прекращения подтекания мочи и проведения полноценной ревизии, после реконструкции поврежденного органа брюшную полость в обязательном порядке санируют.
Внебрюшинные повреждения ушивают без экстраперитонизации. Вне зависимости от типа травмы после восстановления целостности стенки мужчинам накладывают эпицистостому , женщинам устанавливают уретральный катетер. Брюшную или тазовую полость дренируют. После операции продолжают введение антибиотиков, анальгетиков, противошоковую инфузионную терапию.
Прогноз и профилактика
Нарушения целостности стенок мочевого пузыря обоснованно считаются тяжелыми, прогностически неблагоприятными травмами. Соблюдение алгоритма хирургического лечения больных обеспечивает достоверное снижение частоты осложнений даже при тяжелых повреждениях. Профилактика направлена на создание безопасных производственных условий, соблюдение правил дорожного движения, выполнение требований безопасности при занятиях травмоопасными хобби и видами спорта, отказ от злоупотребления алкоголем. Для уменьшения предпосылок к травматизму пациентам с диагностированными заболеваниями простаты, уретры, мочевого пузыря рекомендуется регулярное наблюдение и лечение у уролога.
Источник
Статья посвящена проблеме нейрогенных расстройств мочеиспускания при травме позвоночника и спинного мозга
Путь пациента с осложненной травмой позвоночника, т. е. сопровождающейся повреждением спинного мозга, начинается с нейрохирургического оперативного вмешательства и продолжается многоэтапной реабилитацией, направленной на коррекцию сопутствующих осложнений и восстановление утраченных функций организма [1]. Для таких больных есть специфический термин – «спинальные».
Одним из тяжелейших последствий травмы спинного мозга является расстройство произвольного мочеиспускания, обусловленное нарушением проводимости спинномозговых путей. По данным М.Р. Касаткина, подобное осложнение встречается в 92,1% случаев закрытых повреждений спинного мозга [2]. Патогенез изменений функции нижних мочевых путей при травме спинного мозга, проявляющийся в утрате рефлекторной деятельности, сложен и многообразен [3].
Механизм нормального мочеиспускания и характер его расстройства у спинальных пациентов напрямую связаны с особенностями физиологии этой области. Периферическую иннервацию нижних мочевых путей осуществляют тазовый нерв, представляющий парасимпатическую нервную систему, гипогастральный нерв, реализующий симпатическую регуляцию, и пудендальный соматический нерв. Афферентную информацию несут волокна всех трех нервов – вегетативных от детрузора (гладкой мышцы мочевого пузыря) и уретры и полового нерва от тканей промежности. Первичным анализатором для парасимпатического тазового нерва являются нейроны сакрального центра мочеиспускания, расположенного на уровне S2‒S4 сегментов спинного мозга. Здесь же, в анатомическом соседстве, находится ядро Онуфа, представляющее собой скопление нервных клеток, аксоны которых образуют пудендальный нерв [4]. Симпатическая афферентная иннервация, опосредованная гипогастральным нервом, являющимся частью подчревного и поясничного сплетения, осуществляется через пограничный симпатический ствол и вставочные интернейроны боковых рогов спинного мозга на уровне его Th10‒L2 сегментов. Эти же нервы несут и эфферентные сигналы к иннервируемым органам. Регулирующие структуры спинного мозга связаны с вышерасположенными центрами иннервации проекционно, а также с помощью нейрогуморальных и рефлекторных механизмов [5]. Однако следует отметить, что концепции регуляции функции нижних мочевых путей в норме и патологии являются в большей степени эмпирическими, и единого понимания этого вопроса на сегодняшний день нет.
Клиническая картина
Врачу-неврологу, курирующему пациента с осложненной травмой позвоночника, необходимо оценить уровень и степень повреждения спинного мозга и учесть посттравматические сроки. Клиническая картина в острый и ранний периоды после получения травмы обусловлена спинальным шоком, что проявляется арефлексией и задержкой мочи. По мере восстановления можно наблюдать активизацию рефлекторной деятельности и формирование «в сухом остатке» нейрогенного расстройства мочеиспускания. При повреждении спинного мозга на уровне сакрального центра мочеиспускания и периферических нервных волокон развивается атония или гипотония детрузора, при этом за счет интактности симпатических структур иннервации внутренний уретральный сфинктер сохраняет сократительную способность. Таким образом, нарушается взаимосвязь симпатических и парасимпатических влияний [6]. Клинически наблюдается нейрогенная задержка мочеиспускания с элементами парадоксальной ишурии (выделения мочи по каплям на фоне переполненного мочевого пузыря). При локализации травмы выше сакрального центра и ядра Онуфа повреждаются проводниковые нервные волокна, осуществляющие взаимосвязь регулирующих структур, однако сами центры иннервации могут быть интактны. В этом случае и детрузор, и внутренний сфинктер уретры способны к циклическому сокращению и расслаблению, но рассогласованность в работе приводит не к нормальному акту мочеиспускания, а к детрузорно-сфинктерной диссинергии. Поражение на уровне нижнегрудного и верхнепоясничного отделов позвоночника, вовлекающее симпатические регулирующие структуры, вызывает нарушение сократительной способности внутреннего сфинктера уретры и недержание мочи. Травма спинного мозга на уровне шейного и верхнегрудного отделов позвоночника ведет к прерыванию взаимосвязи спинальных и стволовых, а также кортикальных структур регуляции. В ситуации, когда центры иннервации спинного мозга и нервные проводники между ними сохраняют свою анатомическую целостность, клинически может сформироваться автономный процесс мочеиспускания, а также гиперактивность мочевого пузыря. В этом случае накопление и выделение мочи происходят рефлекторно, в т. ч. с участием аксон-рефлексов, без контроля центров, отвечающих за произвольную составляющую физиологического процесса [7].
Описанные клинические нарушения достаточно вариабельны и зависят от характера и тяжести повреждения, а также сроков, прошедших с момента травмы, поэтому можно наблюдать переход одной формы нейрогенного расстройства мочеиспускания в другую.
Невролог, понимая обусловленность клинической картины уровнем поражения спинного мозга, определяет тактику ведения спинального пациента и дальнейший прогноз. Осуществление адекватной коррекции урологических осложнений лежит, несомненно, в междисциплинарной плоскости. В связи с этим нейроурологическая практика, а вернее, четкое и скоординированное взаимодействие невролога и уролога способно обеспечить квалифицированную и своевременную помощь. И если врач-невролог сосредоточен на повреждении спинного мозга и нарушении иннервации, то уролог контролирует непосредственное функциональное состояние нижних мочевых путей и коррекцию сопутствующих воспалительных и нефротических осложнений. Отсюда вытекает необходимость тесной взаимосвязи специалистов для полноценной коррекции нейрогенных расстройств мочеиспускания.
В представлении уролога, оказывающего специализированную помощь пациентам с неврологическими расстройствами, процесс мочеиспускания выглядит несколько сложнее, чем простой циклический акт, состоящий из чередования фаз накопления и выведения мочи, обеспеченный двумя основными функциями мочевого пузыря: резервуарной и эвакуаторной. Функционально этот процесс определяется синергией детрузора с гладкомышечным сфинктером уретры и мышцами тазового дна, включающими наружный уретральный сфинктер.
Физиологически мочевой пузырь, природой созданный резервуар для сбора мочи, обладает способностью к полному опорожнению в подходящее время и в удобном для совершения акта мочеиспускания месте согласно социально-поведенческим нормам. Эта крайне важная способность реализуется в результате сложной регуляции с участием центральной и периферической нервных систем. Фундаментально акт мочеиспускания – это спинальный рефлекс, обеспечиваемый работой центров головного мозга, реализация и подавление этого рефлекса находятся под волевым контролем. Возможность произвольного управления делает функцию нижних мочевых путей уникальной по сравнению, например, с сердечно-сосудистой системой, и в то же время более уязвимой при неврологических заболеваниях [8]. Таким образом, основными функциями нижних мочевых путей являются накопление мочи в мочевом пузыре, длящееся относительно продолжительное время, и мочеиспускание, занимающее в норме несколько секунд. Реципрокные отношения – расслабление/напряжение детрузора, закрытие уретрального сфинктера и сокращение/расслабление детрузора, открытие уретрального сфинктера – обеспечивают скоординированность процессов накопления и удаления мочи и находятся под нейромедиаторным контролем [9].
Нейрогенная дисфункция нижних мочевых путей является следствием патологии центральной нервной системы или периферических нервных окончаний ‒ отделов нервной системы, выполняющих контроль над актом мочеиспускания. В этом состоит главное отличие рассматриваемого нарушения от нарушений нижних мочевых путей ненейрогенной этиологии, развивающихся вследствие поражения непосредственно мочеполовой системы.
В урологическом сообществе длительное время основной опорой для определения формы нейрогенного расстройства мочеиспускания являлась классификация, предложенная профессором Г. Мадерсбахером в 1980 г. и рекомендуемая Европейской ассоциацией урологов (рис. 1) [10]. В ней автор выделяет 8 основных форм нейрогенных расстройств мочеиспускания в зависимости от состояния детрузора и внутреннего сфинктера уретры. Подразумевается, что указанные структуры могут быть в гипертонусе, гипотонусе и в нормальном состоянии. Однако сложность в постановке диагноза и категоричность в выборе одной из 8 форм нарушений мочеиспускания сегодня заставляют говорить о пересмотре форм расстройств мочеиспускания. С клинической точки зрения все возможные виды нарушений мочеиспускания рассмотреть в рамках одной из существующих классификаций невозможно. В определении поражения у пациента наиболее часто специалисты основываются на преобладающем нарушении эвакуаторной или резервуарной функции мочевого пузыря, различных видах детрузорно-сфинктерной диссинергии и уродинамических показателях максимального детрузорного давления в точке утечки. При этом важность знания о максимальном детрузорном давлении и максимальном давлении в точке утечки делает необходимым проведение специализированного уродинамического исследования практически каждому пациенту с нарушениями мочеиспускания на фоне неврологического заболевания.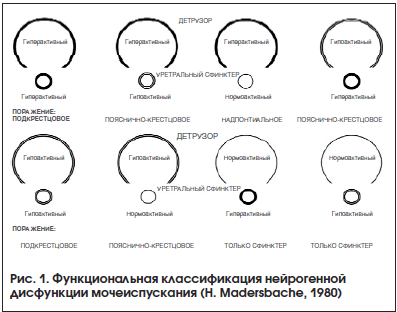
Лечение
Основными задачами урологической помощи на всех этапах нейрореабилитации являются:
1) сохранение и обеспечение функции верхних мочевыводящих путей;
2) независимость регуляции функции нижних мочевыводящих путей;
3) улучшение качества жизни.
С практической точки зрения важны борьба с вторичными осложнениями нейрогенной дисфункции мочеиспускания, а также их профилактика. К таким осложнениям относятся манифестация инфекции мочевыводящих путей (исключая бессимптомную бактериурию), уролитиаз, микроцистис, гидронефротическая трансформация и почечная недостаточность, стриктура уретры и т. д. [11].
Наименьшего риска осложнений со стороны верхних мочевыводящих путей следует ожидать при сохранении резервуарной функции мочевого пузыря с низким внутрипузырным давлением, например при гипотонии детрузора, его достаточной функциональной емкости и нормальном состоянии поперечно-полосатого сфинктера уретры или его гипотонии. В этом случае к хорошим результатам коррекции, в т. ч. улучшению качества жизни спинального пациента, приводит адекватное дренирование нижних мочевых путей, при этом следует руководствоваться международными стандартами и отечественными клиническими рекомендациями. При нарушении функции опорожнения мочевого пузыря вследствие повреждения позвоночника и спинного мозга методом выбора является асептическая периодическая катетеризация. Она подразумевает использование одноразового стерильного лубрицированного катетера. Процедура выполняется самостоятельно или с посторонней помощью каждые 4‒6 ч [12].
Иные методы дренирования мочевого пузыря, такие как приемы Креде или Вальсальвы, длительное использование постоянного мочевого катетера, должны быть строго обоснованы, т. к. несут значительные риски развития вторичных нейрогенных осложнений работы мочевого пузыря, достигающих 34% [13].
Периодическая катетеризация 4‒6 раз в сутки при условии отсутствия выраженных нарушений со стороны верхних мочевыводящих путей, шокового состояния, гнойно-инфекционных процессов в уретре и мочевом пузыре может быть назначена любым специалистом, курирующим пациента. Вопрос о том, когда переводить пациента на периодическую катетеризацию для постоянного уретрального дренажа, находится в стадии обсуждения сообщества специалистов по нейроурологии [14]. Формальных ограничений и четких рекомендаций по срокам нет, однако считается, что при отсутствии противопоказаний и достаточной укомплектованности отделения средним и младшим медицинским персоналом следует избавлять пациента от постоянных дренажей как можно раньше.
Гиперактивный мочевой пузырь, встречающийся на фоне детрузорно-сфинктерной диссинергии и без нее, является другой формой нейрогенного расстройства мочеиспускания вследствие травмы позвоночника и спинного мозга. Если такой тип нарушения клинически проявляется недержанием мочи, то он не несет значительного риска осложнений со стороны верхних мочевыводящих путей. К проблемам нейрогенного гиперактивного мочевого пузыря следует отнести снижение качества жизни.
Детрузорно-сфинктерная диссинергия характеризуется тем, что в момент напряжения мочевого пузыря для его опорожнения происходят различные по силе и продолжительности сокращения внутреннего и наружного сфинктеров уретры, обеспечивающих функцию удержания. В норме сокращения детрузора синхронны с расслаблением этих сфинктеров, что способствует свободному выведению мочи по уретре. Нарушение функции опорожнения в сочетании с высоким внутрипузырным давлением ‒ наиболее опасная форма нейрогенной дисфункции мочеиспускания из-за развития пузырно-мочеточникового рефлюкса, а также возможности структурных повреждений самого мочевого пузыря. В этом случае перед урологом стоят две основные задачи: 1) подавление высокого внутрипузырного давления, 2) обеспечение оттока мочи по уретре.
Для подавления детрузорной гиперактивности в качестве первой линии терапии применяются антихолинергические средства, в дополнение к которым можно назначать препараты из группы бета-3-адреномиметиков [15]. Вторая линия лечения включает инъекционное введение в стенку мочевого пузыря 200 ЕД ботулинического нейропептида. Надо понимать, что терапия направлена на создание низкого внутрипузырного давления в мочевом пузыре, необходимого для нормальной работы верхних мочевых путей. Одним из результатов купирования гиперактивности, особенно при сохранении нормального или повышенного тонуса поперечно-полосатого сфинктера уретры, будет увеличение количества остаточной мочи или отсутствие мочевыделения. Поэтому крайне важно объяснить пациенту необходимость проведения указанной терапии с назначением периодической катетеризации мочевого пузыря.
При своевременной коррекции нарушений мочеиспускания у спинальных пациентов, применении рекомендованного метода отведения мочи, компенсации избыточного внутрипузырного давления вследствие гиперактивности детрузора или детрузорно-сфинктерной диссинергии удается избежать многих вторичных осложнений.
В комплексной программе реабилитационного лечения пациентов с травмой позвоночника и спинного мозга используются методики немедикаментозной коррекции, показавшие различный терапевтический потенциал в ходе исследований. В частности, применение электростимуляции мочевого пузыря с помощью имплантируемых электродов в работе А.В. Лившица и соавт. показало, что создать управляемый акт мочеиспускания невозможно, т. к. возбуждение детрузора распространяется на внутренний сфинктер уретры, моделируя детрузорно-сфинктерную диссинергию [16]. Несмотря на то что исследователи представили некоторые положительные результаты, методика не нашла клинического применения в связи с высокой инвазивностью и риском вторичных осложнений.
Применение электростимуляции переменным пульсирующим током по лонно-сакральной методике и электрофореза с прозерином на передней брюшной стенке в проекции мочевого пузыря в настоящий момент представляется несостоятельным вследствие особенностей физиологии нижних мочевых путей и неучастия мышц живота в акте мочеиспускания.
Перспективно использование современных методик: сакральной инвазивной электронейростимуляции с помощью имплантируемых электродов и ритмической периферической магнитной стимуляции в области сакрального центра мочеиспускания и крестцовых корешков [17, 18]. В настоящее время механизм действия магнитной стимуляции на физиологию нижних мочевых путей остается неясным. Многоступенчатость и сложность нервной регуляции процесса удержания мочи и акта мочеиспускания предполагают возможность вовлечения различных структур в ответ на внешнее воздействие. Клинические и уродинамические эффекты магнитной стимуляции, вероятно, связаны с восстановлением интеграции регуляторных рефлексов, при этом наблюдается эффект нейромодуляции, когда происходит изменение активности (торможение или возбуждение) структур центральной, периферической и вегетативной нервных систем [19, 20].
Нейрогенное нарушение мочеиспускания, обусловленное травмой позвоночника и спинного мозга, клинически чрезвычайно гетерогенно вследствие вариабельности уровня и степени тяжести поражения [21, 22]. Этот аспект диктует необходимость индивидуального диагностического подхода, выбора адекватного метода коррекции работы нижних мочевых путей. Реабилитационный путь спинального пациента в настоящее время невозможно представить без тесного сотрудничества невролога и уролога. Совместный современный подход специалистов к проблеме урологических осложнений травмы спинного мозга обеспечивает пациенту верное понимание собственного состояния и адекватную прогностическую оценку, а также возможность социальной адаптации и повышения качества жизни [23, 24].
Источник
