Метафилактика мочекаменной болезни саенко
- Архив журнала
/ - 2018
/ - №4
Метафилактика мочекаменной болезни. Часть 1. Факторы роста заболеваемости мочекаменной болезнью. Современный взгляд на механизмы камнеобразования
DOI: https://dx.doi.org/10.18565/urology.2018.4.161-169
В.С. Саенко, М.А. Газимиев, С.В. Песегов, Ю.Г. Аляев
Мочекаменная болезнь – одно из наиболее активно прогрессирующих заболеваний, являющихся болезнью обмена веществ на фоне воздействия генетических, экологических факторов и образа жизни. В первой части представлены современные взгляды на факторы инициации образования камней и теории камнеобразования. Обсуждены факторы, играющие важную роль в активации и ингибировании процессов нуклеации и агрегации камнеобразующих веществ.
Литература
1. Fisang С., Anding R., Lats S., Laude N. Dtsch Arztebl Int. 2015;112:83–91.
2. Pearle M.S. Prevention of nephrolithiasis. Curr Opin Nephrol Hypertens 2001;10:203–209.
3. Pearle M.S., Calhoun E.A., Curhan G.C. Urologic Diseases of America Project. Urologic diseases in America project: urolithiasis. J Urol. 2005;173:848–857.
4. Sorokin I., Mamoulakis C., Miyazawa K., Rodgers A., Talati J., Lotan Y. Epidemiology of stone disease across the world. World J Urol. 2017;35(9):1301–1320.
5. Aleksandrov V.P., Tiktinskii O.L. et al. Features of stone formation in the kidneys in patients in families burdened with urolithiasis. Urologiya i nefrologiya. 1993;3:16–19. Russian (Александров В.П., Тиктинский О.Л. и соавт. Особенности камнеобразования в почках у больных в семьях, отягощенных уролитиазом. Урология и нефрология. 1993;3:16–19).
6. Tiktinskii O.L., Aleksandrov V.P. Urolithiasis. SPb. «Piter», 2000. s. 384. Russian (Тиктинский О.Л., Александров В.П. Мочекаменная болезнь. СПб. «Питер», 2000. С. 384).
7. Voshchula I.V. Urolithiasis. Etiotropic and pathogenetic treatment, prevention. Minsk. 2006. Russian (Вощула И.В. Мочекаменная болезнь. Этиотропное и патогенетическое лечение, профилактика. Минск. 2006).
8. Dzhavad-zade S.M. Urolithiasis in the endemic region: etiopathogenesis, clinic, treatment. Dr.Med.Sci. Thesis. M., 1997. Russian (Джавад-заде С.М. мочекаменная болезнь в эндемическом регионе: этиопатогенез, клиника, лечение. Дисс. докт. мед наук. М., 1997).
9. Dzhavad-zade S.M. Modern view on the pathogenesis, course and treatment of urolithiasis. Urologiia. 1999;5:10–12. Russian (Джавад-заде С.М. Современный взгляд на патогенез, течение и лечение мочекаменной болезни. Урология. 1999;5:10–12).
10. Voshchula V.I., Nitkin D.M. Metabolic disorders in urolithiasis. Uchebno-metodicheskoe posobie. Minsk. BelMAPO, 2004. S. 28. Russian (Вощула В.И., Ниткин Д.М. Метаболические нарушения при мочекаменной болезни. Учебно-методическое пособие. Минск. БелМАПО, 2004. С. 28).
11. Gres’ A.A., Voshchula V.I., Nitkin D.M., rybina I.L. Study of biochemical indicators of urine in healthy individuals. Aktual’nye voprosy urologii: tezisy dokl. 6-go belor-pol’skogo simp. Minsk, 2003. S. 19–21. Russian (Гресь А.А., Вощула В.И., Ниткин Д.М., Рыбина И.Л. изучение биохимических показателей мочи у здоровых лиц. Актуальные вопросы урологии: тезисы докл. 6-го белор-польского симп. Минск, 2003. С. 19–21).
12. Daudon M., Doré J.-C., Jungers P., Lacour B. Changes in stone composition according to age and gender of patients: a multivariate epidemiological approach. Urol. Res. 2004;32:241–247.
13. Pearle M.S., Calhoun E.A., Curhan G.C. Urologic Diseases of America Project. Urologic diseases in America project: urolithiasis. J Urol. 2005;173:848–57.
14. Daudon M., Doré J.-C., Jungers P., Lacour B. Changes in stone composition according to age and gender of patients: a multivariate epidemiological approach. Urol. Res. 2004;32:241–247.
15. Adair L.S., Popkin B.M. Are child eating patterns being transformed globally? Obes Res. 2005;13:1281–1299.
16. DeMaria E.J. Bariatric surgery for morbid obesity. N Engl J Med. 2007;356:2176–2183.
17. Konstantinova O.V. Prediction and principles of prevention of urolithiasis. Dr.Med.Sci. Thesis. M., 1999. Russian (Константинова О.В. Прогнозирование и принципы профилактики мочекаменной болезни. Дисс. докт. мед. наук. М., 1999).
18. Dzeranov N.K. Treatment of urolithiasis – a comprehensive medical problem. Quality of life. Meditsina. 2005;2(9):3–8. Russian (Дзеранов Н.К. Лечение мочекаменной болезни – комплексная медицинская проблема. Качество жизни. Медицина. 2005;2(9):3–8).
19. Katkova V.N. Urinary stones: mineralogy and genesis. Syktyvkar: Komi nauchnyi tsentr UrO RAN. 1996. Russian (Каткова В.Н. Мочевые камни: минералогия и генезис. Сыктывкар: Коми научный центр УрО РАН. 1996).
20. Kok D.J. Clinical implications of physicochemistry of stone formation. Endocr Metab Clin N Am. 2002;31:855–867.
21. Hess B., Kok D.J. Nucleation, growth and aggregation of stone forming crystals. In: Coe FL, Favus M, Pak CYC, Parks J, Preminger G, editors. Chapter 1: kidney stones: medical and surgical management. Raven Press. 1995:3–32.
22. Pak C.Y.C. Calcium Urolithiasis: Pathogenesis, Diagnosis, and Management. New York and London. Plenum Medical Book Company. 1978. Р. 162.
23. Abraham P.A., Smith Ch.L. Medical Evaluation and Management of Calcium Nephrolithiasis. Med. Clin. North. Am. 1984;68(2):281–299.
24. Buck A.C. Risk factors in idiopatic stone disease. Scientific Foundation of Urology: 3 ed. Eds. L.D. Chisholm, W.R. Fair. Oxford, Chicago, 1990. P. 176–192.
25. Andriani R.T., Carson C.C. Urolithiasis. Clin. Symposia.1986;38(3):5–25. Someren A. Urologic Pathology with Clinical and Cardiologic Corrections. New York, Toronto, London, 1989.
26. Jones W.F., Waterhouse R.L., Resnick M.I. The evaluation of urinary protein pattern in a stone – forming animal model using two dimensional polyacrylamide gel electrophoresis. J Urol. 1991;145(4):868–874.
27. Hess B. Neue pathophysiologische Aspecte der Nephrolithiasis. Schwez. Med. Wsch. 1989;119(26):929–934.
28. Nancollas G.H., Smesko S.A., Campbello A.A., Richardson C.F., Johansson M., Iadiccico P.A., Binetto J.P., Binetto M. Physical chemical studies of calcium oxalate crystallization. Am. J. Kidney Dis. 1991;17(4):392–395.
29. Litvitskii P.F. Pathophysiology: Textbook: in 2 volumes. M.:GEOTAR-MED, 2002. 365 p. Russian (Литвицкий П.Ф. Патофизиология: Учебник: в 2 томах. М.:ГЭОТАР-МЕД, 2002. 365 с.).
30. Rendall A. The origin and growth of renal calculi. Ann Surg. 1937;105:1009–1027.
31. Randall A. Papillary pathology as a precursor of primary renal calculus. J Urol. 1940;44:580.
32. Randall A. The etiology of primary renal calculus. International Abstract of Surgery. 1940;71:209.
33. Evan A.P., Lingerman J.E., Coe F.L. et al. Renall’s plaque of patients with nephrolithiasis begins in basement membranes of thin loops of Henle. J. Clin. Invest. 2003;111:607–616.
34. Evan A., Lingeman J., Coe F.L., Worcester E. Randall’s plaque: pathogenesis and role in calcium oxalate nephrolithiasis. Kidney Int. 2006;69:1313–1318.
35. Kim S.C., Coe F.L., Tinmouth W.W. et al. Stone formation is proportional to papillary surface coverage be rendall’s plaque. J Urol. 2005;173:117–119.
36. Matlaga Br, Williams Jr Jc, Kim S.C. et al. Еndoscopic evidence of cflculi attachment to Rendall’s plaque L. Urol 2006;175:1720–1774.
37. Williams Jr Jc, Matlaga Br, Kim SC et al. Calcium oxalate calculi found attached to the renal papilla: preliminary for early mechanisms in stone formation. J Endourol. 2006;20:885–890.
38. Evan A.P., Lingerman J.E., Coe F.L., Worcester E.M. Role of interstitial apapite plaque in the pathogenesis of the common calcium oxalate stone. Semin Nephrol. 2008;28:111–119.
39. Evan A.P., Worcester E.M., Coe F.L., Williams J.Jr., Lingeman J.E. Mechanisms of human kidney stone formation. Urolithiasis. 2015,43(suppl.1):19–32.
40. Evan A.P., Coe F.L., Lingeman, J.E., Shao Y., Sommer A.J., Bledsoe S.B., Anderson J.C., Worcester E.M. Mechanism of formation of human calcium oxalate renal stones on Randall’s plaque. Anat. Rec. 2007;290:1315–1323.
41. Kidney stones Nature Reviews Disease Primers 2, Article number: 16008 (2016) Doi:10.1038/nrdp.2016.8.
42. Finlayson B., Reid F. The expectation of free and fixed particles in urinary stone disease. Invest. Urol. 1978;15:442–448.
43. Kok D.J., Khan S.R. Calcium oxalate nephrolithiasis, a free or fixed particle disease. Kidney Int. 1994;46:847–854.
44. Khan S.R. Experimental calcium oxalate nephrolithiasis and the formation of human urinary stones. Scanning Microsc. 1995;9:89–100.
45. Khan S.R., Canales B.K. Unified theory on the pathogenesis of Randall’s plaques and plugs. Urolithiasis. 2015;43(Suppl. 1):109–123.
46. Khan S.R., Canales B.K. Unified theory on the pathogenesis of Randall’s plaques and plugs. Urolithiasis. 2015;43(Suppl. 1):109–123.
47. Khan S.R., Rodriguez D.E., Gower L.B., Monga M. Association of Randall plaque with collagen fibers and membrane vesicles. J. Urol. 2012;187:1094–1100.
48. Bird V.Y., Khan S.R. How do stones form? Is unification of theories on stone formation possible? Arch Esp Urol. 2017;70(1):12–27.
49. Kaufman D.W., Kelly J.P., Curhan G.C. et al. Oxalobacter formigenes may reduce the risk of calcium oxalate kidney stones. J Am Soc Nephrol. 2008;19(6):1197–1203.
50. Tsuji H., Wang W., Sunil J. et al. Involvement of renin–angiotensin–aldosterone system in calcium oxalate crystal induced activation of NADPH oxidase and renal cell injury. World J Urol. 2016;34(1):89–95.
51. Khand F.D., Gordge M.P., Robertson W.G., Noronha-Dutra A.A., Hothersall J.S. Mitochondrial superoxide production during oxalate-mediated oxidative stress in renal epithelial cells. Free Radical Biology & Medicine. 2002;32(12):1339–1350.
52. Umekawa T., Tsuji H., Uemura H., Khan S.R. Superoxide from NADPH oxidase as second messenger for the expression of osteopontin and monocyte chemoattractant protein-1 in renal epithelial cells exposed to calcium oxalate crystals. BJU International. 2009;104(1):115–120.
53. Khan S.R., Khan A., Byer K.J. Temporal changes in the expression of mRNA of NADPH oxidase subunits in renal epithelial cells exposed to oxalate or calcium oxalate crystals, Nephrology Dialysis Transplantation. 2001;26(6):1778–1785.
54. Joshi S., Peck A.B., Khan S.R. NADPH oxidase as a therapeutic target for oxalate induced injury in kidneys. Oxidative Medicine and Cellular Longevity. 2013;2013:18.
55. Cao L.-C., Honeyman T.W., Cooney R., Kennington L., Scheid C.R., Jonassen J.A. Mitochondrial dysfunction is a primary event in renal cell oxalate toxicity. Kidney International. 2004;66(5):1890–1900.
56. Khan S.R. Crystal/cell interaction and nephrolithiasis. Arch. Ital. Urol. Androl. 2011;83:1–5.
57. Khan S.R. Reactive oxygen species as the molecular modulators of calcium oxalate kidney stone formation: evidence from clinical and experimental investigations. J Urol. 2013;189(3):803–811.
58. Golovanov S.A., Yanenko E.K., Dzeranov N.K., Drozhzheva V.V., Beshliev D.A., Kon’kova T.A. Lipid peroxidation and antioxidant system in patients with urolithiasis after remote lithotripsy. Urologiya i nefrologiya. 1998;2:14–16. Russian (Голованов С.А., Яненко Э.К., Дзеранов Н.К., Дрожжева В.В., Бешлиев Д.А., Конькова Т.А. Липидная пероксидация и антиоксидантная система у больных мочекаменной болезнью после дистанционной литотрипсии. Урология и нефрология. 1998;2:14–16).
59. Liang Q., Li X., Zhou W., Su Y., He S., Cheng S., Lu J., Yan Y., Pei X., Qi J. et al. An Explanation of the Underlying Mechanisms for the In Vitro and In Vivo Antiurolithic Activity of Glechoma longituba. Oxid. Med. Cell. Longev. 2016, 3134919.
60. Fasano J.M., Khan S.R. Intratubular crystallization of calcium oxalate in the presence of membrane vesicles: An in vitro study. Kidney Int. 2001;59:169–178.
61. Stoller V.L., Meng M.V., Abrahams H.M., Kane J.P. The primary stone event; a new hypothesis involving a vascular etiology. J Urol. 2004;171:1920–1924.
62. Stoller M.L., Low R.K., Shami G.S. et al. High resolution radiography of cadaveric kidneys: unraveling the mystery of Randall’s plaque formation. J Urol. 1996;156:1263.
63. Sampaio F.J., Aragao A.H. Anatomical relationship between the intrarenal arteries and the kidney collecting system. J Urol. 1990;143:679–81.
64. Bushinsky D.A., Monk R.D. Electolyte quintet: calcium. Lancet. 1998;352:306–11.
65. Carr R.J. A new theory of the formation of renal calculi. Brit J Urol 26:p.105, 1954; Randall A. The origin and growth of renal calculi. Ann Surg. 1937;105:1009.
66. Robertson W.G., Peacock M., Nordin B.E. Calcium oxalate crystalluria and urine saturation in recurrent renal stone-formers. Clin. Sci. 1971;40:365–374.
67. Khan S.R., Hackett R.L. Retention of calcium oxalate crystals in renal tubules. Scanning Microsc. 1991;5:707–711.
68. Khan S.R., Finlayson B., Hackett R.L. Experimental calcium oxalate nephrolithiasis in the rat. Role of the renal papilla. Am. J. Pathol. 1982;107:59–69.
69. Grases F., Söhnel O. Can Randall’s plug composed of calcium oxalate from via the free particle mechanism? BMC Urology. 2017;17:80.
70. Finlayson B., Reid F. The expectation of free and fixed particles in urinary stone disease. Investig Urol. 1978;15:442–448.
71. Kramer G., Klingler H.C., Steiner G.E. Role of bacteria in the development of kidney stones. Curr. Opin. Urol. 2000;10(1):35–38.
72. Barannik S.V. The history of the discovery of nanobacteria. Nauki o cheloveke – Sbornik statei po materialam tret’ego kongressa molodykh uchenykh i spetsialistov. Tomsk, SGMU. 2002. Russian (Баранник С.В. История открытия нанобактерии. Науки о человеке – Сборник статей по материалам третьего конгресса молодых учёных и специалистов. Томск, СГМУ. 2002).
73. Folk R.L. SEM imaging of bacteria and nanobacteria in carbonate sediments and rocks. J Sediment Petrol. 1993:63:990.
74. Leiske J.C., Toback F.G. Renal cell-urinary crystal interaction. Curr Opin Nephrol Hypertens. 2000;9:349.
75. Martel J., Wu C.Y., Young J.D. Translocation of mineralo-organic nanoparticles from blood to urine: a new mechanism for the formation of kidney stones? Nanomedicine (Lond). 2016.
76. Evan A.P. et al. Renal intratubular crystals and hyaluronan staining occur in stone formers with bypass surgery but not with idiopathic calcium oxalate stones. Anat. Rec. (Hoboken). 2008;291:325–334.
77. Khan S.R., Gambaro G. Role of osteogenesis in the formation of Randall’s plaques. Anat. Rec. (Hoboken). 2015;299:5–7.
78. Mezzabotta F. et al. Spontaneous calcification process in primary renal cells from a medullary sponge kidney patient harbouring a GDNF mutation. J. Cell. Mol. Med. 2015;19:889–902.
79. Meyer J.L., Bergert J.H., Smith L.H. Epitaxial relationships in urolithiasis: the calcium oxalate monohydrate–hydroxyapatite system. Clin. Sci. Mol. Med. 1975;49:369–374.
80. Højgaard I., Fornander A.M., Nilsson M.A., Tiselius H.G. The effect of pH changes on the crystallization of calcium salts in solutions with an ion composition corresponding to that in the distal tubule. Urol. Res.1999;27:409–416.
81. Tiselius H.-G. A hypothesis of calcium stone formation: an interpretation of stone research during the past decades. Urol. Res. 2011;39:231–243.
82. Sethman I., Grohe B., Kleebe H.-J. Replacement of hydroxyapatite by whewellite: implications for kidney stone formation. Miner. Mag. 2014;78:91–100.
83. Baumann J.M., Affolter B. From crystalluria to kidney stones, some physicochemical aspects of calcium nephrolithiasis. World J Nephrol. 2014;3(4):256–267.
84. Saw N.K., Rao P.N., Kavanagh J.P. A nidus, crystalluria and aggregation: key ingredients for stone enlargement. Urol Res. 2008;36(1):11–15.
85. Haggitt R.C., Pitcock J.A. Renal medullary calcifications: a light and electron microscopic study. J. Urol. 1971;106:342–347.
Об авторах / Для корреспонденции
А в т о р д л я с в я з и: В. С. Саенко – д.м.н., профессор кафедры урологии ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» (Сеченовский Университет), Москва, Россия; e-mail: Saenko_vs@mail.ru
Похожие статьи
- Генетические аспекты первичной гипероксалурии: эпидемиология, этиология, патогенез и клинические проявления заболевания
- Мультиперкутанная нефролитотомия в лечении коралловидных камней почек
- Оценка влияния качества и микроэлементного состава питьевой воды на заболеваемость мочекаменной болезнью в различных регионах Дагестана
- Метафилактика мочекаменной болезни. Часть 2. Факторы роста заболеваемости МКБ. Современный взгляд на механизмы камнеобразования (продолжение)
- Дисциркуляторные изменения в паренхиме почек больных мочекаменной болезнью после различных методов хирургического лечения
Источник

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Существующие методы оперативного лечения, включая хирургический, дают возможность получить лишь относительный эффект в лечении мочекаменной болезни (МКБ), но не позволяют остановить процесс камнеобразования. По мнению М.М. Газымова (2003) в ближайшие 3 года после удаления (отхождения) конкрементов частота рецидивов доходит до 30%. R. Kocvara и др. (1999, 2000) отмечают, что после первого эпизода спорадического отхождения конкремента из почки вероятность его рецидива в течение последующих 5 лет составляет от 27 до 50%.
Значительное количество резидуальных камней/фрагментов в мочевых путях, особенно после дистанционной литотрипсии (ДЛТ), степень выраженности хронического воспалительного процесса в мочевых путях требует проведения соответствующего лечения и контроля его эффективности. В связи с этим особую значимость приобретает актуальность амбулаторного динамического наблюдения, преследующего цели профилактики обострения хронического пиелонефрита, подбора и проведения литокинетической и литолитической терапии, метафилактики рецидивного камнеобразования.
Материалы и методы
Метафилактика (от лат. meta – после, за чем-либо и filasso – сторожить), подразумевает комплекс мероприятий общеоздоровительного характера и медикаментозного лечения, направленных на предотвращение рецидивного камнеобразования. Метафилактика больных мочекаменной болезнью после различных видов оперативного лечения начинается со дня выписки пациента из стационара и заканчивается последним днем его жизни. Ее необходимо разделить на период раннего амбулаторного послеоперационного ведения и период динамической метафилактики мочекаменной болезни. Это деление определяется задачами, которые предстоит решать на каждом этапе наблюдения.
Подход к периоду раннего амбулаторного наблюдения по нашему мнению принципиально не зависит от метода проведенного оперативного лечения. В этот период особое значение приобретает задача купирования и профилактики обострения хронического пиелонефрита, улучшения уро- и гемодинамики почек, подбора и проведения литокинетической терапии. По данным Ю.Г. Аляева и др. (2001) к моменту выписки из стационара полное отхождение фрагментов камня после дистанционной литотрипсии отмечено лишь у 28,1% больных.
По нашему мнению первое знакомство врача с пациентом после оперативного лечения должно включать ультразвуковое исследование почек и мочевых путей, которое является наиболее доступным методом исследования и динамического наблюдения. Этот метод позволяет определить наличие фрагментов камня в чашечках почки, оценить их размеры и локализацию, изменение их расположения, в динамике выявить расширение мочевых путей, обусловленное миграцией фрагментов. Своевременное получение этой информации, безусловно, необходимо для определения тактики лечения больного. Кроме рутинного ультразвукового исследования почек целесообразно при необходимости и наличии технических возможностей использовать исследование мочеточника, его интрамурального отдела через переднюю брюшную стенку ректальным датчиком. При локализации камня в предпузырном и интрамуральном отделах ультразвуковое исследование через переднюю брюшную стенку проводится при хорошо наполненном мочевом пузыре. Использование ректального датчика оказывает существенную помощь при визуализации камней в юкставезикальном и интрамуральном отделах мочеточника. Камень четко определяетсякакгиперэхогенное образование, дающее ультразвуковую тень. Нередко удается визуализировать расширение мочеточника в предпузырном отделе до камня. Для профилактики развития осложнений необходимо проводить динамический контроль расположения фрагментов разрушенного конкремента и состояния мочевых путей. Это позволяет оценить степень окклюзии мочевых путей и угрозу развития гнойных осложнений. При миграции фрагмента камня в мочеточник определение анатомических и функциональных изменений в верхних мочевых путях имеет решающее значение в определении показаний к выбору метода лечения. Выявление сохраненной сократительной способности мочевых путей позволяет проводить консервативную терапию с применением спазмолитиков, диуретиков, физиотерапии, водных нагрузок. Снижение же сократительной способности мочевых путей является показанием к оперативным методам лечения. Кроме того, оценка локализации камня в мочеточнике и состояние мочевых путей имеет неоспоримое значение не только для определения показаний к проведению физиотерапевтических процедур, направленных на изгнание камня, но и в динамике проведения физиотерапевтических процедур для коррекции положения электродов на теле больного.
Не меньшее значение ультразвуковое исследование имеет в период динамической метафилактики мочекаменной болезни. Мы считаем показанным контрольные ультразвуковые исследования каждые 3-4 мес. после применения оперативных методов лечения в течение первого года наблюдения и не реже 2 раз год в последующие годы наблюдения. Камнеобразование – это результат множественных, комплексных и взаимосвязанных процессов, происходящих в почках и мочевых путях. Ведущие теории литогенеза определяют следующие факторы этого процесса:
- Концентрация в моче литогенных ионов.
- Дефицит ингибиторов кристаллизации и агрегации кристаллов.
- Присутствие в моче активаторов камнеобразования.
- Локальные изменения.
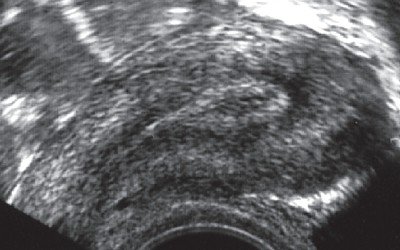
Наиболее привлекательной среди теорий, объясняющих литогенез локальными изменениями,является теория “папиллярной патологии”, предложенная А. Рендаллом в 1936 г. Он полагал, что под влиянием повреждающих причин, особенно бактериальных токсинов, в области почечного сосочка возникает выраженная тенденция к обызвествлению подслизистого слоя. Образовавшаяся известковая пластинка нарушает целостность покрывающего ее эпителия и начинает контактировать с мочой в просвете чашечки. Возникают условия для формирования чашечкового камня, покрывающего сосочек, подобно щиту. В других случаях, по мнению А. Рендалла, начало камнеобразования связано не с внутрисосочковой калъцификацией, а с осаждением солей в дистальной части собирательных трубок и их отверстий в решетчатой мембране. Любое вещество при значительной кристаллурии и нарушении внутрипочечного транспорта мочи может положить начало образованию ядра, прикрепляющегося по типу пробки к отверстию собирательной трубки. Подтверждением данной теории могут служить данные ультразвукового исследования и эндоскопическая картина, нередко выявляемая при осмотре области почечного сосочка. При ультразвуковом исследовании в проекции чашечки выявляется гиперэхогенное образование размерами от 2 до 5 мм без четкой ультразвуковой тени, описанное как “чашечка Рендалла”. При этом над ним нередко выявляется “гипоэхогенный венчик” или жидкостное образование до 2-3 мм в диаметре (рис. 1).

Рис. 1. Ультрасонограмма гиперэхогенного образования в проекции средней чашечки без четкой УЗ-тени. Над ним определяется “гипоэхогенный венчик”.
При эндоскопическом исследовании возможно выявление конкремента, расположенного под слизистой свода чашечки (рис. 2).
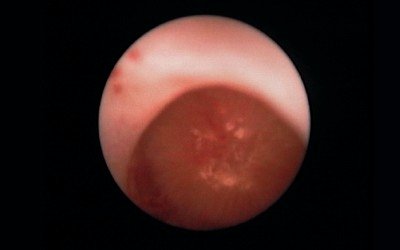
Рис. 2. При эндоскопическом исследовании визуализируется конкремент, расположенный под слизистой свода чашечки.
Подобные изменения требуют ультразвукового динамического контроля, так как проведение литоизгоняющей терапии при наличии “чашечки Рендалла” бесперспективно, а при наличии камня целесообразно.
Наиболее часто диагностические ошибки в ходе ультразвукового исследования встречаются при дифференциальной диагностике “чашечки Рендалла” и мелких конкрементов/фрагментов в чашечно-лоханочной системе. Это обусловлено тем, что их эхографические признаки по плотности приближаются к изображению чашечных структур и почечного синуса. Поэтому камни, толщина которых менее 5 мм, нередко остаются нераспознанными. Кроме того, определенные трудности представляет диагностика уратных камней небольшого размера, особенно когда камень плоской формы и имеются некротические массы в чашечно-лоханочной системе, которые характеризуются повышенной эхоплотностью и дают акустическую тень. С целью уменьшения диагностических ошибок при ультразвуковомисследованиипоповоду диагностики рецидивного камнеобразования и динамическом наблюдении после оперативных вмешательств по поводу мочекаменной болезни необходимо строгое соблюдение методологических принципов проведения исследования:
- Сканирование необходимо осуществлять в нескольких проекциях при различных углах наклона датчика и разных положениях больного.
- Использовать фармакоультразвуковое исследование для выявления мелких камней.
При проведении дифференциальной диагностики “чашечки Рендалла” и мелкого камня в проекции чашечно-лоханочной системы проводилось фармакоультразвуковое исследование почек на фоне искусственной полиурии. Применяемая методика создает оптимальные условия для выявления конкрементов. На фоне дилатированнои чашечно-лоханочнои системы мелкие конкременты могут менять свое положение, хорошо визуализируются, нередко удается определить акустическую дорожку.
Выводы
Таким образом, динамическое ультразвуковое исследование в периоды раннего амбулаторного послеоперационного наблюдения и динамической метафилактики больного с мочекаменной болезнью создает условия для оценки степени освобождения мочевых путей от фрагментов камня, эффективного контроля метафилактики мочекаменной болезни и раннего выявления рецидива камнеобразования.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Источник
