Как проводят лучевую мочевого пузыря
Лучевой цистит – это реакция тканей мочевого пузыря на ионизирующее облучение, проводимое в рамках лечения злокачественных опухолей малого таза. Симптомы зависят от полученной лучевой нагрузки, варьируются от незначительного дискомфорта при мочеиспускании, частых позывов и микрогематурии до выраженных болей, появления рецидивирующего кровотечения, угрожающего жизни. Диагноз подтверждают с помощью общего анализа мочи, цистоскопии. Лечение пострадиационного цистита определяется степенью выраженности поражения, может быть консервативным или оперативным с выполнением цистэктомии, решением вопроса с отведением мочи.
Общие сведения
Лучевой цистит регистрируют у 5-21% пациентов как осложнение лучевой терапии. Наиболее часто симптомы появляются после лечения рака мочевого пузыря (18%), простаты (14%), шейки матки (5%). Патология развивается в среднем через 32 недели после лечения, у мужчин чаще, чем у женщин (2,8:1). Конформная лучевая терапия, брахитерапия сопряжены с меньшей вероятностью возникновения пострадиационного цистита по сравнению с обычной. Но даже при таком лечении случайное облучение близлежащих тканей неизбежно из-за проникновения новообразования в окружающие органы или из-за близости рака к соседним структурам таза.
Лучевой цистит
Причины
Во время лучевой терапии происходит передача энергии ионизирующего излучения молекулам опухолевых клеток и тканям соседних органов, в частности – мочевому пузырю, прямой кишке. В результате альтерации нарушается трофика, кровоснабжение, позднее развиваются фиброзно-склерозирующие изменения. Пострадиационный цистит вызывает прохождение лучевой терапии по поводу опухолей:
- предстательной железы;
- влагалища, матки, ее шейки, яичников;
- мочевого пузыря;
- толстой, прямой кишки.
Определенное значение имеют локализация новообразования, стадия болезни, ежедневная и суммарная доза облучения (количество сеансов), тип лучевой терапии. К способствующим циститу факторам относятся:
- общее снижение иммунной реактивности организма на фоне злокачественного новообразования;
- выполненное оперативное вмешательство, например, трансуретральная резекция (ТУР) простаты или стенки пузыря с опухолью;
- одновременное прохождение химиотерапии;
- урологические заболевания: сопутствующий воспалительный процесс, цистолитиаз, дивертикулы;
- патологии, предрасполагающие к плохому заживлению, локальной ишемии: СПИД, сахарный диабет, болезни сосудов;
- ожирение (ИМТ >30 кг/м2);
- проведение гормонального лечения по поводу рака простаты;
- хроническая никотиновая интоксикация (≥1 пачки в день).
Патогенез
Радиация взаимодействует с внутриклеточной жидкостью, в результате высвобождаются свободные радикалы, нарушающие синтез ДНК, что приводит к гибели клеток. На фоне терапии повреждаются мембраны как раковых, так и здоровых клеток, изменения затрагивают сосуды. Субэндотелиальная пролиферация, отек постепенно истощают кровоснабжение облученной зоны. Неоваскуляризация, неадекватная регенерация провоцируют формирование хрупких поверхностных сосудов, ответственных за макрогематурию при геморрагическом цистите.
Отложение коллагена запускает процессы рубцевания, способствует дальнейшей облитерации кровеносных сосудов, вследствие чего развивается гипоксия, некроз. В мочевом пузыре на фоне ишемии слизистой оболочки повреждается уротелий, что вызывает подслизистый фиброз, поскольку субэпителиальные ткани подвергаются едкому воздействию мочи. Образование язв, поражение нервов, пострадиационный фиброз обеспечивают появление развернутой клинической симптоматики.
Классификация
Лучевой цистит может быть ранним, возникающим в течение 4 недель или 6-12 месяцев после терапии, и поздним, с появлением симптомов спустя год или позже. Выделяют острое и хроническое течение пострадиационного воспаления. Специалисты в сфере онкоурологии используют в работе специальную шкалу для оценки степени выраженности изменений мочевого пузыря, подвергшегося лучевому воздействию:
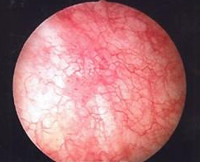
- 1 степень подразумевает незначительную эпителиальную атрофию и расширение сосудов, обнаружение единичных эритроцитов в моче. Клинические проявления чаще отсутствуют.
- 2 степень характеризуется обнаружением множественных телеангиэктазий, эпизодами макрогематурии. Мочеиспускание учащено, появляются жалобы на недержание урины.
- 3 степень представлена видоизменением сосудов по всей поверхности, формированием микроциста (уменьшением емкости органа), стойким недержанием мочи, изнурительными позывами на мочевыделение до 40 эпизодов в сутки, включая ноктурию, рецидивирующей макрогематурией.
- 4 степень при цистоскопии обнаруживаются участки некротизации, признаки тотального геморрагического цистита с участками петехий, емкость пузыря при тугом наполнении менее 100 мл, отмечается полная утрата контроля над мочевыделением, требующая вспомогательных мер (катетеризации или цистэктомии). В моче постоянно присутствует кровь, белок, слущенный эпителий.
- 5 степень наиболее неблагоприятна в прогностическом плане, гематурия приводит к развитию угрожающей жизни анемии, формированию свищей. Определяется максимально выраженный болевой синдром, высокий риск летального исхода.
Симптомы лучевого цистита
Сразу или через несколько недель после одномоментного получения значительной дозы радиации развивается острый воспалительный процесс. Как правило, ранний цистит является самоограниченным, симптомы аналогичны острому инфекционному воспалению, включают рези при учащенном мочеиспускании и после, боли внизу живота, ургентные позывы на мочевыделение. Может присутствовать кровь в моче, но более типична микрогематурия. Отмечается хороший ответ на терапию.
Лучевой цистит, возникший спустя несколько месяцев либо лет после лечения, может проявляться постоянной дизурией, сильной болью, позывами к мочеиспусканию через каждые 10-15 минут из-за формирования микроциста, выделением урины с кровью, стойкой инконтиненцией. Макрогематурия приобретает рецидивирующий характер, обнаруживается значительная кровопотеря. Повышение температуры свидетельствует о вторичном бактериальном инфицировании.
Осложнения
Лучевой цистит осложняется присоединением инфекции с развитием бактериального воспалительного процесса в почках (пиелонефрит в 20%), прогрессирующим уменьшением емкости или рубцовым сморщиванием органа и неоплазией (менее 2%), образованием свища (2%), контрактуры шейки (3-5%). При выраженном пострадиационном воспалении возникает некупируемый хронический болевой синдром, значительно ухудшающий качество жизни.
Кровотечению из видоизмененных сосудов (геморрагический цистит в 3-5%) нередко сопутствует анемия, иногда частота и выраженность кровотечения настолько значительна, что требуется проведение цистэктомии, поскольку неоднократные коагуляции лишь усугубляют фиброзно-склеротический процесс. Гематурия может сопровождаться образованием сгустков, которые приводят к острой задержке мочеиспускания за счет гемотампонады уретры.
Диагностика
Прохождение лечения с использованием ионизирующего облучения с отсроченным появлением типичных жалоб – основной критерий, на основании которого врач-уролог выставляет предварительный диагноз лучевого цистита. Учитывая то, что данные симптомы могут свидетельствовать о ряде других патологических процессов, показано прохождение углубленного клинико-урологического обследования, которое включает:
- Лабораторные анализы. В ОАМ обнаруживают микро- или макрогематурию, белок, эпителий, иногда бактерии, лейкоциты. Бакпосев производят для исключения инфекции мочевыводящих путей. Цитология мочи обоснована при подозрении на рак мочевого пузыря. В результатах анализа крови обращают внимание на гемоглобин, гематокрит, уровень тромбоцитов. Коагулограмма позволяет исключить нарушения в работе свертывающей системы.
- Инструментальную диагностику. Основным исследованием является цистоскопия, которая позволяет исключить другие причины жалоб, например, камень или мочепузырную опухоль. Типичная картина – множественные телеангиэктазии на фоне отечной слизистой, на продвинутой стадии – множественные эрозии. Прочие методы визуализации (МРТ, КТ, экскреторную урографию) назначают для исключения свищей, других причин гематурии.
- Биопсию стенки пузыря. Морфологическое исследование проводят после получения неоднозначных результатов УЗИ, цистоскопии и КТ или МРТ при высокой вероятности опухолевого процесса. Перед выполнением биопсии учитывают потенциальный риск кровотечения из поверхностных сосудов в результате травматизации.
Дифференциацию осуществляют между уроцистолитиазом, распространением опухоли из малого таза в пузырь, прогрессированием рака, сопровождающегося кровотечением, болевым синдромом. КТ и МРТ становятся основными диагностическими процедурами в данной клинической ситуации.
Лечение лучевого цистита
Терапевтические мероприятия зависят от выраженности процесса, в каждом случае определяются индивидуально. Первая и вторая степени цистита после облучения требуют активной тактики только при наличии жалоб. Цистэктомия рассматривается как крайний вариант для лечения постлучевого цистита, выполняется при безуспешности консервативной терапии.
Медикаментозное лечение
Радиационно-индуцированная гематурия может быть легкой или опасной для жизни, во втором случае прибегают к реанимационным мероприятиям, переливанию компонентов крови. Перечень препаратов для лечения включает:
- антихолинергические средства;
- обезболивающие агенты;
- фибринолитики;
- лекарства, улучшающие кровообращение;
- альфа-1-адреноблокаторы.
Инстилляции в мочевой пузырь
Вливание растворов – следующий этап лечения при неэффективности пероральной терапии лучевого цистита и налаженной системы орошения. Используют следующие препараты:
- Гиалуроновая кислота. Мукополисахарид, присутствующий в соединительной и эпителиальной тканях, ингибирует образование иммунных комплексов, нейтрализует функции нейтрофилов при регуляции пролиферации фибробластов, эндотелиальных клеток. Аналогичным действием обладает хондроитин-сульфат.
- Аминокапроновая кислота. Стабилизирует процесс свертывания крови путем фибринолиза.
- Формалин. 1% раствор является тканевым фиксатором, который денатурирует поверхностный слой уротелия, обеспечивая гемостаз. Лечение сопровождается сильной болью, что требует назначения анальгетиков. Высок риск побочных эффектов.
- Соли алюминия. 1% сульфат алюминия-аммония или сульфат алюминия-калия вызывают осаждение белка на поверхности клеток и в интерстициальных пространствах, что позволяет прекратить кровоточивость.
- Плацентарный экстракт. Эффективен в эпителизации эрозий, язв.
Хирургическое лечение
Если консервативная терапия и внутрипузырные инстилляции не могут остановить кровотечение, прибегают к различным эндоскопическим или чрескожным вмешательствам. Цистоскопия с фульгурацией проблемных участков, эвакуация кровяного сгустка, выполнение электрокоагуляции являются разумными шагами в дальнейшей тактике. Виды вмешательств при лучевом цистите:
- Введение ботулинического токсина А. Препарат вводится в стенку мочевого пузыря при отсутствии эффекта от антихолинергических средств. Лечение направлено на увеличение емкости пузыря, снижение частоты мочеиспускания, купирование ургентных позывов.
- Наложение чрескожного нефростомического дренажа. Отведение мочи из ЧЛС почек способствует регенерации уротелия нижних отделов мочевого тракта. Через 3-6 месяцев восстанавливают анатомически правильный отток урины.
- Эндоскопическая склеротерапия. Введение склерозанта в кровоточащие области эффективно не в 100% случаев, но у большинства пациентов с трудноизлечимым геморрагическим циститом обеспечивает снижение выраженности симптоматики, гемостаз.
- Эмболизация сосудов. Помогает остановить кровотечение при рефрактерном пострадиационном геморрагическом цистите.
- Паллиативная цистэктомия. Органоуносящая операция показана при рецидивирующей гематурии при безуспешности всех видов лечения, формировании свища, микроцисте (объем менее 200 мл) с изнуряющими позывами на мочеиспускание, стойком болевом синдроме. Урину отводят путем создания кондуита толстой кишки или выполнения двусторонней транскутанеостомии.
Физиотерапия
Гипербарическая кислородная терапия (оксигенация) способствует нормализации ангиогенеза, мобилизации стволовых клеток, остановке кровотечения за счет активации процессов фибринолиза, разрешению ишемии. Используется как дополнительный способ лечения лучевого цистита. Проведение оксигенобаротерапии не имеет каких-либо неблагоприятных последствий.
Прогноз и профилактика
Лучевой цистит, развившийся через 4-6 недель от начала сеансов ЛТ, имеет более благоприятный прогноз. Улучшение наступает примерно через 1,5 месяца, но у 5-20% процесс переходит в стойкую форму с рецидивирующими клиническими проявлениями через несколько месяцев или даже 10-20 лет. Хронические формы менее благоприятны.
Профилактика подразумевает выбор типа лучевой терапии с максимальным воздействием на опухоль, но не на соседние ткани, выполнение инстилляций на основе гиалуроновой кислоты с превентивной целью, прием растительных диуретиков. Исследования показали уменьшение симптомов цистита при использовании добавок, содержащих клюквенный экстракт.
Источник
Рак мочевого пузыря входит в число наиболее распространенных онкологических заболеваний. В России он составляет 4,5% от всех злокачественных опухолей, ежегодно диагностируются более 10 тысяч новых случаев. Наиболее распространено заболевание среди людей старше 67 лет, мужчины болеют примерно в 4,5 раза чаще по сравнению с женщинами.
В Европейской клинике можно получить лечение при раке мочевого пузыря по современным международным стандартам. Наши врачи выполняют хирургические вмешательства любой сложности, применяют противоопухолевые препараты последнего поколения с доказанной эффективностью.
Классификация и стадии рака мочевого пузыря
Подавляющее большинство злокачественных опухолей мочевого пузыря представлено уротелиальным раком (другое название — переходно-клеточный рак). Он развивается из клеток, которые образуют слизистую оболочку органа — уротелий (переходно-клеточный эпителий). Также уротелием выстлан мочеиспускательный канал, мочеточники, почечные лоханки, поэтому здесь могут встречаться такие же опухоли.
В 1–2% случаев (по данным Американского онкологического сообщества — American Cancer Society) в мочевом пузыре встречается плоскоклеточный рак (состоит из плоских клеток, напоминающих те, что входят в состав эпидермиса кожи), в 1% случаев — аденокарциномы (злокачественные опухоли из железистых клеток), менее чем в 1% случаев — мелкоклеточный рак (из нейроэндокринных клеток). Крайне редко в мочевом пузыре обнаруживают саркомы — злокачественные опухоли из соединительной ткани.
Классификация рака мочевого пузыря по стадиям осуществляется в соответствии с общепринятой системой TNM. Буквой T обозначают характеристики первичной опухоли, N — наличие очагов поражения в регионарных лимфоузлах, M — наличие отдаленных метастазов в других органах.

В упрощенном варианте, в зависимости от характеристик T, N и M, выделяют пять основных стадий рака мочевого пузыря:
- Стадия 0 — неинвазивная карцинома, она находится только в пределах слизистой оболочки и не прорастает глубже в стенку органа. Это так называемый рак на месте. Все остальные стадии — это инвазивный рак.
- Стадия I — опухоль углубилась в стенку мочевого пузыря, но не достигла мышечного слоя (T1). Нет очагов поражения в регионарных узлах (N0) и отдаленных метастазов (M0).
- Стадия II — опухоль проросла в мышечный слой органа (T2), но не проросла сквозь него. N0, M0.
- Стадия III — злокачественная опухоль проросла сквозь стенку мочевого пузыря и распространилась на окружающую его жировую клетчатку (T3) или в соседние органы (T4a). Опухолевые клетки на этой стадии могут распространяться в регионарные лимфоузлы (N1—3), отдаленных метастазов нет (M0).
- Стадия IV — злокачественная опухоль проросла в стенку таза или живота (IVA), либо имеются метастазы в отдаленных лимфоузлах, других органах (IVB). При этом первичная опухоль может иметь любые размеры, распространяться или не распространяться в регионарные лимфатические узлы.
Методы диагностики
К сожалению, не существует эффективных методов скрининга, которые можно было бы регулярно проводить у всех людей с целью ранней диагностики рака мочевого пузыря. Симптомы заболевания неспецифичны и могут напоминать проявления других патологий, например, цистита, аденомы простаты. Из-за этого злокачественные опухоли нередко диагностируют на поздних стадиях, когда лечить их уже намного сложнее.
Важно внимательно относиться к своему здоровью, обращать внимание на любые симптомы, которые сохраняются в течение длительного времени, и при их возникновении сразу обращаться к врачу.
При подозрении на рак мочевого пузыря применяют следующие виды диагностики:
- Цитологическое исследование мочи — её изучение под микроскопом на предмет наличия опухолевых клеток. Этот анализ иногда помогает диагностировать рак на ранних стадиях, но он не идеален.
- Исследование мочи на онкомаркеры — вещества, повышение уровней которых может свидетельствовать о злокачественной опухоли. Это также не совсем надежный тест.
- Цистоскопия — эндоскопическое исследование мочевого пузыря, когда в орган вводят специальный инструмент — цистоскоп — с видеокамерой. Наиболее информативна так называемая цистоскопия с синим светом. В мочевой пузырь вводят специальный препарат, который накапливается в опухолевых клетках и заставляет их флуоресцировать («светиться») в лучах синего света.
- Биопсия — исследование, во время которого получают фрагмент патологически измененной ткани и изучают в лаборатории под микроскопом. Это самый надежный способ разобраться, присутствуют ли в патологическом образовании раковые клетки, и является ли оно злокачественным. Материал для биопсии можно получить во время цистоскопии.
- Внутривенная пиелография. Пациенту внутривенно вводят раствор рентгеноконтрастного препарата, который затем начинает выводиться почками и «прокрашивает» мочевыводящие пути на рентгеновских снимках. Это помогает обнаружить опухоли.
- Ретроградная пиелография — исследование, во время которого рентгеноконтрастный раствор вводят через катетер, установленный в мочевом пузыре или мочеточнике.
- Ультразвуковое исследование помогает оценить размеры опухоли, выяснить, не распространилась ли она за пределы мочевого пузыря, проверить состояние почек. Под контролем УЗИ в обнаруженную опухоль можно ввести иглу и провести биопсию.
- Компьютерная томография и МРТ помогают оценить размеры, расположение, количество опухолевых очагов, обнаружить распространение рака на соседние органы, в лимфатические узлы, выявить метастазы. Под контролем КТ также можно провести биопсию с помощью иглы.
- Рентгенографию применяют для поиска метастазов в легких, костях.
Лечение рака мочевого пузыря
Тактику лечения при раке мочевого пузыря составляет команда врачей, в которую входят клинические онкологи, хирурги, урологи, химиотерапевты, радиотерапевты и другие специалисты.
Как выбирают лечение при раке мочевого пузыря?
Тактика лечения рака мочевого пузыря зависит от многих факторов: стадии опухоли, ее типа и молекулярно-генетических характеристик, общего состояния здоровья пациента, его возраста, наличия у него сопутствующих заболеваний. Прибегают к различным видам хирургических вмешательств, пациенту может быть назначена лучевая терапия, химиотерапия, иммунотерапия (в том числе введение препаратов внутрь мочевого пузыря).
Хирургическое лечение
В большинстве случаев злокачественную опухоль мочевого пузыря удается удалить хирургически. Есть разные виды операций, врач выбирает подходящую, в зависимости от стадии рака.
Иногда можно прибегнуть к трансуретральной резекции опухоли. Во время этого вмешательства не нужно делать разрез. Через мочеиспускательный канал (чаще всего пациент находится под общим наркозом) вводят специальный инструмент — резектоскоп. Он представляет собой петлю, которую накидывают на опухоль и отсекают ее. Для того чтобы уничтожить оставшиеся раковые клетки, прибегают к фульгурации (прижиганию током высокой частоты) или используют лазер.
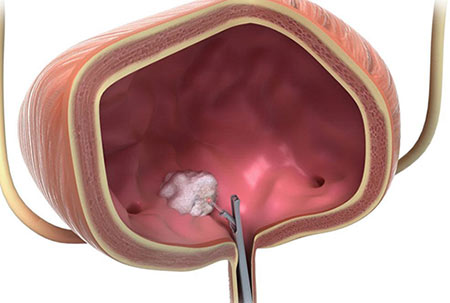
Трансуретральная резекция для лечения рака мочевого пузыря показана в двух случаях:
- Для того чтобы удалить поверхностно расположенные опухоли на ранних стадиях.
- Для того чтобы диагностировать рак, разобраться, насколько глубоко он прорастает в стенку мочевого пузыря.
Если опухоль проросла в мышечный слой стенки органа, но имеет небольшие размеры, можно выполнить резекцию — удалить только часть мочевого пузыря. На оставшуюся часть накладывают швы, и она продолжает выполнять свои функции, но в ней не может поместиться прежний объем мочи, и человеку приходится чаще посещать туалет. У резекции есть один большой недостаток: высок риск рецидива.
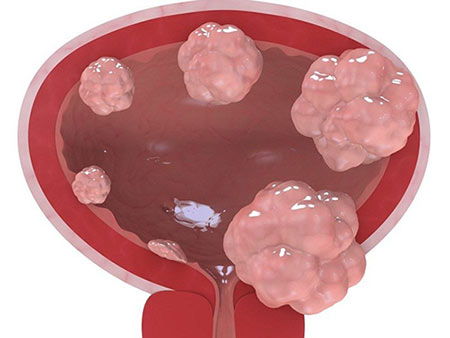
Большинству больных приходится выполнять цистэктомию — полностью удалять мочевой пузырь. Вместе с ним удаляют близлежащие лимфоузлы, у мужчин — семенные пузырьки и простату, у женщин — матку с шейкой и придатками, верхнюю часть влагалища. Операцию выполняют разными способами: через разрез, лапароскопически, в некоторых клиниках прибегают к роботизированной хирургии. После цистэктомии пациент остается без мочевого пузыря. Для того чтобы восстановить отток мочи, прибегают к разным вариантам реконструктивных операций:
- Врач может удалить часть сигмовидной кишки, сформировать из нее новый мочевой пузырь и соединить его с мочеточниками. Из участка кишки на поверхность кожи выводят отверстие: через него оттекает моча. При этом на коже постоянно придется носить мешочек для сбора мочи и периодически опорожнять его.
- Более совершенный вариант оперативного лечения — когда хирург формирует в кишке специальный клапан. Этот клапан перекрывает отверстие и не дает моче вытекать. Когда пациент хочет помочиться, он вставляет в отверстие катетер, клапан открывается, и моча вытекает по катетеру.
- Наиболее современная операция — когда хирург подсоединяет к одному концу кишки мочеточники, а к другому — мочеиспускательный канал. У большинства пациентов в течение нескольких месяцев восстанавливается способность к самостоятельным мочеиспусканиям, но зачастую остается недержание мочи по ночам.
Иногда запущенный рак, который не может быть удален хирургически, приводит к недержанию мочи или, напротив, создает препятствие для ее оттока. В таких случаях прибегают к паллиативным хирургическим вмешательствам.
Химиотерапия
Химиопрепараты при злокачественных опухолях мочевого пузыря могут решать разные задачи:
- Неоадъювантную химиотерапию проводят до хирургического вмешательства. Благодаря препаратам опухоль уменьшается, и ее становится проще удалить.
- Адъювантная химиотерапия применяется после операции. Если в организме пациента остались раковые клетки, химиопрепараты их уничтожают, за счет этого снижается риск рецидива.
- Химиолучевая терапия — когда химиопрепараты назначают «в помощь» лучевой терапии. За счет этого повышается эффективность лечения рака.
- Паллиативная химиотерапия — один из основных методов лечения на поздних стадиях, когда опухоль неоперабельна, имеются отдаленные метастазы. Химиопрепараты помогают продлить жизнь пациента и избавить от некоторых симптомов.
Злокачественные новообразования мочевого пузыря лечат цисплатином, гемцитабином, винбластином, метотрексатом, доксорубицином, карбоплатином, доцетакселом, паклитакселом. Эти препараты назначают в различных сочетаниях. Если пациент не может переносить два и более препарата из-за побочных эффектов, назначают один препарат, чаще всего цисплатин или гемцитабин.
На ранних стадиях проводят внутрипузырную химиотерапию: химиопрепарат вводят внутрь мочевого пузыря через мочеиспускательный канал.
Лучевая терапия
Показания к лечению лучевой терапией при злокачественных опухолях мочевого пузыря:
- Лечение опухоли на ранних стадиях, если пациенту противопоказана операция, либо если во время хирургического вмешательства удален не весь мочевой пузырь.
- Для борьбы с симптомами, вызванными злокачественной опухолью.
Иммунотерапия рака мочевого пузыря
Иммунитет человека умеет уничтожать не только болезнетворные микроорганизмы, проникшие извне, но и собственные клетки, в генах которых возникли «ошибки». Именно из-за таких «ошибок» нормальная клетка превращается в раковую. Однако, опухолевые клетки умеют «обманывать» иммунитет, и используют для этого сложные молекулярные механизмы.
Так, иммунная система использует некоторые молекулы (они называются контрольными точками), чтобы подавлять собственную активность и не атаковать нормальные ткани организма. На поверхности иммунных клеток находится белок PD-1, который, взаимодействуя с белком PD-L1 на поверхности других клеток, подавляет иммунную реакцию. Для того чтобы снять блок с иммунной системы, для лечения применяют две группы иммунопрепаратов:
- Блокаторы PD-1: пембролизумаб (Кейтруда), ниволумаб (Опдиво).
- Блокаторы PD-L1: атезолизумаб (Тецентрик), авелумаб (Бавенцио), дурвалумаб (Имфинци).
Все эти препараты вводят внутривенно через каждые 2–3 недели. Обычно их назначают пациентам, у которых опухоль не реагирует на химиотерапию и продолжает прогрессировать.
Спустя несколько недель после трансуретральной резекции могут быть назначены внутрипузырные введения вакцины БЦЖ. Она стимулирует местные иммунные механизмы, которые уничтожают оставшиеся опухолевые клетки. БЦЖ вводят в мочевой пузырь через мочеиспускательный канал, обычно раз в неделю в течение шести недель.

Каким будет план лечения на разных стадиях рака мочевого пузыря?
Лечебная тактика на разных стадиях выглядит примерно следующим образом:
- На стадии 0 (когда опухоль находится в верхнем слое слизистой оболочки): трансуретральная резекция с последующим введением в мочевой пузырь вакцины БЦЖ или химиопрепаратов.
- На стадии I (опухоль в слизистой оболочке, которая не вросла в мышечный слой стенки) лечение начинают с трансуретральной резекции, но ее проводят не для того, чтобы вылечить пациента, а чтобы определить стадию рака. Далее может быть проведена повторная трансуретральная резекция с последующим введением в мочевой пузырь БЦЖ или химиопрепаратов. При больших, множественных и агрессивных опухолях рекомендуется удалить мочевой пузырь. Если операция противопоказана из-за слабого здоровья пациента, назначают лучевую или химиолучевую терапию, но шансы на успешное лечение в таком случае ниже.
- На стадии II (опухоль проросла в мышечный слой) удаляют мочевой пузырь, до или после операции проводят курс лечения химиотерапией. У немногих пациентов удается удалить только часть мочевого пузыря. Иногда при небольших опухолях проводят трансуретральную резекцию с последующей химиотерапией и лучевой терапией, но это сомнительный подход, не все врачи с ним согласны.
- На стадии III (опухоль распространяется за пределы мочевого пузыря) выполняют цистэктомию, проводят курс адъювантной или неоадъювантной химиотерапии. Если пациент не может перенести операцию, врач может назначить трансуретральную резекцию, химиотерапию, лучевую терапию, иммунотерапию.
- На стадии IVA (опухоль прорастает в стенку брюшной полости, таза) лечение начинают с курса химиотерапии или химиолучевой терапии. Когда опухоль уменьшается в размерах, может быть проведено хирургическое вмешательство. Если пациент не может перенести химиотерапию, назначают лучевую терапию, иммунопрепараты.
- На стадии IVB (имеются отдаленные метастазы) лечение начинается с химиотерапии или химиолучевой терапии. Если пациент не может перенести химиотерапию, назначают лучевую терапию, иммунопрепараты. Проводят паллиативные хирургические вмешательства, направленные на восстановление оттока мочи или борьбу с недержанием.
Как лечить опухоли мочевого пузыря с метастазами?
На момент постановки диагноза у 10–15% больных со злокачественными новообразованиями мочевого пузыря уже имеются отдаленные метастазы. У 30% пациентов после радикального лечения (полного удаления опухоли) происходит рецидив в мочевом пузыре или в виде метастазов.
Бороться с метастазировавшим раком сложно. Обычно радикальное хирургическое лечение и наступление ремиссии невозможно. Лечение начинают с химиотерапии. Учитывают состояние здоровья пациента и молекулярно-генетические характеристики опухолевых клеток:
- Если больному не противопоказан цисплатин: гемцитабин (Гемзар) + цисплатин или DDMVAC (уплотненная доза MVAC): метотрексат + винбластин + доксорубицин (адриамицин) + цисплатин.
- Больному противопоказан цисплатин, но не противопоказан карбоплатин: гемцитабин (Гемзар) + карбоплатин.
- Больному противопоказан цисплатин, и в опухолевых клетках обнаружен маркер PD-L1: гемцитабин (Гемзар) + карбоплатин, атезолизумаб (Тецентрик), пембролизумаб (Кейтруда).
- Больному противопоказаны все препараты платины: атезолизумаб (Тецентрик), пембролизумаб (Кейтруда).
Если на фоне применения препаратов первой линии заболевание продолжает прогрессировать, назначают препараты второй линии:
- После лечения препаратами платины: пембролизумаб (Кейтруда), атезолизумаб (Тецентрик), ниволумаб (Опдиво), дурвалумаб (Имфинзи), авелумаб (Бавенцио), эрдафитиниб (Балверса — для пациентов, у которых обнаружены мутации FGFR2 и FGFR3).
- После лечения ингибиторами контрольных точек, если пациенту противопоказан цисплатин: гемцитабин (Гемзар) + карбоплатин.
- После лечения ингибиторами контрольных точек, если пациенту не противопоказан цисплатин: гемцитабин (Гемзар) + цисплатин, DDMVAC.
Параллельно с противоопухолевыми препаратами может применяться лучевая терапия.
Какие методы лечения рака мочевого пузыря наиболее эффективны?
На этот вопрос нет однозначного ответа. Всё зависит от стадии, типа, молекулярно-генетических характеристик опухоли, состояния здоровья пациента, наличия и отсутствия у него противопоказаний.
Оптимальные методы лечения злокачественных опухолей мочевого пузыря прописаны в специальных документах — протоколах. Они составлены на основе результатов многочисленных клинических исследований с участием тысяч пациентов по всему миру и регулярно пересматриваются, обновляются.
Врачи в Европейской клинике руководствуются последними версиями американских, европейских, израильских протоколов лечения.
Насколько эффективны современные методы лечения, каков прогноз?
В среднем в течение 5 лет остаются в живых 77% пациентов, в течение 10 лет — 70%, в течение 15 лет — 65%. Пятилетняя выживаемость при злокачественных опухолях мочевого пузыря зависит от стадии:
- Стадия 0–98%.
- Стадия I—88%.
- Стадия II—63%.
- Стадия III—46%.
- Стадия IV—15%.
В настоящее время проводятся клинические исследования, врачи ищут более эффективные способы борьбы с заболеванием, а значит, есть надежда, что в ближайшем будущем эти показатели улучшатся.
Источник
