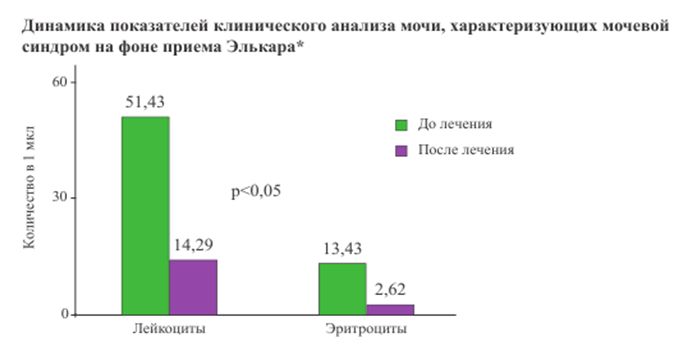
Элькар при нейрогенном мочевом пузыре
Комментарии
Е.Л. ВИШНЕВСКИЙ, И.С. БЕЛОУСОВА
ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава»
Международным обществом по вопросам удержания мочи в 2004 году для описания расстройств мочеиспускания рекомендован к использованию новый термин – синдром гиперактивного мочевого пузыря (ГАМП), характеризующийся поллакиурией, императивными позывами и императивными недержаниями мочи различной степени выраженности, часто – в сочетании с энурезом.
В отечественной литературе для обозначения данного состояния традиционно использовался термин «нейрогенная дисфункция мочевого пузыря», в рамках которого в зависимости от состояния резервуарной пузырной функции выделялось три варианта патологии: гипер-, нормо- и гипорефлекторный мочевой пузырь.
В КАКОМ ВОЗРАСТЕ СИМПТОМОКОМПЛЕКС ГАМП У ДЕТЕЙ СТОИТ СЧИТАТЬ ЗАБОЛЕВАНИЕМ?
К 4 годам большинство детей имеют волевой контроль основных функций мочевого пузыря и формируют «зрелый тип мочеиспускания», характеризующийся:
полным удержанием мочи днем и ночью;
- умением задерживать и прерывать при необходимости акт мочеиспускания;
- умением опорожнять мочевой пузырь без предшествующего позыва на мочеиспускание;
- поведенческие реакции, сопровождающие акт мочеиспускания – стремление к уединению при появлении позыва и пр.
В норме дети 3-4 лет опорожняют мочевой пузырь 5-8 раз во время бодрствования; средний эффективный объем мочевого пузыря колеблется от 80 до 150 мл.
Таким образом, о формировании симптомо-комплекса ГАМП можно говорить, если у ребенка 4 лет и старше число мочеиспусканий и эффективный объем мочевого пузыря выходят за рамки нормативных показателей, мочеиспускание неконтролируемо в той или иной степени.
Очевидно, что в силу негативного влияния ГАМП на качество жизни и риска присоединения микробно-воспалительных заболеваний мочевой системы нарушения мочеиспускания подлежат ранней диагностике и лечению.
ПРИНЦИПЫ ЛЕЧЕНИЯ ГАМП
С 1870 года единственными хорошо изученными и эффективными средствами медикаментозного лечения данной патологии являются препараты на основе атропина – М-холинобло-каторы. И в настоящий момент М-холинобло-каторы (оксибутинина гидрохлорид, толтеро-дина тартрат) остаются препаратами первого ряда в лечении симптомов гиперактивного мочевого пузыря (Международное общество по вопросам удержания мочи, 2000).
М-холиноблокаторы демонстрируют высокую эффективность при подавлении неконтролируемых сокращений детрузора. Однако наряду с этим им свойственна высокая частота появления системных побочных эффектов: общая атропинизация (40-65%) и нарушения со стороны центральной нервной системы (10-15%), которые становятся главным ограничением при лечении. При этом частота возникновения побочных эффектов у детей в 4 раза превосходит таковую у взрослых. Из-за выраженности побочных эффектов терапию вынуждены прекращать 10-30% пациентов.
Все вышеперечисленное диктует необходимость поиска новых этиопатогенетических методов лечения гиперактивного мочевого пузыря у детей.
В последние годы детально изучается влияние гипоксии на функцию мочевого пузыря. Нарушения кровоснабжения мочевого пузыря, тканевая гипоксия и сопряженные нарушения биоэнергетики детрузора признаны важнейшими патогенетическими звеньями расстройств мочеиспускания. Объясним интерес к средствам оптимального фармакологического воздействия на них.
Основным средством метаболической терапии, широко используемым при лечении расстройств мочеиспускания, является препарат из группы ноотропных средств – Пикамилон.
Ранее было показано, что у большинства детей симптомокомплекс ГАМП разворачивается на измененном биоэнергетическом фоне (на фоне политканевой митохон-дриальной дисфункции), оказывающем заметное влияние на формирование и клинические проявления расстройств мочеиспускания. Это явилось основанием для использования в лечении данной патологии препарата L-карнити-на (Элькар®).
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
При анализе имеющихся разрозненных данных об эффективности использования различных метаболических препаратов возникают практические вопросы. Какова их сравнительная клиническая эффективность у детей с ГАМП? У какой категории пациентов использование изучаемых фармакологических средств является наиболее обоснованным и эффективным?
Нами была проведена сравнительная оценка клинической эффективности Элькара и Пи-камилона в режиме монотерапии у детей с ГАМП различной степени тяжести
Обследовано 77 детей с ГАМП в возрасте от 4 до 15 лет. Максимальное количество дисфункций приходилось на дошкольный возраст. Клиническая картина заболевания характеризовалась поллакиурией, императивными позывами и императивными недержаниями мочи различной степени выраженности, часто в сочетании с энурезом.
Использованы общепринятые лабораторные и рентген-урологические методы обследования. Учитывая вариабельность клинической картины, для объективизации оценки расстройств мочеиспускания использовалась квали-метрическая Таблица оценки расстройств мочеиспускания, составленная на основании рекомендаций Международного комитета по удержанию мочи у детей с учетом возрастных нормативов (табл.1). Результатом заполнения таблицы являлся суммарный балл расстройств мочеиспускания, определенный в качестве главного объективного критерия для оценки выраженности клинической симптоматики и эффективности терапии.
Таблица 1
Ф.И.О.________________________________________________________________________№и/б
Дата рождения__________________________________________________________________Пол
| ТАБЛИЦА ОЦЕНКИ МОЧЕИСПУСКАНИЯ (для детей от 4 до 15 лет) | ||||
| Параметр | Балл | |||
| 1. Позыв на мочеиспускание | Нормальный Императивный — не каждый день Императивный — каждый день 1 раз Императивный — каждый день неск. раз | 0 1 3 5 | ||
| 2. Императивное недержание мочи | Нет Не каждый день Каждый день — 1 раз Каждый день — несколько раз | 0 1 3 5 | ||
| 3. Непроизвольное мочеиспускание во время сна | Нет Несколько раз в месяц Несколько раз в неделю Каждую ночь — 1 раз Каждую ночь — несколько раз Во время дневного сна | 0 1 3 5 7 7 | ||
| 4. Ритм спонтанных мочеиспусканий | А. Число м/и в сутки: | |||
| 1-2 3-4 5-6 7-8 9-10 11-12 13-14 15-16 17-18 19-20 Более 21 | 6 3 2 4 6 8 10 12 14 | |||
| Б. Средний эффективный объем мочевого пузыря, мл | Возраст, лет | |||
До 50 мл 51-75 76—100 101—125 126-150 151—175 176—200 201—250 251-300 Более 300 Ср. эффективный объем, мл | 4-7 4 3 2 1 1 2 3 | 8-11 5 4 3 2 1 1 2 | 12-15 6 5 4 3 2 1 1 | |
| Диурез с 1800 до 600 в % от суточного | До 40% 41—50% 51—60% 61—70% Более 71% | 0 3 6 9 12 | ||
| Суммарный балл | ||||
В зависимости от степени выраженности расстройств мочеиспускания, определенных по квалиметрическим таблицам, для анализаклинических наблюдений было выделено 3 группы больных:
- 1 группа – легкая степень расстройств мочеиспускания, суммарный балл 2-10.
- 2 группа – средняя степень расстройств, суммарный балл 11-20.
- 3 группа – тяжелая степень расстройств мочеиспускания, суммарный балл 21-30.
Курс терапии L-карнитином (Элькар®, компания «Пик-Фарма», Россия) получили 43 ребенка. 34 пациентам проведено лечение вазоактив-ным препаратом Пикамилоном. Распределение детей случайное.
Общая оценка эффективности терапии проводилась на основании рекомендаций Международного общества по удержании мочи у детей (1998 г.) по динамике эпизодов недержаний мочи и/или энуреза. Ответ на лечение считался полным в случае исчезновения более чем 90% эпизодов недержания мочи; частичным (улучшение) – при снижении числа эпизодов недержаний мочи на 50-90%; уменьшение числа эпизодов недержаний мочи менее чем на 50% расценивалось как отсутствие ответа (резистентность).
Проведенный по окончанию месячного курса терапии анализ динамики исходных клинических показателей расстройств мочеиспускания показал, что терапевтическая эффективность Элькара составила 84%, тогда как эффективность Пикамилона составила 80%. Более чем в половине наблюдений ответ на терапию Элькаром носил частичный характер и заключался в уменьшении количества эпизодов недержания мочи на 50-90%
У пациентов, получавших Элькар, было зарегистрировано достоверное снижение суммарного балла расстройств мочеиспускания с 13,8 до 6,3, т.е. на 56% от исходного, что не отличалось от регрессии клинической симптоматики на фоне приема Пикамилона.
На фоне терапии Элькаром наиболее стабильно обратному развитию подвергались дневные симптомы ГАМП, в то время как энурез являлся стойким и медленно поддающимся обратному развитию симптомом – его редукция отмечена только в половине наблюдений.
Во всех немногочисленных случаях исчезновения энуреза достигнутый эффект был нестойким. У 4 детей на фоне уменьшения дневных симптомов расстройств мочеиспускания ночная продукция мочи и кратность энуреза увеличились.
Эффективность терапии Элькаром зависела от исходной степени выраженности расстройств мочеиспускания. Так, при легкой и средней степени тяжести расстройств эффективность терапии составила 81 и 93% соответственно, при тяжелой степени – не превышала 66%. Во всех трех группах в большинстве наблюдений отмечался частичный ответ на терапию.
У детей с исходно сниженной емкостью мочевого пузыря Элькар оказывал позитивное влияние на резервуарную функцию: при легкой и средней степени тяжести расстройств мочеиспускания среднеэффектив-ный объем мочевого пузыря увеличился на треть (31 и 29%), а при тяжелой – более чем на половину.
Примечательно, что при тяжелой степени расстройств увеличение резервуарной способности мочевого пузыря на фоне приема Элькара было более существенным по сравнению с Пикамилоном. В то время как влияние Пикамилона на резервуарную функцию было гораздо более значимым у детей со средней степенью нарушений.
У пациентов с исходно увеличенным сред-неэффективным объемом мочевого пузыря вне зависимости от исходной степени тяжести расстройств Элькар влияния на резервуарную функцию не оказывал. Практически все дети остались резистентыми к терапии.
Обратная динамика симптомов расстройств мочеиспускания на фоне приема Элькара в целом схожа с показателями, достигнутыми на фоне приема Пикамилона. Исключение составили дети с исходно тяжелой степенью расстройств, у которых улучшение клинической симптоматики на фоне приема Элькара было более существенным (рис. 1).
Рисунок 1 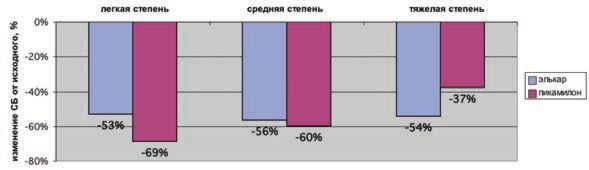
Изменение суммарного балла расстройств мочеиспускания (по Таблицам расстройств мочеиспускания) от исходного у детей с ГАМПразличной степени тяжести на фоне терапии элькаром и пикамилоном.
Примечание: СБ — суммарный балл по таблицам расстройств мочеиспускания.
Рисунок 2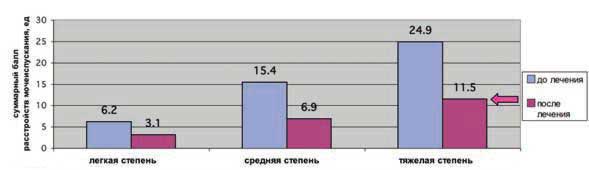
Суммарный балл расстройств мочеиспускания (по Таблицам расстройств мочеиспускания) у детей с ГАМП различной степени тяжести до и после терапии элькаром
Обратная динамика симптомов расстройств мочеиспускания на фоне терапии Элькаром была практически одинаковой у детей с различной исходной тяжестью расстройств и составляла 53-56% от базового показателя. Однако, учитывая различный стартовый уровень выраженности клинических проявлений, достигнутые на фоне лечения показатели принципиально различались. Так, у детей с исходно умеренной степенью расстройств мочеиспускания произошло их уменьшение до легкой степени, пациенты с тяжелой степенью расстройств к моменту окончания лечения сохраняли нарушения средней степени (рис.2).
Таким образом, проведенное исследование показало, что у детей с гиперактивным мочевым пузырем препарат Элькар в режиме монотерапии демонстрирует высокую клиническую эффективность, сопоставимую с действием Пикамилона – традиционного метаболического средства, используемого при лечении изучаемой патологии. Оба препарата имеют хорошую переносимость.
Элькар оказывает более выраженное позитивное влияние на дневные симптомы расстройств мочеиспускания, отражающие выпадение резерву-арной функции (поллакиурия, императивные позывы, императивное недержание мочи).
Применение Элькара в режиме монотерапии в лечении детей с гиперактивным мочевым пузырем является оправданным в случае исходной выраженности расстройств мочеиспускания легкой (0-10 баллов) и средней (11-20 баллов) степени при сохранной или сниженной резервуарной функции.
У детей с тяжелой выраженностью симптомов (более 21 балла) терапия Элькаром оказывает достоверное позитивное действие на изучаемые клинические параметры расстройств мочеиспускания, однако достигнутый при этом эффект не является достаточным для их нормализации. Исходя из полученных данных, можно ожидать, что у данной категории пациентов включение Элькара в комбинированную терапию позволит улучшить результаты лечения.
Данные клинических исследований позволяют применять обоснованный дифференцированный подход к лечению детей с ГАМП и оптимизировать лечебную тактику.
Сведения об авторах: Евгений Леонидович Вишневский, руководитель отдела урологии и нейроурологии ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава», профессор, д-р мед. наук
Ирина Станиславовна Белоусова, сотрудник отдела урологии и нейроурологии, ФГУ «Московский НИИ педиатрии и детской хирургии Росздрава», канд. мед. наук
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Элькар может применяться в практике детских нефрологов/урологов в комплексной терапии:
- гиперактивного мочевого пузыря
- нефропатий различного генеза, в том числе эконефропатии
1. Элькар снижает число эпизодов недержания мочи у детей с синдромом ГАМП, улучшая энергообеспечение и функциональное состояние детрузора
В исследовании, проведенном под руководством В. В. Длина и С. Л. Морозова, на базе НИКИ Педиатрии им. Ю. Е. Вельтищева, была установлена эффективность применения препарата Элькар раствор для приема внутрь 300 мг/мл у детей с синдромом ГАМП, а именно влияния препарата на повышение уровня энергетического фермента — сукцинатденидрогеназы и нормализацию энергетического обеспечения детрузора. В исследование были включены 120 детей с синдромом гиперактивного мочевого пузыря в возрасте от 6 до 14 лет (средний возраст составил – 8,78 ± 2,4 лет). У всех детей с синдромом ГАМП выявлено снижение среднеэффективного объема мочеиспускания и увеличение ритма спонтанных мочеиспусканий. У всех детей с гиперактивным мочевым пузырем проводился цитохимический анализ уровня ферментов локализованных в митохондриях лимфоцитов периферической крови, отвечающих за показатели клеточного энергообмена, в частности сукцинатдегидрогеназы (СДГ). У детей с гиперактивным мочевым пузырем исходный уровень СДГ в среднем составлял 16,1±2,74 у. е., при норме 18-23 у. е., и был снижен у 80% обследуемых. Для коррекции энергетического обмена Элькар назначался в дозе 50 мг/кг в сутки в течении 3-х месяцев. По данным цитохимического анализа по окончании терапии у детей с ГАМП уровень СДГ в среднем повысился на 38,6% и достиг показателей нормы
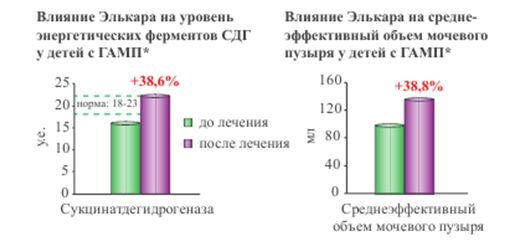
* НИКИ Педиатрии им. Ю. Е. Вельтищева, Длин В. В. Дети 6-14 лет с ГАМП, n=120. Элькар р-р для приема внутрь 300 мг/мл 50 мг/кг в сутки, 90 дней
Эффективность терапии препаратом Элькар синдрома ГАМП (% детей от исходного количества)*
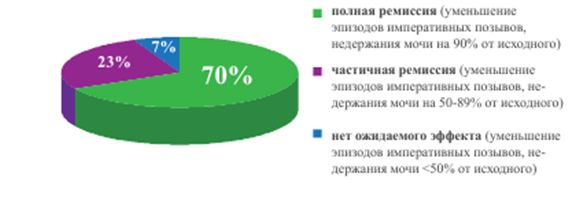
* НИКИ Педиатрии им. Ю. Е. Вельтищева, Длин В. В. Дети 6-14 лет с ГАМП, n=120. Элькар р-р для приема внутрь 300 мг/мл 50 мг/кг в сутки, 90 дней
Нормализация энергообеспечения детрузора, привела к снижению выраженности симптомов ГАМП и улучшению функционального состояния мочевого пузыря, а именно:
- увеличению среднеэффективного объема мочевого пузыря на 38,8%,
- снижению числа эпизодов императивного мочеиспускания и недержания мочи: у 70% детей на 90%, что расценивалось исследователями как полная ремиссия синдрома ГАМП; частичная ремиссия имела место у 23% детей в виде уменьшения числа эпизодов императивных позывов и недержания мочи на 50-89%. У 7% пациентов монотерпия препаратом Элькар не дала ожидаемого эффекта — число эпизодов императивного мочеиспускания и недержания мочи было снижено менее чем на 50% (28)
Вывод: У детей с ГАМП монотерапия препаратом Элькар улучшает энергетическое обеспечение детрузора, увеличивает среднеэффективный объем мочевого пузыря, снижает число эпизодов императивных позывов на мочеиспускание и недержания мочи.
27. В. В. Длин, Н. Б. Гусева, С. Л. Морозов «Гиперактивный мочевой пузырь у детей. Перспективы энерготропной терапии. Эффективная фармакотерапия. Педиатрии, №42/2013 с.32-36
28. В. В. Длин, С. Л. Морозов. Научный отчет по результатам открытого, одноцентрового проводимого в группах сравнения исследования «Оценка терапевтического влияния препаратов левокарнитина (Элькар) и гопантеновой кислоты (Пантогам) у детей с гиперактивным мочевым пузырем» , Москва, 2014, с.23
2. Элькар ускоряет выведение ксенобиотиков из организма и рекомендуется для лечения и профилактики эконефропатий у детей
В исследовании, проведенном в МНИИ Педиатрии и детской хирургии было показано, что Элькар® в монотерапии нивелирует негативные действия ксенобиотиков на почки, способствует выведению ксенобиотиков из организма.
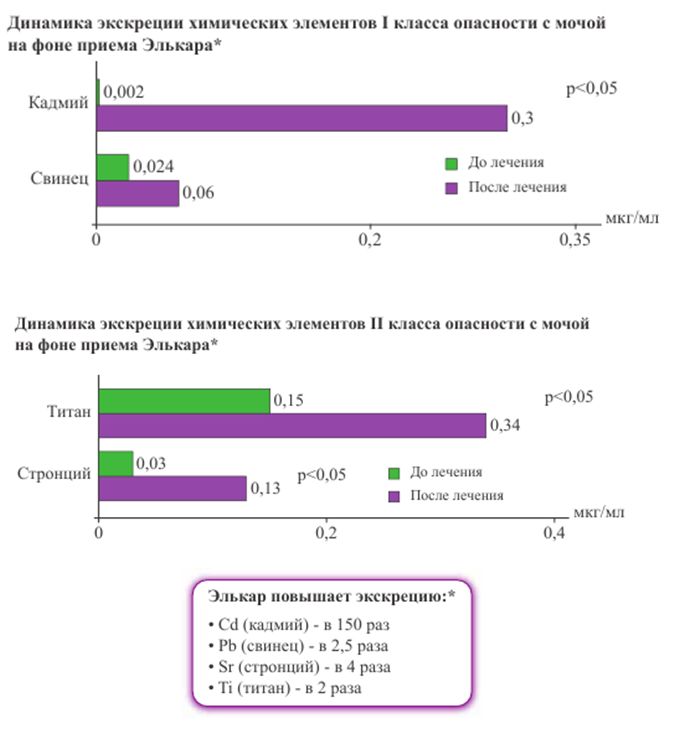

*МНИИ Педиатрии и детской хирургии Росздрава, А. Д. Царегородцев, дети средний возраст 7,58+ 1,29 лет, n= 30, Элькар р-р для приема внутрь 300 мг/мл 20-30 мг/кг 2 раза в сутки, 14 дней
На фоне лечения Элькаром повышается экскреция нефротоксических элементов (кадмия, свинца, мышьяка, титана), улучшаются процессы клубочковой фильтрации и канальцевой реабсорбции, снижается оксалатурия.
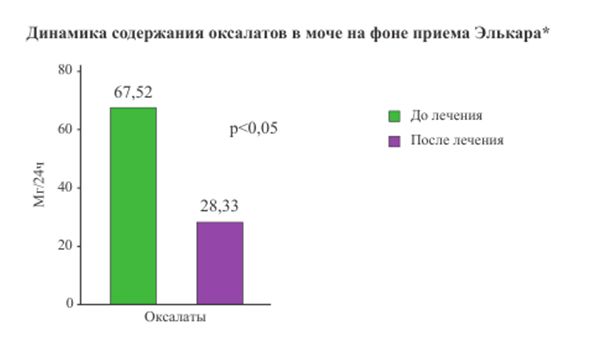
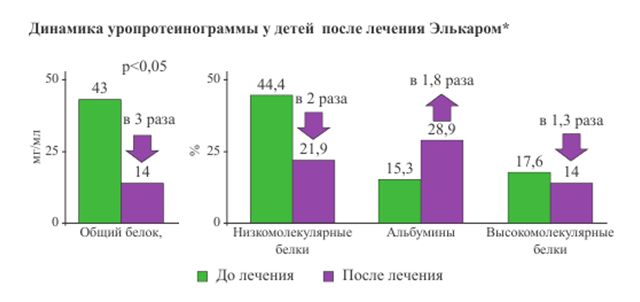
*МНИИ Педиатрии и детской хирургии Росздрава, А. Д. Царегородцев, дети средний возраст 7,58+ 1,29 лет, n= 30, Элькар р-р для приема внутрь 300 мг/мл 20-30 мг/кг 2 раза в сутки, 14 дней
Таким образом, повышая выведение ксенобиотиков из организма, Элькар может способствовать предотвращению развития эконефропатий у детей, проживающих в крупных городах и других экологически-неблагоприятных местностях.
*А. Д. Царегородцев, М. В.Кудин, В. В. Длин, А. В. Скрипкин, Ю. Н. Федоров, И. А.Поверинова Лечение и профилактика экологически обусловленной нефропатии у детей из селебитных зон цементной промышленности с позиции доказательной медицины. 2012;И Оверлей; М.: с.29-44
**Приказ МЗ РФ от 09.11.2012 №762н “Об утверждении стандарта специализированной медицинской помощи при нарушениях развивающихся в результате дисфункции почечных канальцев (тубулопатии)”.
—>
Источник
Комментарии
Опубликовано в журнале:
Медицинский вестник, № 3-4 (430-431), 1 февраля 2008 г.
Л.М. КУЗЕНКОВА, заведующая отделением психоневрологии Института педиатрии, доктор медицинских наук
О.И. МАСЛОВА, консультант Консультативно-диагностического центра, профессор, доктор медицинских наук
А.Г. ТИМОФЕЕВА, ученый секретарь, кандидат медицинских наук
О.В. БЫКОВА, старший научный сотрудник отделения психоневрологии Института педиатрии, кандидат медицинских наук ГУ “Научный центр здоровья детей” РАМН (Москва)
А.С. АРТЮХИНА, доктор медицинских наук. Центр лечения детей с нарушениями мочеиспускания (Волгоград)
Энурез – расстройство, проявляющееся стойким, непроизвольным мочеиспусканием днем или ночью (без связи с временем суток). У детей 1,5-2 лет недержание мочи является физиологическим явлением, связанным с незрелостью соматовегетативной регуляции. В возрасте 3-4 лет начинают устанавливаться навыки задержки мочи при наполнении мочевого пузыря, к 5 годам жизни контроль за тазовыми функциями достигается в преобладающем большинстве случаев. По разным данным, ночным энурезом страдают от 10 до 20% детей в возрасте 5 лет, 5% – десятилетних и 2% – больных от 12 до 14 лет. По мере взросления распространенность энуреза снижается, и к 18 годам он сохраняется лишь у 1% подростков. У мальчиков ночное недержание мочи наблюдается чаще, чем у девочек (2:1 до 3:2), дневное недержание мочи чаще отмечается у девочек.
Этиология
Этиология расстройств мочеиспускания мультифакториальная и основными причинами являются:
– инфекции мочевыводящей системы;
– пороки развития и нарушения функции почек, мочевого пузыря и мочевыводящих путей;
– органические поражения нервной системы, неврозы; расстройства психики (редко) и психологические стрессы;
– нарушения циркадного ритма секреции гормонов, регулирующих экскрецию воды и солей (вазопрессин, натрийуретический гормон, система ренин-ангиотензин-альдостерон);
– врожденное нарушение формирования условного “сторожевого” рефлекса;
– задержка становления навыков регуляции мочеиспускания;
– нарушение приобретенного рефлекса мочеиспускания вследствие воздействия неблагоприятных факторов;
– наследственная отягощенность.
Основа регулирования функции мочевого пузыря представляется сложной и не до конца изученной. Местные внутристеночные нервные узлы, спинальные, подкорковые (зрительный бугор и гипоталамус) и корковые (парацентральная долька, передняя центральная извилина) центры регуляции мочеиспускания объединены проводящими путями в единую функциональную систему. Взаимодействие различных элементов этой системы реализуется в 12 интегральных пузырных рефлексах. Недостаточность или избыточная активность хотя бы одного из пузырных рефлексов может вызвать серьезные нарушения функции мочевого пузыря.
Профилактика развития энуреза связана со своевременным формированием навыков опрятности, выявлением и лечением урологической патологии, комфортной психологической обстановкой в семье и коллективе.
Классификация
Выделяют дневной энурез – недержание мочи в течение дня и ночной – мочеиспускание во время сна. Кроме того, различают первичный (персистирующий) и вторичный, или психогенный (приобретенный) энурез. При первичном энурезе у пациента контроль над функциями мочевого пузыря не сформирован с рождения. При вторичном энурезе условный рефлекс, вызывающий пробуждение, уже был выработан, но оказался утрачен или резко ослаблен по ряду причин (психическая травма, тяжелые инфекционные заболевания, интоксикации).
Клиническая картина и диагностика
Клиническую картину смотрите в таблице 1.
Таблица 1. Клиническая картина первичного и вторичного энуреза
| Первичный (персистирующий) | Вторичный (психогенный) |
Диагностика и дифференциальная диагностика энуреза основывается на адекватной оценке анамнестических, клинических и параклинических данных (табл. 2).
Таблица 2. Анамнестические, клинические и параклинические данные энуреза
| Анамнестические | Клинические | Параклинические |
Лечение
Немедикаментозное лечение: использование мочевых будильников, ночные пробуждения по расписанию, обязательное опорожнение мочевого пузыря перед сном, жесткая постель, комфортный температурный и световой режим, благоприятная психоэмоциональная обстановка, психотерапия (только при лечении детей с нормальным интеллектом), диетотерапия, ограничение потребления любой жидкости после ужина, исключение из рациона продуктов, обладающих мочегонным действием, физиотерапия.
Хирургическое лечение назначают при пороках развития мочевыводящей системы или при стойком отсутствии эффекта от консервативной терапии.
Лекарственная терапия:
1. При энурезе вследствие инфекции мочевых путей назначаются антибиотики и уросептики (с учетом чувствительности выделенной патогенной микрофлоры к антибиотикам).
2. При первичном ночном энурезе – десмопрессин в дозе 0,2 мг 1 раз на ночь, при недостаточном эффекте – увеличение дозы до 0,4 мг. Курс лечения – от 6 недель до 3 месяцев с последующей отменой препарата в течение одной недели и возобновлением терапии при необходимости.
3. При нейрогенной дисфункции мочевого пузыря – м-холинолитики.
4. При вторичном (психогенном) ночном энурезе – препараты ноотропного, тимолептического действия, транквилизаторы.
Поскольку в патогенезе энуреза значительная роль принадлежит нарушению интегративных функций центральной нервной системы, то не вызывает сомнения необходимость воздействия на высшие центры регуляции актов мочеиспускания с помощью нейротропных средств. При вторичном энурезе рекомендуются препараты, улучшающие метаболические и биоэнергетические процессы в нервных клетках, влияющие на нейромедиаторные системы мозга, – ноотропы.
Одним из таких препаратов является Пантогам® – кальциевая соль Б(+)-пантоил-гамма-аминомасляной кислоты. Положительный терапевтический эффект Пантогама® у детей с вторичным энурезом обусловлен его вегетотропной активностью, транквилизирующим действием, способностью повышать контроль подкорковых областей, стимулировать корковую деятельность и формирование условно-рефлекторных связей, а также воздействовать непосредственно на функции сфинктера, т.к. метаботропные ГАМК-рецепторы найдены не только в центральной нервной системе, но и во многих внутренних органах, в т.ч. и в мочевом пузыре.
Многочисленные исследования показали эффективность препарата Пантогам® для коррекции невротических состояний, часто сопровождающих энурез у детей. Прием Пантогама® расширяет адаптационные возможности ребенка путем нормализации соматовегетативных, когнитивных и эмоциональных компонентов психической деятельности детей.
При первом назначении Пантогама® рекомендуется титрование дозы в начале курса лечения и по его окончании, по трапеции (постепенное наращивание дозы в течение 10- 20 дней, прием препарата в максимальной дозе на протяжении 20-30 дней и затем снижение дозы в течение следующих 10-20 дней до полной отмены). Возможно повторение курса 2- 3 раза в год. В схему лечения “большими” ноотропами, к которым мы относим Пантогам®, не рекомендуется одновременное назначение других ноотропов. Однако показано назначение сосудистых средств, поливитаминов и антиоксидантов.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
