Экстрофия мочевого пузыря видео
Экстрофия мочевого пузыря – это порок развития мочеполовой системы, при котором формирование мочевого пузыря и передней брюшной стенки в его проекции остается незавершенным. С рождения наблюдается открытая и вывернутая наружу слизистая оболочка задней стенки мочевого пузыря, а также постоянное отделение и стекание мочи из открывающихся в нижней части органа протоков мочеточников. Экстрофия мочевого пузыря часто сочетается с пороками наружных и внутренних половых органов, мочеточников и почек. Диагностируется по характерным внешним признакам, дополнительно проводится рентгенологическое и УЗИ-обследование. Лечение оперативное, выполняются реконструктивно-пластические и заместительные операции.
Общие сведения
Экстрофия мочевого пузыря – одна из наиболее часто встречаемых аномалий развития мочеполовой системы. Частота в популяции – 1 случай на 30-50 тысяч новорожденных, примерно 1/5 часть пациентов имеет сочетанные пороки развития. В большей степени страдают мальчики, по данным разных авторов распространенность патологии среди них в 2-6 раз выше, чем среди девочек.
Специалисты в сфере педиатрии и хирургии сталкиваются с большими трудностями в лечении экстрофии мочевого пузыря, хотя первые операции для коррекции этой аномалии были предложены еще в 1960-х годах. Реконструкция и пластика не приводят к излечению. Сохраняющееся недержание мочи значительно ухудшает качество жизни ребенка, а частые восходящие инфекции становятся причиной хронической почечной недостаточности, представляющей серьезную опасность для жизни.
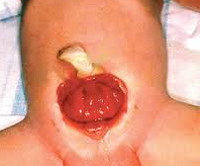
Экстрофия мочевого пузыря
Причины
Конкретной причины данной аномалии развития не выявлено, патология считается мультифакториальной. Доказана генетическая предрасположенность к некоторым сочетанным порокам органов брюшной полости, в числе которых присутствует и экстрофия мочевого пузыря. Кроме того, повышает риск развития аномалии воздействие различных токсических и инфекционных агентов во время беременности, в частности, курение, внутриутробные инфекции, некоторые медикаменты и т. д. Травмы плода также могут способствовать нарушению правильного эмбриогенеза с развитием пороков.
Патогенез
Основной патогенетический момент экстрофии мочевого пузыря – задержка обратного развития клоакальной перегородки, которая препятствует внедрению мезодермального листка между наружным и внутренним эмбриональными слоями. Это приводит к тому, что процесс формирования стенок мочевого пузыря оказывается незавершенным, и орган остается открытым и вывернутым наружу. Описанные процессы в норме протекают на 4-6 неделе эмбрионального развития, поэтому воздействие тератогенных факторов наиболее опасно в самом начале беременности. Впрочем, это касается не только экстрофии мочевого пузыря, но и большинства пороков развития.
Симптомы
Проявления порока визуально заметны сразу после рождения. Неонатолог при осмотре новорожденного обращает внимание на ярко-красную слизистую оболочку мочевого пузыря, которая замещает отсутствующую часть передней брюшной стенки. Слизистая, как правило, имеет обычную морфологию, но возможно и псевдопапилломатозное изменение. В нижней части заметны отверстия мочеточников, из которых постоянно выделяется моча.
С течением времени основной проблемой при экстрофии мочевого пузыря становится раздражение окружающих тканей мочевыми солями, постоянная мацерация вокруг открытого участка и в области бедер. Инфицирование слизистой оболочки мочевого пузыря является причиной восходящей инфекции мочеточников и почек.
Экстрофия мочевого пузыря часто сочетается с аномалиями верхних мочевыводящих путей. Кроме того, экстрофии всегда сопутствует расхождение лобкового симфиза. Вследствие анатомических различий у мальчиков и девочек наблюдаются разные изменения в соседних органах. У мальчиков встречается расщепление пещеристых тел или их редукция, у девочек – расщепление клитора, аномалии развития влагалища.
Диагностика
В последние годы активно развиваются методы антенатальной диагностики данного порока. Экстрофия мочевого пузыря может быть заметна уже на втором УЗИ-скрининге, однако такое случается не всегда. Часто аномалия развития обнаруживается только после рождения. Поскольку симптоматика специфична, диагноз не вызывает сомнений.
Обязательно проведение рентгенографии брюшной полости для выявления сочетанных пороков, в первую очередь, в мочевыделительной системе, но также в кишечнике и спинном мозге (наиболее характерные сочетания с экстрофией мочевого пузыря). С этой же целью проводится УЗИ. Рекомендована экскреторная урография, которая позволяет убедиться в целостности и правильном развитии мочеточников и почек.
Лечение экстрофии мочевого пузыря
Лечение оперативное. Тип операции зависит от степени экстрофии мочевого пузыря, а именно – от размеров вывернутой части органа и, соответственно, отсутствующего сегмента передней брюшной стенки, а также от сопутствующих пороков развития. Если размер дефекта не превышает 4 см, проводится реконструктивно-пластическое вмешательство, цель которого – закрытие дефекта с помощью близлежащих тканей и восстановление целостности мочевого пузыря. Этого достаточно, поскольку гистологически орган развит правильно, несмотря на патологию в анатомии.
В случае больших размеров дефекта создается искусственный мочевой пузырь, который может выполнять функцию резервуара и опорожняться по желанию. Также часто мочеточники выводятся в сигмовидную кишку (уретеросигмостомия) – это обязательная мера в случае их расщепления.
Большую проблему для детских хирургов представляет расхождение костей таза при экстрофии мочевого пузыря. Накопленный врачебный опыт говорит о высокой частоте неудовлетворительных результатов операций, что связано с большим количеством сочетанных пороков и значительным дефектом передней брюшной стенки.
Прогноз и профилактика
Прогноз для выздоровления сомнительный. Неоперированные пациенты редко доживают до 10 лет. Что касается успеха оперативного лечения, то 20-80% проведенных вмешательств приводят лишь к незначительному улучшению. Нарушения уродинамики продолжают прогрессировать, сохраняется недержание. Риск развития восходящей инфекции остается высоким.
Профилактика экстрофии мочевого пузыря возможна в антенатальном периоде, еще лучше – на этапе планирования беременности, чтобы максимально исключить воздействие тератогенных факторов, особенно на этапе закладки основных органов и систем, то есть в первые 4-8 недель внутриутробного развития.
Источник
Экстрофия мочевого пузыря у детей. Диагностика и лечениеЭкстрофия мочевого пузыря встречается с частотой 1 случай на 35 000-40 000 новорожденных. Мальчиков среди больных в 2 раза больше, чем девочек. Тяжесть дефекта мочевого пузыря колеблется от мелкого наружного свища или простой эписпадии до полной клоакальной экстрофии, захватывающей дистальный отдел толстой кишки, прямую кишку и мочевой пузырь. Экстрофия возникает в результате того, что мезодерма не распространяется в краниальном направлении в клоакальную мембрану. Тяжесть экстрофии зависит от протяженности дефекта мембраны. При классической экстрофии мочевого пузыря его слизистая оболочка выпадает через дефект брюшной стенки. Пупок смещен книзу. Ветви лобковой кости и прямые мышцы живота по срединной линии разделены. При полной эписпадии у мальчиков мошонка широкая и плоская, яички в нее не опущены, имеется паховая грыжа. При полной эписпадии у девочек половые губы широко раздвинуты, клитор расщеплен. Как у мальчиков, так и у девочек задний проход смещен кпереди, имеется выпадение прямой кишки. Для больных экстрофией характерно отставание в росте. В отсутствие коррекции экстрофия сопровождается полным недержанием мочи и является фактором риска рака мочевого пузыря, как правило аденокарциномы. Грубая деформация половых органов делает невозможной нормальную половую жизнь, особенно у мужчин. Отсутствие лобкового симфиза приводит к характерной походке с широко расставленными ногами, но нормальному передвижению не препятствует. Верхние отделы мочевых путей обычно нормальные. Лечение экстрофии мочевого пузыря у детей начинают с рождения. Обнаженную слизистую оболочку мочевого пузыря покрывают пластиковой пленкой, чтобы она оставалась влажной. (Накладывать марлю, даже смоченную вазелиновым маслом, не следует.) Сразу после этого ребенка доставляют в клинику, в которой имеются условия для хирургической коррекции экстрофии. Раньше ее всегда проводили в несколько этапов, в последнее время популярна одномоментная пластика. Одномоментное устранение порока предпочтительно. Оно включает мобилизацию брюшной стенки и сведение ветвей лобковой кости к срединной линии. В первые 48 ч жизни подвижность их достаточна, чтобы восстановить лобковый симфиз. При операции в более поздние сроки, чтобы сблизить ветви лобковой кости, приходится проводить остеотомию костей таза. При классической экстрофии ранняя пластика выполнима почти всегда. Откладывать операцию приходится в тех случаях, когда она сопряжена с особым риском интра- и послеоперационных осложнений, например, у недоношенных. Классическая экстрофия мочевого пузыря у новорожденной девочки. Полная коррекция экстрофии включает восстановление целости мочевого пузыря и брюшной стенки, а у мальчиков, кроме того, коррекций эписпадии путем расщепления полового члена. В связи с риском гидронефроза и ИМП прооперированные дети нуждаются в тщательном проспективном наблюдении. Часто эписпадии сопутствует пузырно-мочеточниковый рефлюкс, поэтому после операции показана профилактика ИМП антибактериальными препаратами. Если коррекция эписпадии не проведена сразу после рождения, ее выполняют в возрасте 1-2 года. До этого из-за отсутствия сфинктера у больных наблюдается полное недержание мочи. Заключительная стадия хирургического лечения состоит в воссоздании сфинктера мочевого пузыря и коррекции пузырно-мочеточникового рефлюкса. Как правило, ее удается выполнить к 3 годам, когда емкость мочевого пузыря составляет по крайней мере 80 мл и ребенок в состоянии контролировать дефекацию. К пубертатному возрасту в области наружных половых органов появляется оволосение. Для воссоздания типа оволосения, близкого к нормальному, необходима пластика лобка. Прогноз экстрофии мочевого пузыря у детей. Описанная выше схема лечения, по данным некоторых клиник, позволяет в 70 % случаев устранить недержание мочи. Осложнения со стороны верхних отделов мочевых путей наблюдаются менее чем в 15 % случаев. Возможность устранить недержание зависит не только от успешного выполнения реконструктивных операций, но и от размера мочевого пузыря и качества его стенки. Восстановление контроля над мочеиспусканием более вероятно у детей, которым пластика мочевогo пузыря проведена в период новорожденности. При невозможности пластики шейки мочевого пузыря из-за его малого размера и в случаях, когда недержание сохраняется более 1 года после нее, прибегают к другим методам достижения контроля над мочеиспусканием. В их числе: Длительное проспективное наблюдение показало, что половая функция у мужчин с экстрофией мочевого пузыря удовлетворительная, хотя половой член достигает лишь 1/2 нормального размера. Однако фертильность у них низкая, по-видимому, из-за повреждения половых органов в ходе реконструктивных операций. У женщин фертильность не страдает, но возможно выпадение матки во время беременности. – Также рекомендуем “Клоакальная экстрофия и эписпадия мочевого пузыря у детей. Дивертикулы” Оглавление темы “Патология мочевых путей у детей”:
|
Источник
Экстрофия мочевого пузыря и эписпадия у детей – клиника, диагностикаМежду амнионом и клоакой располагается тонкая пластинка — клоакальная мембрана. В норме по мере развития эмбриона она постепенно уменьшается и смещается к промежности. Если по какой-то причине этот процесс нарушается, то сохранившаяся мембрана препятствует смыканию мезодермальной пластинки спереди и нижняя часть передней брюшной стенки остается неразвитой. В конце концов клоакальная мембрана разрывается. Если к моменту разрыва разделение клоаки уже произошло, то возникает экстрофия мочевого пузыря. При этом его задняя стенка выступает через дефект брюшной стенки. Если же разделение не завершилось, то порок будет еще более тяжелым — экстрофия клоаки. Экстрофия мочевого пузыря почти всегда сочетается с эписпадией. Эписпадия без экстрофии возникает, когда персистирует только нижняя часть клоакальной мембраны. Экстрофия мочевого пузыря встречается у 1 из 30—40 тысяч живых новорожденных, чаще у мальчиков. Риск рождения в семье второго ребенка с экстрофией составляет 1%. При осмотре в нижней части живота виден дефект брюшной стенки, замещенный задней стенкой мочевого пузыря. Лобковый симфиз не сомкнут, ветви лобковых костей отстоят друг от друга на несколько сантиметров и развернуты кнаружи. У мальчиков короткий и широкий половой член с дорсальным искривлением, мочеиспускательный канал в виде открытого желобка. У девочек лобок и клитор расщеплены, дорсальная поверхность мочеиспускательного канала зияет. У детей обоих полов нарушений со стороны внутренних половых органов обычно нет. Часты косые паховые грыжи. Аномалии лобково-прямокишечной мышцы могут приводить к выпадению прямой кишки. Верхние мочевые пути обычно сохранны, но иногда встречаются сращение и другие аномалии развития почек. Почти у всех больных наблюдается двусторонний пузырно-мочеточниковый рефлюкс. Лечение экстрофии мочевого пузыря и эписпадии — хирургическое. Реконструктивные операции включают восстановление лобкового симфиза (с остеотомией или без), формирование мочевого пузыря и мочеиспускательного канала, закрытие дефекта брюшной стенки, у мальчиков — пластику полового члена. Одновременно стремятся поддержать функцию почек. Операции обычно проводят в несколько этапов, причем восстановление мочевого пузыря выполняют уже в первые 2 сут. Устранение эписпадии и пластику полового члена для его удлинения осуществляют в возрасте 6—12 мес. Наконец, чтобы устранить недержание мочи и пузырно-мочеточниковый рефлюкс, проводят реконструкцию шейки мочевого пузыря и реимплантацию мочеточников (уретероцистонеостомию). Эту операцию выполняют при достаточной емкости мочевого пузыря, примерно в возрасте 4—5 лет. Хорошие предварительные результаты получены в последнее время при одномоментном восстановлении мочевого пузыря и устранении эписпадии. К сожалению, несмотря на успешное закрытие дефекта мочевого пузыря и устранение эписпадии, в ряде случаев мочевой пузырь остается нерастяжимым. Таким больным может потребоваться цистопластика с подшиванием участка кишки и периодической катетеризацией. При выполнении реконструктивных операций в несколько этапов самостоятельного мочеиспускания без недержания мочи удается добиться у 75—85% детей. Вестибулярная форма экстрофии мочевого пузыря (сагиттальный разрез). – Также рекомендуем “Уретроррагия у мальчиков – клиника, диагностика” Оглавление темы “Аномалии мочеточника”:
|
Источник

УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5″ высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Экстрофия мочевого пузыря (ЭМП) – редкий тяжелый врожденный порок развития нижних мочевых путей, характеризующийся отсутствием передней брюшной стенки и передней стенки мочевого пузыря, а также расхождением лонного сочленения (диастаз). Через дефект передней брюшной стенки пролабирует слизистая оболочка. В нижней части обнаженной слизистой оболочки расположены устья мочеточников, из которых постоянно выделяется моча. Пуповина впадает низко в верхний край дефекта передней брюшной стенки.
Экстрофийные пороки нижних мочевых путей делят на классическую экстрофию мочевого пузыря и экстрофию клоаки. У мальчиков экстрофия мочевого пузыря сочетается с расщеплением мочеиспускательного канала (эписпадия). Экстрофия мочевого пузыря у девочек сопровождается расщеплением клитора, расщеплением или отсутствием мочеиспускательного канала, а также спайками больших и малых половых губ [1, 2].
В литературе экстрофия мочевого пузыря чаще всего описывается в комплексе с эписпадией, хотя имеются сообщения об изолированном поражении стенки мочевого пузыря, когда его шейка и мочеиспускательный канал сформированы. Такая патология называется неполной экстрофией, или переднепузырным свищом. При неполной экстрофии патология половых органов отсутствует [3, 4]. Наиболее тяжелой и редкой формой порока является экстрофия клоаки, при которой расщепление распространяется не только на урогенитальную область, но и на терминальный отдел кишечника [5, 6].
Впервые экстрофию мочевого пузыря, как врожденный порок развития, описал Schenk von Grafenberg в 1597 г. В 1780 г. Chaussier впервые использовал термин “экстрофия”. Упоминания об экстрофии мочевого пузыря обнаружены на ассирийских табличках, сделанных 2000 лет до н. э. [7]. Частота экстрофии мочевого пузыря составляет 0,25-0,5 на 10 тыс. новорожденных. Соотношение классической экстрофии мочевого пузыря у мальчиков и девочек 3:1 [1, 8]. При экстрофии мочевого пузыря встречаются сопутствующие врожденные аномалии – паховые грыжи (у 56 % мальчиков, у 15 % девочек), крипторхизм (20 %), колоректальные аномалии (1,8 %) и др. [1, 2]. Экстрофия мочевого пузыря может входить в состав комплекса OEIS (omphalocele, extrophy, imperforate anus, spinal defects), OMIM 258040.
Пренатальная диагностика экстрофии мочевого пузыря возможна уже при первом скрининговом обследовании в 11-14 нед беременности, когда в норме полость мочевого пузыря начинает наполняться мочой. Визуализация мочевого пузыря обязательно входит в стандартные протоколы исследования пренатального скрининга.
Эмбриопатогенез
Экстрофия мочевого пузыря формируется на 4-5-й неделе эмбриогенеза, когда на 28-32-й день происходит каудальная миграция мембраны клоаки. В то же время формируется передняя брюшная стенка, однако если мезенхима не переходит из одного клеточного слоя нижней брюшной стенки в другой, то это приводит к нестабильности клоакальной мембраны. Преждевременный разрыв мембраны клоаки приводит к комплексу “подпупочных” аномалий. Разрыв клоакальной мембраны после полного разделения “урогенитальной” части от пищеварительного тракта приводит к формированию классической экстрофии мочевого пузыря.
Если повреждение мембраны происходит до того, как спускается уроректальная перегородка, тогда это приводит к вывороту нижнего уретрального тракта и части пищеварительного тракта с формированием клоакальной экстрофии. Генетические факторы, связанные с экстрофией мочевого пузыря, на сегодняшний день не выявлены, однако существует гипотеза, что потеря экспрессии р63 из-за полиморфизмов очередности у промотера является фактором риска развития экстрофии мочевого пузыря [1, 9].
Ниже представлен случай диагностики экстрофии мочевого пузыря в III триместре беременности.
Материал и методы
Пациентка С.,18 лет, настоящая беременность первая, от первого брака, супруги соматически здоровы, профессиональных вредностей не имеют, наследственность не отягощена. На учете в женской консультации пациентка состояла с 9 нед беременности. Беременность протекала без осложнений. При скрининговом УЗ-исследовании в I и II триместрах по месту жительства ВПР и УЗ-маркеров хромосомных перестроек у плода не обнаружено.
При УЗ-обследовании в 34 нед беременности в женской консультации по месту жительства было обнаружено образование средней эхогенности размером 28x23x25 мм в области нижних отделов передней брюшной стенки. Женщина была направлена в медикогенетическое отделение МОНИИАГ с диагнозом: “ВПР плода, экстрофия мочевого пузыря?”.
УЗ-исследование проводилось на сканере WS80A (компании Samsung Medison) с использованием объемного датчика CV1-8A.
Результаты
При УЗ-исследовании обнаружен один живой плод женского пола в головном предлежании. Гестационный срок составил 34,4 нед. Фетометрические показатели плода соответствовали данному сроку. Патологических изменений плаценты и околоплодных вод не выявлено. При исследовании мочевой пузырь в типичном месте не визуализировался.
В нижних отделах передней брюшной стенки в надлобковой области визуализировалось эхогенное образование размером 30x28x25 мм (рис. 1, 2). Определялось низкое впадение пуповины. Почки плода визуализировались в типичном месте, без структурных изменений. Патологических изменений других органов не было выявлено.
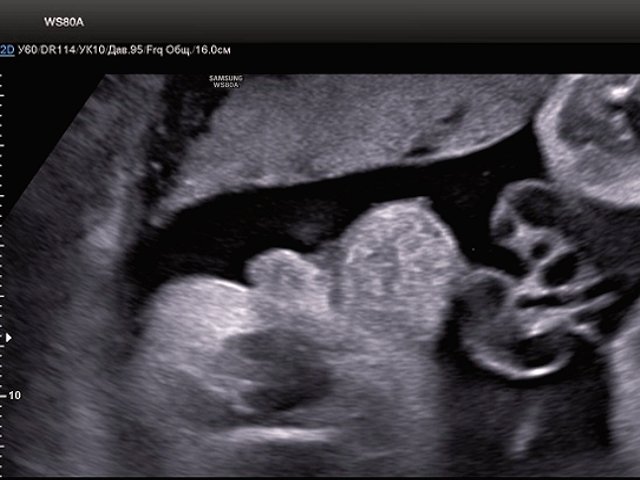
Рис. 1. Эхогенное образование в нижнем отделе передней брюшной стенки (экстрофированный мочевой пузырь).
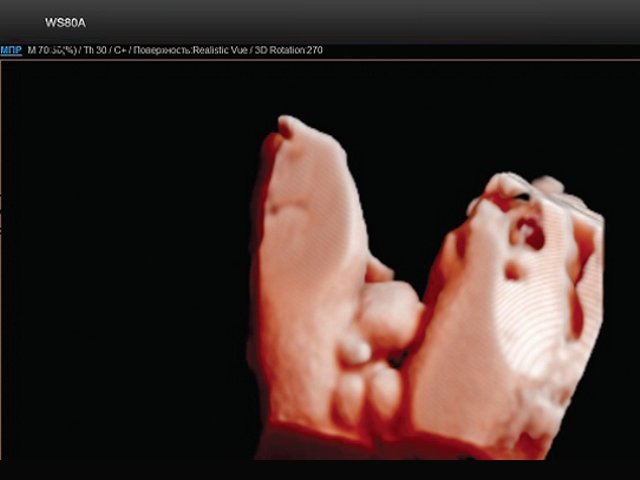
Рис. 2. Экстрофия мочевого пузыря в сочетании с отсутствием видимой патологии наружных половых органов (режим трехмерной реконструкции).
Поставлен диагноз: “Беременность 34,4 нед. ВПР плода – экстрофия мочевого пузыря”.
Обсуждение
Пренатальными УЗ-признаками экстрофии мочевого пузыря являются: отсутствие визуализации мочевого пузыря при нормальном количестве околоплодных вод, структурно неизмененные почки, визуализация эхогенного образования в надлобковой области, аномалии строения половых органов. Использование ЦДК является дополнительным инструментом для диагностики экстрофии мочевого пузыря. В норме пупочные артерии проходят вдоль стенки мочевого пузыря при поперечном сканировании нижней части живота. Для экстрофии мочевого пузыря характерно низкое впадение пуповины, при котором артерии охватывают образование в надлобковой области. При отсутствии визуализации мочевого пузыря в типичном месте необходимо провести повторное сканирование через 30-40 мин для адекватной оценки его расположения и степени наполнения.
Изолированная экстрофия мочевого пузыря, как правило, не сочетается с хромосомными перестройками у плода и не требует пренатального кариотипирования.
В данном клиническом наблюдении экстрофия мочевого пузыря была диагностирована у плода женского пола, что встречается значительно реже, чем у плодов мужского пола. Кроме того, отсутствие выраженной деформации наружных половых органов позволяет предположить неполную форму экстрофии. Оценка анатомии мочевого пузыря включена в протокол обязательного скринингового обследования во всех триместрах беременности. Отсутствие визуализации мочевого пузыря в типичном месте должно насторожить врачей УЗ-диагностики. Однако часто экстрофия мочевого пузыря диагностируют лишь в III триместре беременности.
После рождения детям с экстрофией мочевого пузыря требуется многоэтапная сложная хирургическая коррекция. Процент неудовлетворительных отдаленных результатов, к сожалению, остается на сегодняшний день очень высоким, как правило, вследствие присоединения таких осложнений, как нарушение функции тазовых органов: недержание мочи, рубцовая деформация половых органов, половая дисфункция, выраженная деформация передней брюшной стенки, уретерогидронефроз III-IV степени, непрерывно рецидивирующий пиелонефрит со снижением функции почек, хроническая почечная недостаточность и др. [4, 7]. Огромной и сложной проблемой остается медико-социальная реабилитация больных с экстрофией мочевого пузыря.
Заключение
Сложности ранней диагностики связаны с невыраженными УЗ-проявлениями достаточно тяжелой патологии. Четкое соблюдение алгоритма скрининговых УЗ-исследований анатомии плода в 11-14 и 20-22 нед беременности позволяет диагностировать экстрофию мочевого пузыря. При выявлении экстрофии мочевого пузыря у плода необходимо проведение медико-генетического консультирования с оформлением пренатального консилиума. Требуется тщательное разъяснение родителям сути выявленной патологии, а также информация о частых послеоперационных отдаленных последствиях и осложнениях как физического, так и психогенного генеза.
Литература
- Лопаткин Н.А., Пугачев А.Г. Пороки развития мочевого пузыря и уретры. В кн. Детская урология. Руководство. М.: Медицина, 1986. С. 207-242.
- Gearhart J.P. Criteria for the prenatal diagnosis of classic bladder exstrophy / J.P. Gearhart, J. Ben-Chaim, R.D. Jeffs // Obstet. Gynecol. 1995. Jun. 1. V. 85. № 6. P. 961-964.
- Михельсон А.И. Оперативное лечение недержания мочи на почве врожденных аномалий мочевой системы. Минск, Госсиздат БССР. 1957.
- Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей: автореф. дисс. докт. мед. наук. СПб, 1996.
- Ахунзянов А.А. Диагностика и лечение врожденной клоаки у детей // Хирургия. 1976. № 9. С. 98-101.
- Захаров Н.Л. Дефекты передней брюшной стенки у новорожденных // Хирургия. 1986. № 6.
- Hollowell J.G., Ransley P.G. Surgical management of Incontinence in bladder exstrophy // Brit. J. Urol. 1991. V. 68. № 5. P. 543-548.
- Kockum C.C., Hansson E.E., Stenberg A.et. al. Bladder exstrophy in Sweden-a long-term follow-up study // Eur. J. Pediatr. Surg. 1996. V. 6. P. 208-211.
- Баиров Г.А., Ахметджанов И.А., Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей // Вестник хирургии. 1986. Т. 136. № 6. С. 105-108.

УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5″ высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Источник
