Экстрофия мочевого пузыря пренатальная диагностика
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
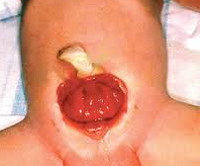
Экстрофия мочевого пузыря (ЭМП) – редкий тяжелый врожденный порок развития нижних мочевых путей, характеризующийся отсутствием передней брюшной стенки и передней стенки мочевого пузыря, а также расхождением лонного сочленения (диастаз). Через дефект передней брюшной стенки пролабирует слизистая оболочка. В нижней части обнаженной слизистой оболочки расположены устья мочеточников, из которых постоянно выделяется моча. Пуповина впадает низко в верхний край дефекта передней брюшной стенки.
Экстрофийные пороки нижних мочевых путей делят на классическую экстрофию мочевого пузыря и экстрофию клоаки. У мальчиков экстрофия мочевого пузыря сочетается с расщеплением мочеиспускательного канала (эписпадия). Экстрофия мочевого пузыря у девочек сопровождается расщеплением клитора, расщеплением или отсутствием мочеиспускательного канала, а также спайками больших и малых половых губ [1, 2].
В литературе экстрофия мочевого пузыря чаще всего описывается в комплексе с эписпадией, хотя имеются сообщения об изолированном поражении стенки мочевого пузыря, когда его шейка и мочеиспускательный канал сформированы. Такая патология называется неполной экстрофией, или переднепузырным свищом. При неполной экстрофии патология половых органов отсутствует [3, 4]. Наиболее тяжелой и редкой формой порока является экстрофия клоаки, при которой расщепление распространяется не только на урогенитальную область, но и на терминальный отдел кишечника [5, 6].
Впервые экстрофию мочевого пузыря, как врожденный порок развития, описал Schenk von Grafenberg в 1597 г. В 1780 г. Chaussier впервые использовал термин “экстрофия”. Упоминания об экстрофии мочевого пузыря обнаружены на ассирийских табличках, сделанных 2000 лет до н. э. [7]. Частота экстрофии мочевого пузыря составляет 0,25-0,5 на 10 тыс. новорожденных. Соотношение классической экстрофии мочевого пузыря у мальчиков и девочек 3:1 [1, 8]. При экстрофии мочевого пузыря встречаются сопутствующие врожденные аномалии – паховые грыжи (у 56 % мальчиков, у 15 % девочек), крипторхизм (20 %), колоректальные аномалии (1,8 %) и др. [1, 2]. Экстрофия мочевого пузыря может входить в состав комплекса OEIS (omphalocele, extrophy, imperforate anus, spinal defects), OMIM 258040.
Пренатальная диагностика экстрофии мочевого пузыря возможна уже при первом скрининговом обследовании в 11-14 нед беременности, когда в норме полость мочевого пузыря начинает наполняться мочой. Визуализация мочевого пузыря обязательно входит в стандартные протоколы исследования пренатального скрининга.
Эмбриопатогенез
Экстрофия мочевого пузыря формируется на 4-5-й неделе эмбриогенеза, когда на 28-32-й день происходит каудальная миграция мембраны клоаки. В то же время формируется передняя брюшная стенка, однако если мезенхима не переходит из одного клеточного слоя нижней брюшной стенки в другой, то это приводит к нестабильности клоакальной мембраны. Преждевременный разрыв мембраны клоаки приводит к комплексу “подпупочных” аномалий. Разрыв клоакальной мембраны после полного разделения “урогенитальной” части от пищеварительного тракта приводит к формированию классической экстрофии мочевого пузыря.
Если повреждение мембраны происходит до того, как спускается уроректальная перегородка, тогда это приводит к вывороту нижнего уретрального тракта и части пищеварительного тракта с формированием клоакальной экстрофии. Генетические факторы, связанные с экстрофией мочевого пузыря, на сегодняшний день не выявлены, однако существует гипотеза, что потеря экспрессии р63 из-за полиморфизмов очередности у промотера является фактором риска развития экстрофии мочевого пузыря [1, 9].
Ниже представлен случай диагностики экстрофии мочевого пузыря в III триместре беременности.
Материал и методы
Пациентка С.,18 лет, настоящая беременность первая, от первого брака, супруги соматически здоровы, профессиональных вредностей не имеют, наследственность не отягощена. На учете в женской консультации пациентка состояла с 9 нед беременности. Беременность протекала без осложнений. При скрининговом УЗ-исследовании в I и II триместрах по месту жительства ВПР и УЗ-маркеров хромосомных перестроек у плода не обнаружено.
При УЗ-обследовании в 34 нед беременности в женской консультации по месту жительства было обнаружено образование средней эхогенности размером 28x23x25 мм в области нижних отделов передней брюшной стенки. Женщина была направлена в медикогенетическое отделение МОНИИАГ с диагнозом: “ВПР плода, экстрофия мочевого пузыря?”.
УЗ-исследование проводилось на сканере WS80A (компании Samsung Medison) с использованием объемного датчика CV1-8A.
Результаты
При УЗ-исследовании обнаружен один живой плод женского пола в головном предлежании. Гестационный срок составил 34,4 нед. Фетометрические показатели плода соответствовали данному сроку. Патологических изменений плаценты и околоплодных вод не выявлено. При исследовании мочевой пузырь в типичном месте не визуализировался.
В нижних отделах передней брюшной стенки в надлобковой области визуализировалось эхогенное образование размером 30x28x25 мм (рис. 1, 2). Определялось низкое впадение пуповины. Почки плода визуализировались в типичном месте, без структурных изменений. Патологических изменений других органов не было выявлено.
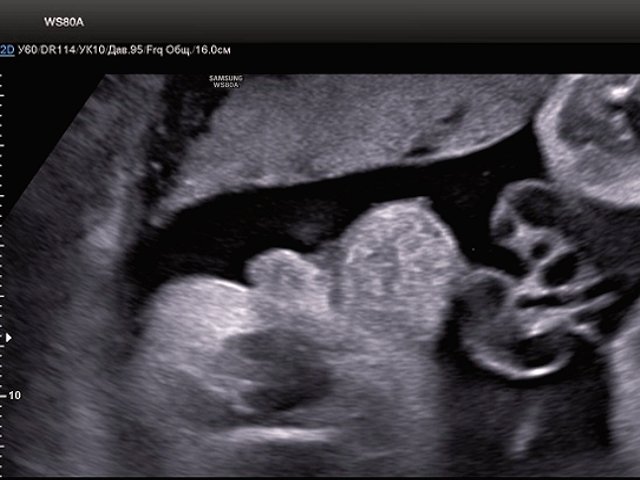
Рис. 1. Эхогенное образование в нижнем отделе передней брюшной стенки (экстрофированный мочевой пузырь).
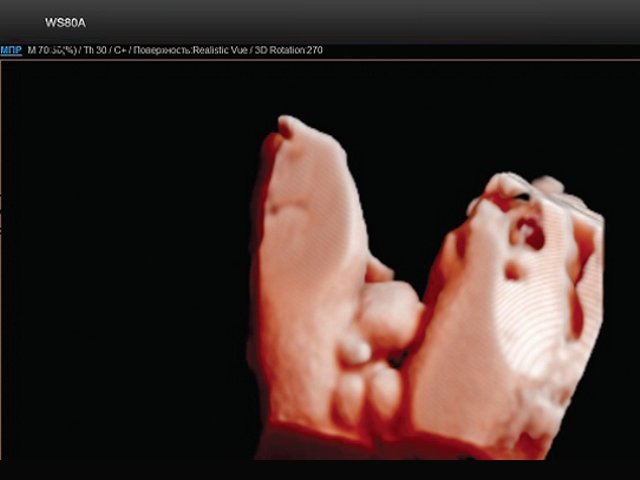
Рис. 2. Экстрофия мочевого пузыря в сочетании с отсутствием видимой патологии наружных половых органов (режим трехмерной реконструкции).
Поставлен диагноз: “Беременность 34,4 нед. ВПР плода – экстрофия мочевого пузыря”.
Обсуждение
Пренатальными УЗ-признаками экстрофии мочевого пузыря являются: отсутствие визуализации мочевого пузыря при нормальном количестве околоплодных вод, структурно неизмененные почки, визуализация эхогенного образования в надлобковой области, аномалии строения половых органов. Использование ЦДК является дополнительным инструментом для диагностики экстрофии мочевого пузыря. В норме пупочные артерии проходят вдоль стенки мочевого пузыря при поперечном сканировании нижней части живота. Для экстрофии мочевого пузыря характерно низкое впадение пуповины, при котором артерии охватывают образование в надлобковой области. При отсутствии визуализации мочевого пузыря в типичном месте необходимо провести повторное сканирование через 30-40 мин для адекватной оценки его расположения и степени наполнения.
Изолированная экстрофия мочевого пузыря, как правило, не сочетается с хромосомными перестройками у плода и не требует пренатального кариотипирования.
В данном клиническом наблюдении экстрофия мочевого пузыря была диагностирована у плода женского пола, что встречается значительно реже, чем у плодов мужского пола. Кроме того, отсутствие выраженной деформации наружных половых органов позволяет предположить неполную форму экстрофии. Оценка анатомии мочевого пузыря включена в протокол обязательного скринингового обследования во всех триместрах беременности. Отсутствие визуализации мочевого пузыря в типичном месте должно насторожить врачей УЗ-диагностики. Однако часто экстрофия мочевого пузыря диагностируют лишь в III триместре беременности.
После рождения детям с экстрофией мочевого пузыря требуется многоэтапная сложная хирургическая коррекция. Процент неудовлетворительных отдаленных результатов, к сожалению, остается на сегодняшний день очень высоким, как правило, вследствие присоединения таких осложнений, как нарушение функции тазовых органов: недержание мочи, рубцовая деформация половых органов, половая дисфункция, выраженная деформация передней брюшной стенки, уретерогидронефроз III-IV степени, непрерывно рецидивирующий пиелонефрит со снижением функции почек, хроническая почечная недостаточность и др. [4, 7]. Огромной и сложной проблемой остается медико-социальная реабилитация больных с экстрофией мочевого пузыря.
Заключение
Сложности ранней диагностики связаны с невыраженными УЗ-проявлениями достаточно тяжелой патологии. Четкое соблюдение алгоритма скрининговых УЗ-исследований анатомии плода в 11-14 и 20-22 нед беременности позволяет диагностировать экстрофию мочевого пузыря. При выявлении экстрофии мочевого пузыря у плода необходимо проведение медико-генетического консультирования с оформлением пренатального консилиума. Требуется тщательное разъяснение родителям сути выявленной патологии, а также информация о частых послеоперационных отдаленных последствиях и осложнениях как физического, так и психогенного генеза.
Литература
- Лопаткин Н.А., Пугачев А.Г. Пороки развития мочевого пузыря и уретры. В кн. Детская урология. Руководство. М.: Медицина, 1986. С. 207-242.
- Gearhart J.P. Criteria for the prenatal diagnosis of classic bladder exstrophy / J.P. Gearhart, J. Ben-Chaim, R.D. Jeffs // Obstet. Gynecol. 1995. Jun. 1. V. 85. № 6. P. 961-964.
- Михельсон А.И. Оперативное лечение недержания мочи на почве врожденных аномалий мочевой системы. Минск, Госсиздат БССР. 1957.
- Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей: автореф. дисс. докт. мед. наук. СПб, 1996.
- Ахунзянов А.А. Диагностика и лечение врожденной клоаки у детей // Хирургия. 1976. № 9. С. 98-101.
- Захаров Н.Л. Дефекты передней брюшной стенки у новорожденных // Хирургия. 1986. № 6.
- Hollowell J.G., Ransley P.G. Surgical management of Incontinence in bladder exstrophy // Brit. J. Urol. 1991. V. 68. № 5. P. 543-548.
- Kockum C.C., Hansson E.E., Stenberg A.et. al. Bladder exstrophy in Sweden-a long-term follow-up study // Eur. J. Pediatr. Surg. 1996. V. 6. P. 208-211.
- Баиров Г.А., Ахметджанов И.А., Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей // Вестник хирургии. 1986. Т. 136. № 6. С. 105-108.

УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Источник
Экстрофия мочевого пузыря – это порок развития мочеполовой системы, при котором формирование мочевого пузыря и передней брюшной стенки в его проекции остается незавершенным. С рождения наблюдается открытая и вывернутая наружу слизистая оболочка задней стенки мочевого пузыря, а также постоянное отделение и стекание мочи из открывающихся в нижней части органа протоков мочеточников. Экстрофия мочевого пузыря часто сочетается с пороками наружных и внутренних половых органов, мочеточников и почек. Диагностируется по характерным внешним признакам, дополнительно проводится рентгенологическое и УЗИ-обследование. Лечение оперативное, выполняются реконструктивно-пластические и заместительные операции.
Общие сведения
Экстрофия мочевого пузыря – одна из наиболее часто встречаемых аномалий развития мочеполовой системы. Частота в популяции – 1 случай на 30-50 тысяч новорожденных, примерно 1/5 часть пациентов имеет сочетанные пороки развития. В большей степени страдают мальчики, по данным разных авторов распространенность патологии среди них в 2-6 раз выше, чем среди девочек.
Специалисты в сфере педиатрии и хирургии сталкиваются с большими трудностями в лечении экстрофии мочевого пузыря, хотя первые операции для коррекции этой аномалии были предложены еще в 1960-х годах. Реконструкция и пластика не приводят к излечению. Сохраняющееся недержание мочи значительно ухудшает качество жизни ребенка, а частые восходящие инфекции становятся причиной хронической почечной недостаточности, представляющей серьезную опасность для жизни.

Экстрофия мочевого пузыря
Причины
Конкретной причины данной аномалии развития не выявлено, патология считается мультифакториальной. Доказана генетическая предрасположенность к некоторым сочетанным порокам органов брюшной полости, в числе которых присутствует и экстрофия мочевого пузыря. Кроме того, повышает риск развития аномалии воздействие различных токсических и инфекционных агентов во время беременности, в частности, курение, внутриутробные инфекции, некоторые медикаменты и т. д. Травмы плода также могут способствовать нарушению правильного эмбриогенеза с развитием пороков.
Патогенез
Основной патогенетический момент экстрофии мочевого пузыря – задержка обратного развития клоакальной перегородки, которая препятствует внедрению мезодермального листка между наружным и внутренним эмбриональными слоями. Это приводит к тому, что процесс формирования стенок мочевого пузыря оказывается незавершенным, и орган остается открытым и вывернутым наружу. Описанные процессы в норме протекают на 4-6 неделе эмбрионального развития, поэтому воздействие тератогенных факторов наиболее опасно в самом начале беременности. Впрочем, это касается не только экстрофии мочевого пузыря, но и большинства пороков развития.
Симптомы
Проявления порока визуально заметны сразу после рождения. Неонатолог при осмотре новорожденного обращает внимание на ярко-красную слизистую оболочку мочевого пузыря, которая замещает отсутствующую часть передней брюшной стенки. Слизистая, как правило, имеет обычную морфологию, но возможно и псевдопапилломатозное изменение. В нижней части заметны отверстия мочеточников, из которых постоянно выделяется моча.
С течением времени основной проблемой при экстрофии мочевого пузыря становится раздражение окружающих тканей мочевыми солями, постоянная мацерация вокруг открытого участка и в области бедер. Инфицирование слизистой оболочки мочевого пузыря является причиной восходящей инфекции мочеточников и почек.
Экстрофия мочевого пузыря часто сочетается с аномалиями верхних мочевыводящих путей. Кроме того, экстрофии всегда сопутствует расхождение лобкового симфиза. Вследствие анатомических различий у мальчиков и девочек наблюдаются разные изменения в соседних органах. У мальчиков встречается расщепление пещеристых тел или их редукция, у девочек – расщепление клитора, аномалии развития влагалища.
Диагностика
В последние годы активно развиваются методы антенатальной диагностики данного порока. Экстрофия мочевого пузыря может быть заметна уже на втором УЗИ-скрининге, однако такое случается не всегда. Часто аномалия развития обнаруживается только после рождения. Поскольку симптоматика специфична, диагноз не вызывает сомнений.
Обязательно проведение рентгенографии брюшной полости для выявления сочетанных пороков, в первую очередь, в мочевыделительной системе, но также в кишечнике и спинном мозге (наиболее характерные сочетания с экстрофией мочевого пузыря). С этой же целью проводится УЗИ. Рекомендована экскреторная урография, которая позволяет убедиться в целостности и правильном развитии мочеточников и почек.
Лечение экстрофии мочевого пузыря
Лечение оперативное. Тип операции зависит от степени экстрофии мочевого пузыря, а именно – от размеров вывернутой части органа и, соответственно, отсутствующего сегмента передней брюшной стенки, а также от сопутствующих пороков развития. Если размер дефекта не превышает 4 см, проводится реконструктивно-пластическое вмешательство, цель которого – закрытие дефекта с помощью близлежащих тканей и восстановление целостности мочевого пузыря. Этого достаточно, поскольку гистологически орган развит правильно, несмотря на патологию в анатомии.
В случае больших размеров дефекта создается искусственный мочевой пузырь, который может выполнять функцию резервуара и опорожняться по желанию. Также часто мочеточники выводятся в сигмовидную кишку (уретеросигмостомия) – это обязательная мера в случае их расщепления.
Большую проблему для детских хирургов представляет расхождение костей таза при экстрофии мочевого пузыря. Накопленный врачебный опыт говорит о высокой частоте неудовлетворительных результатов операций, что связано с большим количеством сочетанных пороков и значительным дефектом передней брюшной стенки.
Прогноз и профилактика
Прогноз для выздоровления сомнительный. Неоперированные пациенты редко доживают до 10 лет. Что касается успеха оперативного лечения, то 20-80% проведенных вмешательств приводят лишь к незначительному улучшению. Нарушения уродинамики продолжают прогрессировать, сохраняется недержание. Риск развития восходящей инфекции остается высоким.
Профилактика экстрофии мочевого пузыря возможна в антенатальном периоде, еще лучше – на этапе планирования беременности, чтобы максимально исключить воздействие тератогенных факторов, особенно на этапе закладки основных органов и систем, то есть в первые 4-8 недель внутриутробного развития.
Источник
МКБ-10
Q64.1Экстрофия мочевого пузыря
1. Клинические рекомендации “Экстрофия мочевого пузыря у детей” (Союз педиатров России).
Определение
Эпидемиология
Этиология
Классификация
Диагностика
Лечение
Прогноз
Профилактика
Жалобы и анамнез
Диагноз экстрофия обычно устанавливается сразу после рождения ребенка при обычном осмотре новорожденного.
Картина ЭМП достаточно специфична. Брок и О’Нил в 1988 г. писали, что ЭМП создает впечатление, как будто пациент получил рассечение тканей по средней линии от пупка до полового члена. При этом наблюдается расхождение кожи и мышц передней брюшной стенки, передней стенки мочевого пузыря и мочеиспускательного канала. Ткани раздвинуты в стороны, как «страницы раскрытой книги».
ЭМП может быть диагностирована еще до рождения ребенка – во втором триместре примерно после 20 недели беременности (чаще на 28-ой неделе) с помощью ультразвукового исследования (УЗИ).
Признаками экстрофии на УЗИ могут являться:
- на нескольких процедурах не видна тень мочевого пузыря (в ходе процедуры не видно, как он наполняется и опорожняется);
- избыточные массы ткани (выпуклость) на передней брюшной стенке под пуповиной;
- более низкое расположение пуповины;
- более высокое положение ануса;
- диастаз лонных костей (редко могут различить);
- измененные гениталии.
Эти и другие признаки могут сигнализировать специалисту УЗИ, что что-то не так и заподозрить экстрофию. Очевидными плюсами прeнатальной диагностики экстрофии являются:
- возможность для родителей и родственников узнать больше о пороке;
- возможность подготовиться морально и физически к предстоящим испытаниям, связанным с транспортировкой в больницу (зачастую приходится лететь на самолете в другой город), операцией, длительным пребыванием ребенка в клинике (обычно месяц от рождения);
- возможность связаться заранее с хирургом и обсудить все тонкости предстоящего лечения.
Физикальное обследование
При рождении ребенка с ЭМП диагноз достаточно легко поставить на основании осмотра.
Обычно, но не всегда, ЭМП ассоциируется со следующими изменениями в анатомии органов новорожденного:
- Эписпадия – уретра укорочена и расщеплена по передней стенке по всей или части своей длины. Сфинктер мочевого пузыря также расщеплен, раскрыт. Таким образом, у мальчиков мочеиспускательный канал и головка полового члена расщеплены по дорсальной поверхности, а у девочек уретра тоже не сформирована и выходит между расщепленным клитором и половыми губами;
- Дорсальное искривление полового члена: пенис подтянут к животу;
- Шейка и сфинктер мочевого пузыря отсутствуют;
- Малый объем площадки мочевого пузыря. Даже после закрытия мочевого пузыря местными тканями он не может в начале удерживать нормальный, достаточный объем мочи, но при благоприятных условиях мочевой пузырь может расти;
- Неправильное расположение устьев мочеточников, что может привести к пузырно-мочеточниковому рефлюксу (ПМР) – обратному забросу мочи из мочевого пузыря в почки (последний присутствует у 90 % пациентов);
- Диастаз лонных костей при ЭМП. Диастаз может различаться по размеру. За счет диастаза – прямая мышца на каждой стороне прикрепляется к лонному бугорку, при этом происходит смещение внутреннего пахового кольца таким образом, что он располагается непосредственно над наружным паховым кольцом. Данная анатомическая особенность обусловливает частые непрямые паховые грыжи при этой патологии (80% мальчиков и 10% девочек);
- Уретра, влагалище (у девочек), пенис (у мальчиков) несколько короче, нежели обычно;
- Более короткое расстояние пупок-анус: анус расположен чуть выше (ближе к мошонке у мальчиков и влагалищу у девочек), что никак не отражается на функции кишечника; а пупок с рождения расположен наоборот более низко, чем обычно.
В ряде случаев для определения пола ребенка и расположения органов таза необходима консультация и обследование узкого специалиста.
Лабораторная диагностика
Для подтверждения диагноза не требуется.
- Для определения наличия нарушения функции почек перед реконструктивными операциями рекомендуется проведение стандартного биохимического и общего анализов крови, общего анализа мочи.
Сила рекомендации – 1 (достоверность доказательств – В)
Инструментальная диагностика
- Рекомендуется проведение ультразвукового исследование органов мочевыводящей системы.
Сила рекомендаций – 1 (достоверность доказательств – С)
Комментарии:
Для исключения сопутствующих врожденных пороков развития.
- Рекомендуется проведение ЭХО-КГ.
Сила рекомендаций – 1 (достоверность доказательств – С)
Комментарии:
Для исключения сопутствующих врожденных пороков развития сердечно-сосудистой системы перед реконструктивной операцией.
- Рекомендуется проведение по показаниям (а также с учетом выявленных изменений при УЗИ) дополнительных диагностических мероприятий:
- Экскреторная урография;
- Микционная цистоуретрография (на последующих этапах реконструкции для исключения ПМР);
- Радионуклидное исследование мочевыводящей системы (статическая и динамическая нефросцинтиграфия);
- Допплерография сосудов почек;
- Цистоскопия;
- Магнитно-резонансная томография (МРТ) и компьютерная томография;
- Уродинамическое обследование.
Сила рекомендаций – 1 (достоверность доказательств – С)
Комментарии:
Комбинированное уродинамическое обследование включает выполнение урофлоуметрии и ретроградной цистометрии для определения формы и степени нарушения функции мочевого пузыря и назначения медикаментозной терапии и физиотерапии.
Иная диагностика
Не требуется.
Консультации специалистов
- Рекомендуются консультации:
- генетика;
- гинеколога при подозрении на соответствующую патологию;
- ортопеда для исключения/подтверждения сопутствующих аномалий развития костно-мышечной системы.
Сила рекомендаций – 1 (достоверность доказательств – С)
Компьютерная томография (КТ)
Ультразвуковое исследование (УЗИ)
Эхокардиография (ЭхоКГ)
Биохимический анализ крови
Общий анализ крови
Общий анализ мочи
Источник
