Диоксидин для инстилляций в мочевой пузырь
В амбулаторной урологии, наверное, второй излюбленной процедурой после массажа предстательной железы, являются инстилляции лекарственных средств в мочевой пузырь. Причем выполняется эта процедура и мужчинам, и женщинам любого возраста, а спектр заболеваний вообще с трудом поддается перечислению – и хронические циститы, и простатиты, и уретриты, и дизурии неясной этиологии. Возможно урологи таким образом выражают свои большие надежды на местную терапию. До недавнего времени вводимых препаратов было мало – протаргол, облепиховое масло, гидрокортизон, они применялись как отдельно, так и в составе «болтушек». В последние год-два стали появляться препараты, которые предназначены специально для внутрипузырной терапии и характеризуются созданием высокой концентрации действующего вещества на поверхности уротелия. Тем не менее, для выполнения инстилляций лекарственных веществ в мочевой пузырь должны быть строгие показания. Мы задали вопросы, касающиеся инстилляций, известному урологу, имеющему большой практический опыт лечения заболеваний нижних мочевых путей д.м.н., проф. кафедры урологии и хирургической андрологии РМАПО Любови Александровне Синяковой.
– Любовь Александровна, как Вы считаете, есть ли место внутрипузырным инстилляциям (ВИ) в современной урологии?
– Безусловно, ВИ являются эффективным методом лечения, чаще всего в составе комбинированной терапии.
– Кому, каким пациентам, с какой патологией показаны ВИ?
– Как правило, это пациентки с рецидивирующими инфекциями нижних мочевых путей, поствоспалительными изменениями в мочевом пузыре по типу лейкоплакии, больные интерстициальным циститом. Отдельную группу составляют больные с опухолями мочевого пузыря, которым показана БЦЖ-терапия, внутрипузырное введение препаратов после трансуретральной резекции мочевого пузыря.
– Есть ли противопоказания для ВИ?
– Противопоказаниями для ВИ являются острые воспалительные заболевания мочевых путей, стриктуры уретры.
– Какие осложнения могут возникнуть после ВИ? Как их устранить?
– ВИ могут вызвать обострение хронического уретрита, рецидивирующего цистита у женщин, уретральную лихорадку у мужчин, при наличии пузырно-мочеточникового рефлюкса – развитие восходящего пиелонефрита, также может возникнуть рефлюкс. Для профилактики развития осложнений необходимо строго соблюдать показания к выполнению ВИ, не нарушать методику, по показаниям проводить антибактериальную профилактику.
– Применяются ли ВИ у мужчин для лечения простатита, уретрита, цистита и т. д.? Какие осложнения у них могут возникнуть?
– ВИ используются в основном у женщин с воспалительными заболеваниями нижних мочевых путей.
– Есть ли патоморфологическое обоснование применения ВИ?
– Для решения вопроса о необходимости выполнения ВИ обязательным условием служит выполнение цистоскопии с биопсией, поскольку одной цистоскопии для принятия решения о выборе метода лечения недостаточно. Одним из морфологических обоснований для применения инстилляций является наличие плоскоклеточной метаплазии эпителия мочевого пузыря без ороговения с признаками хронического воспаления в подслизистом слое, что исключает истинную лейкоплакию, являющуюся «предраком», подтверждает наличие поствоспалительных изменений в мочевом пузыре. Существуют также морфологические признаки интерстициального цистита/синдрома болезненного мочевого пузыря, при котором также показаны ВИ.
– Какие препараты применяют с целью ВИ?
– Гепарин, диметилсульфоксид (ДМСО), диоксидин. При раке мочевого пузыря – противоопухолевые препараты, вакцина БЦЖ.
В настоящее время появились препараты гиалуроновой кислоты – например, Уро-гиал, который показал положительные результаты при лечении хронических циститов, в том числе интерстициальных.
– Надо ли выполнять цистоскопию и биопсию с целью подтверждения диагноза до ВИ? Можно ли ограничиться только цистоскопией?
– Для оценки эффективности ВИ необходимо, прежде всего, оценивать клиническую картину, анализировать динамику симптомов заболевания. Так как ВИ чаще всего используются в составе комбинированной терапии, вопрос о цистоскопии решается индивидуально.
– Как Вы относитесь к инстилляциям протарголом? Почему их нежелательно применять?
– К использованию протаргола я отношусь отрицательно. Проведены экспериментальные исследования, которые выявили развитие склеротических изменений в мочевом пузыре на фоне указанных ВИ.
Таким образом, можно определить следующие положения по ВИ:
- Цель ВИ: восстановление муцинового слоя, регрессия плоскоклеточной метаплазии.
- Показания: рецидивирующие инфекции нижних мочевых путей, поствоспалительные изменения в мочевом пузыре по типу лейкоплакии, интерстициальный цистит, рак мочевого пузыря.
- Противопоказания: острые воспалительные заболевания мочевых путей, стриктуры уретры, опухоли мочевыводящих путей.
- Осложнения ВИ: обострение хронических воспалительных процессов в мочеполовых путях (хронический уретрит, простатит, цистит), при наличии пузырно-мочеточникового рефлюкса – восходящий пиелонефрит.
- Препараты для ВИ:
Уро-гиал, гепарин, лидокаин, диметил-сульфоксид, кеналог, гидрокортизон, лонгидаза.
Материал подготовлен В. А. Шадеркиной
УС №1(17) 2012
Источник

Яков Борисович Миркин. Врач-уролог отделения восстановительного лечения ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России.
«Урология сегодня» № 6 (22) 2012
Внутрипузырная терапия хронического цистита вообще и бактериального в частности давно привлекает внимание урологов, как в России, так и за рубежом.
Действительно, у местной терапии есть преимущества:
- Возможность создать достаточно высокую концентрацию препарата в месте введения.
- Минимизация системных побочных эффектов.
- Обеспечение комплаенса, поскольку процедуры обычно проводит лечащий врач.
- Некоторые препараты вообще невозможно ввести иным путем (ботулинический токсин, резинифератоксин, гиалуроновая кислота, диоксидин, димексид и пр.).
Однако есть и недостатки:
- Отсутствие стандартов внутрипузырной терапии.
- Необходимость регулярной катетеризации в процессе лечения.
- Недостаточное время воздействия.
За рубежом в основном применяются смеси глюкокортикоидов, анестетиков и протекторов уротелия (гепарин, гиалуронат натрия). Например, R. Moldwin рекомендует коктейль из 20 мл 0,5 % маркаина, 20 мл 2 % лидокаина, 10 000 ЕД гепарина, 40 мг триамцинолона и 80 мг гентамицина.
Видимо, урологическому сообществу еще предстоит разработать методические рекомендации для внутрипузырной терапии. Возможно, имеет смысл создать рабочую группу или экспертный совет.
А пока, давайте попробуем разобраться в основных целях и принципах внутрипузырной терапии хронического бактериального цистита.
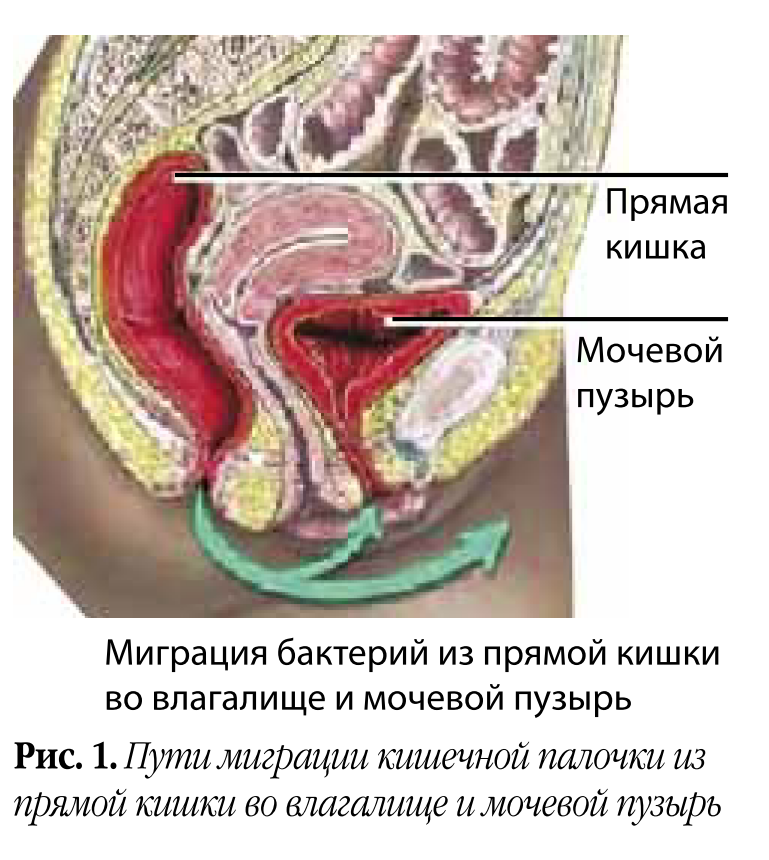
 Во-первых, это патогенетическая терапия. Основным возбудителем цистита до недавнего времени считалась E. coli (рис. 1), точнее ее уропатогенные штаммы, обладающие инструментами вирулентности: гиалуронидазой для разрушения гликозаминогликанового слоя мочевого пузыря и фимбриями для прикрепления к уротелию.
Во-первых, это патогенетическая терапия. Основным возбудителем цистита до недавнего времени считалась E. coli (рис. 1), точнее ее уропатогенные штаммы, обладающие инструментами вирулентности: гиалуронидазой для разрушения гликозаминогликанового слоя мочевого пузыря и фимбриями для прикрепления к уротелию.
Перорального применения фторхинолонов было вполне достаточно для ее элиминации. Однако, в последнее время доказана возможность образования микробных ассоциаций в уротелии, защищенных биопленками. Такие микроколонии могут содержать несколько десятков видов микроорганизмов (в том числе анаэробов) с разделением функций. Проникновение в них антибиотиков при системном применении затруднено (рис. 2).

Таким образом, потенциальный препарат для внутрипузырной антибактериальной терапии должен обладать широким спектром действия, проникать в уротелий и микроколонии.
Во-вторых, необходимо в короткие сроки купировать болевой синдром и поллакиурию. Для этого можно использовать местные анестетики (лидокаин, маркаин) или М-холинолитики.
В-третьих, представляется целесообразным сформировать местный иммунитет.
В четвертых, необходимо восстановить поврежденный уротелий.
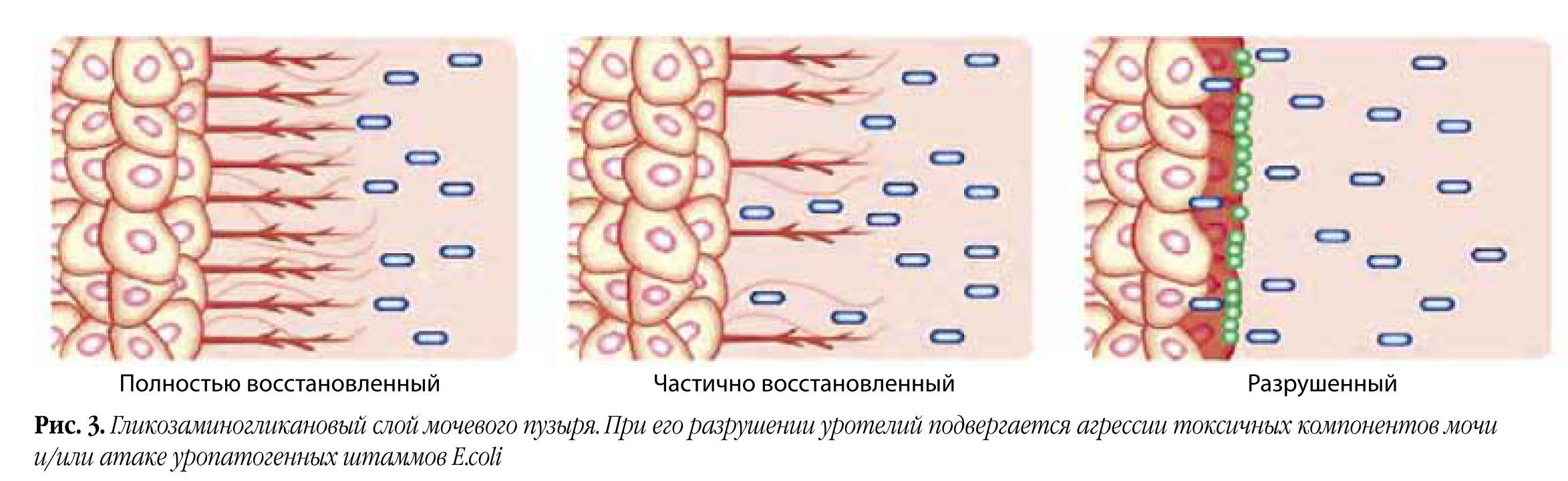
И наконец, в пятых – восстановить гликозаминогликановый слой мочевого пузыря, препятствующий адгезии бактерий (рис. 3).
Одним из главных недостатков внутрипузырной терапии является слабая адгезия препаратов к уротелию. То есть, они выводятся из мочевого пузыря вскоре после введения. Следовательно, необходимо обеспечить длительную адгезию, минимум 24 ч. Понятно, что такое продолжительное воздействие должен обеспечивать целый комплекс препаратов. Однако, фармакохимическое взаимодействие в таком «коктейле» достаточно трудно спрогнозировать и оценить. Кроме того, на разных этапах терапии требуется различное воздействие, которое, кстати, зависит еще и от динамики патологического процесса.
Поэтому совместно с группой биохимиков, которую возглавляет проф. Н.Д. Олтаржевская, мы решили разработать комплекс препаратов для внутрипузырной терапии хронического бактериального цистита.
В основу легла концепция 3 этапов терапии цистита.
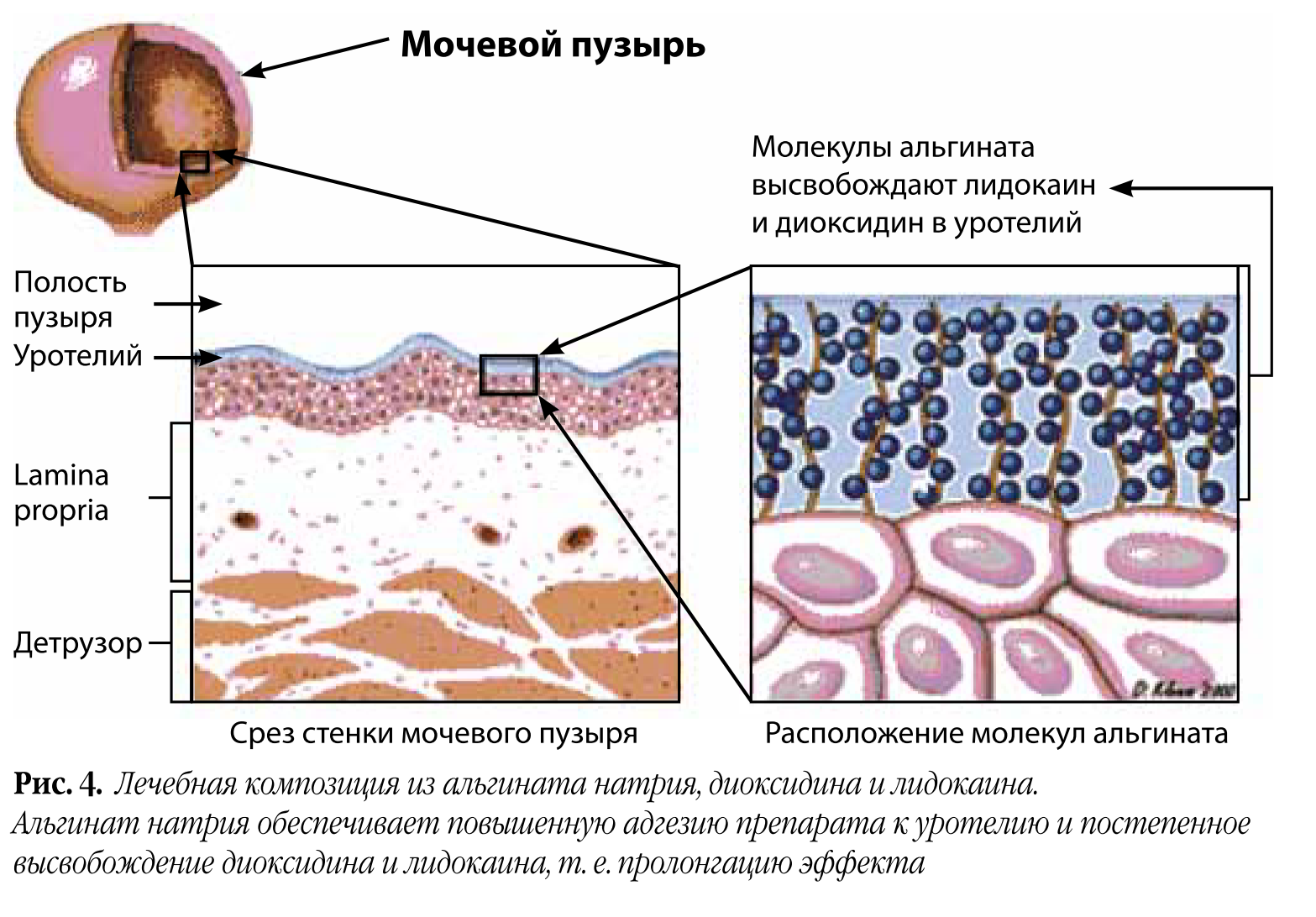
Первый этап – антибактериальная и симптоматическая терапия. Для этого мы выбрали комбинацию антибактериального препарата широкого спектра действия диоксидина и анестетика лидокаина. Для усиления адгезии к уротелию мы использовали альгинат натрия (рис. 4). Этот полисахарид обеспечивает длительное действие диоксидина и лидокаина.
Был проведен эксперимент in vitro по сравнению степени адгезии к коллагеновой мембране раствора гиалуроната натрия и комбинации гиалуроната натрия с альгинатом натрия. Степень адгезии композиции с альгинатом была соответственно в 8 раз выше, продолжительность действия также была больше. Таким образом, симптомы (боль и поллакиурия) исчезали через несколько минут после введения. Длительность действия составила от 24 до 48 ч.
Данная композиция (диоксидин, лидокаин, альгинат натрия) зарегистрирована под названием Колетекс-АДЛ. В урологии применяется под торговой маркой УРОЛАЙН-АДЛ (шприцы объемом 20 мл.).
Что касается усиления диффузии в уротелий – этого можно добиться использованием димексида (ДМСО).
Поскольку в различных клинических ситуациях возможно использование различных методик, было решено не добавлять димексид в Колетекс-АДЛ, а создать отдельную композицию на основе димексида и альгината натрия (Колетекс-Д/УРОЛАЙН-Д). При необходимости во время инстилляции можно через тот же катетер ввести димексид.
Второй этап – репаративная и иммунокоррегирующая терапия. Для этого принято решение использовать комбинацию дерината и альгината натрия, так как деринат обладает следующим комплексом свойств.
В качестве иммуномодулятора:
- модулирует активность фагоцитов и прежде всего макрофагов;
- нормализует показатели клеточного иммунитета;
- нормализует показатели гуморального иммунитета.
В качестве репаранта и цитопротектора:
- предупреждает альтерацию, связанную со свободно-радикальным повреждением клеток;
- проявляет антиоксидантные и мембраностабилизирующие свойства;
- обладает высокой репаративной и регенераторной способностью. Для увеличения адгезионных свойств раствора также был применен альгинат натрия. Данный препарат зарегистрирован под названием Колетекс-ДНК/УРОЛАЙН-ДНК.
Третий этап – восстановление гликозаминогликанового слоя уротелия. Основным компонентом гликозаминогликанового слоя является гиалуроновая кислота (УРО-ГИАЛ (гиалуронат натрия)).
Таким образом, трехэтапная внутрипузырная терапия хронического бактериального цистита с использованием альгината натрия для усиления адгезии и пролонгации действия, димексида или внутрипузырного электрофореза с целью увеличения диффузии препаратов в уротелий, является перспективным способом лечения этой патологии. Необходимо проведение дополнительных исследований, оценивающих ее эффективность и безопасность.
Источник
А.Е. Пигарева, Н.А. Цап, С.Ю. Комарова, Н.П. Федорова, С.А. Мельникова, О.А. Костина, П.Л. Основин
ГОУ ВПО «Уральская государственная медицинская академия», Областная детская клиническая больница №1,
Детская городская клиническая больница №9 (г. Екатеринбург)
Актуальность проблемы
Цистит – инфекционно – воспалительное заболевание слизистой оболочки и подслизистого слоя мочевого пузыря с нарушением его функции является одним из наиболее частых проявлений инфекции мочевой системы у детей. Считается, что при остром цистите преимущественно поражаются слизистый и подслизистый слои, тогда как хронический воспалительный процесс затрагивает и более глубокий мышечный слой. Заболевание встречается у детей любого возраста и обоего пола, причем у девочек в 3- 5 раз чаще, чем у мальчиков, и главным образом, в возрасте от 4 до 12 лет. Ведущее место при возникновении первичного хронического цистита у девочек принадлежит анатомо – топографическим особенностям их мочеполовой системы: короткой уретре, близкому анатомическому расположению влагалища, ануса к наружному отверстию мочеиспускательного канала. Это создает благоприятные условия для распространения микрофлоры из этих органов в просвет мочевого пузыря. Для возникновения цистита, помимо проникновения бактерий в мочевой пузырь, необходимо влияние комплекса других факторов: грипп, ОРЗ, ветряная оспа, ФНК, авитаминозы, атопический дерматит, мацерации промежности и слизистой оболочки половых органов также хронические запоры. Важную роль в развитии цистита играют функционально- обструктивные нарушения уродинамики, врожденные и приобретенные заболеваниях верхних и нижних мочевых путей, таких как ПМР, УГН, ГН, клапан уретры. Способствуют этому и различные инструментальные эндоуретральные вмешательства (катетеризация мочевого пузыря, цистоскопия).
В отделении урологии ОДКБ №1 в течение года проходят лечение 110 детей с хроническими циститами из них 32 ребенка с плоскоклеточной метаплазией эпителия, в возрасте от 3 до 17 лет. В 85% случаев хронический цистит сочетается с нейрогенной дисфункцией мочевого пузыря и пузырно- мочеточниковым рефлюксом, в 10% – с гидронефрозом и уретерогидронфрозом и в 5% – сочетание цистита с МКБ, экстрофией мочевого пузыря и другими пороками мочеполовой системы. По половому признаку патология характерна для девочек и составляет 98%. Клинические проявления цистита определяются прежде всего его формой и течением, а также возрастом ребенка. Наиболее типичными жалобами являются следующие: нарушение ритма мочеиспускания, энурез, неудержание мочи, боли в нижних отделах живота и поясничной области.
При лабораторном исследовании в общем анализе мочи выявляется стойкая лейкоцитурия и бактериурия, в общем анализе крови- лейкоцитоз, повышение СОЭ, сдвиг лейкоцитарной формулы. При бактериологическом исследовании мочи в большинстве случаев выявляется E.coli, в титре более 105. Помимо общеклинических обследований, в стандарт обследования включается урофлоуметрию, по показателям которой выявляется нарушения ритма мочеиспусканий.
Основным методом диагностики циститов является эндоскопическое исследование- цистоскопия и биопсия слизистой мочевого пузыря. Эндоскопическая картина представлена отечной и гиперемированной слизистой мочевого пузыря, выраженным сосудистым рисунком и трабеккулярностью, буллезными разрастаниями. Гистологически определяются лимфангиоматоз, лимфоидные фолликулы со светлым центром размножения и плоскоклеточная метаплазия эпителия.
Материалы и методы
За период с 1999 по 2009 гг. в отделение урологии с диагнозом хронический цистит находилось на лечении 808 детей в возрасте от 5 до 18 лет, причем 98% составляли девочки. Характерными жалобами являются нарушение суточного ритма мочеиспусканий, энурез, неудержание мочи, рецидивирующие инфекции мочевой системы.
Всем детям проводилось комплексное лечение, которое включало антибактериальную терапию с учетом чувствительности или уроантисептики, сосудистую, метаболическую, антиоксидантную, иммунномоделирую-щую терапию, физиотерапевтические процедуры на область мочевого пузыря (электрофорез с цинком, эуфиллином, прозерином, ДМСО с фурадонином, амплипульс, МЛТ, ионофорез с тизолем, парафин- озокеритовые аппликации).
Основным методом лечения пациентов с хроническим циститом считается эндовезикальное введение композиционного препарата тизоля с 0,1% раствором диоксидина. Введение композиции осуществляется после опорожнения мочевого пузыря через уретральный катетер с помощью шприца в количестве 10 мл. с экспозицией 60 минут. Затем ребенку предлагается самостоятельно помочиться. Курс лечения составляет 10-14 дней. Применение этих препаратов позволяет в большинстве случаев добиваться длительной ремиссии пиелонефрита уже после первого курса внутрипузырных инстилляций, тогда как при ранее применявшейся схеме лечения требовалось 2-3 курса консервативного лечения. Кроме того, проведение инстилляций с тизолем позволяет избежать назначения дорогостоящих антибиотиков. В 75% наблюдений эффективность подтверждена стерильными посевами мочи. Нормализация клинико-лабораторных и эндоскопических данных наблюдается у 52% девочек, у 30% – после двух курсов лечения и у 18% – после трех курсов. Повторный эндоскопический и лабораторный контроль проводился через 3-4 месяца.
Таким образом, применение лекарственной композиций тизоля с диоксидином в лечении хронического цистита привело к уменьшению количества курсов с 5-6 до 2-3 и продолжительности самих курсов с 20-24 дней до 14. Отмечается высокая эффективность лекарственной композиции у подавляющего большинства детей (74 %) с хроническим циститом. Рекомендуется более широкое применение композиций тизоля в детской практике.
Источник
Интерстициальный цистит: консервативное лечение. Часть 2.
20.07.2018
В предыдущей статье мы поговорили о пероральной терапии. В этой статье продолжим тему консервативного лечения интерстициального цистита с помощью инстилляций в мочевой пузырь.
Сведения об авторах:
Миркин Я.Б. – заведующий отделением урогинекологии и нейроурологии ММЦ «УРО-ПРО», г. Краснодар, mirkom@yandex.ru
Mirkin Ya.B. – the of the department of urogynecology and neurourology MMC “URO-PRO”, Krasnodar, mirkom@yandex.ru
Инстилляции в мочевой пузырь
Преимуществом внутрипузырного введения препаратов является создание высокой концентрации действующего вещества в очаге поражения при минимуме побочных эффектов. Недостатками являются необходимость катетеризации, которая при интерстициальном цистите может быть болезненной, и риск инфекционных осложнений.
Лидокаин
Существует несколько публикаций об успешной терапии интерстициального цистита при помощи инстилляций лидокаина в мочевой пузырь [31, 32]. Подщелачивание раствора лидокаина улучшает его фармакокинетику [33].
Исследование C.L. Parsons показало, что инстилляция комбинации 1-2% лидокаина, гепарина и бикарбоната натрия приводит к немедленному купированию болевого синдрома, а также ирритативной симптоматики у 94% пациентов [34].
Согласно данным J.C.Nickel, инстилляции лидокаина и бикарбоната натрия в течение 5 дней приводят к улучшению состояния на период до 1 мес. [35].
Пентозан полисульфат
Пентозан полисульфат применяется также внутрипузырно вследствие низкой биодоступности при пероральном приеме. После 3 мес. терапии внутрипузырными инстилляциями пентозан полисульфата 40% пациентов сообщили о значительном улучшении, тогда как в группе, получавшей инстилляции плацебо (физиологический раствор), об улучшении сообщили только 20% [36].
Емкость мочевого пузыря повысилась только в группе, получавшей пентозан полисульфат. Через 18 мес. терапии об улучшении сообщали 80% в группе пентозан полисульфата и 40% в контрольной группе. В другом сравнительном рандомизированном исследовании женщины с интерстициальным циститом были разделены на 2 группы: принимавшие пентозан полисульфат перорально и его же внутрипузырные инстилляции; принимавшие пентозан полисульфат перорально и внутрипузырные инстилляции плацебо.
Курс инстилляций продолжался 6 нед., прием пентозан полисульфата per os продолжался до 12 нед. В обеих группах было продемонстрировано улучшение состояния пациенток, однако в группе, получавшей комбинированную терапию, оно оказалось более значимым [37].
Гепарин
Инстилляции гепарина в мочевой пузырь были предложены для защиты уротелия от воздействия ионов калия, а также для восстановления его защитного гликозаминогликанового слоя.
Половина пациентов с интерстициальным циститом, получавших инстилляции гепарина в течение 3 мес., сообщила об улучшении самочувствия [38]. Kuo et al. опубликовали результаты своего исследования, по их данным 80% участников с позитивным KCl-тестом отмечали улучшение после 3-х месяцев инстилляций гепарина [39].
Baykal et al. исследовали эффективность инстилляций гепарина в сочетании с электростимуляцией тибиального нерва и отмечали уменьшение болевого синдрома, поллакиурии и увеличение емкости мочевого пузыря [40].
Гиалуроновая кислота (гиалуронат натрия)
Гиалуронат натрия является природным протеогликаном, восстанавливающим дефекты гликозаминогликанового слоя мочевого пузыря.
О положительных результатах инстилляций гиалуроната натрия на 4-й нед. терапии сообщили 56% пациентов, и 71% – на 7-й нед. [41]. После 24-й нед. эффективность инстилляций гиалуроновой кислоты снижалась.
Nordling et al. и Kallestrup et al. опубликовали результаты 3-летнего наблюдения за пациентами, которые получали инстилляции гиалуроната натрия в течение 3 мес. [42, 43].
Положительный долговременный эффект продемонстрировали 2/3 пациентов. Еще одно исследование показало аналогичные результаты инстилляций гиалуроновой кислоты пациентам с положительным KCl-тестом [44]. Участники получали еженедельные инстилляции 40 мг гиалуроната натрия (50 мл 0,08% раствора) в течение 10 нед.
Болевой синдром оценивался по визуальной аналоговой шкале. Также в одном из исследований оценивались отдаленные результаты внутрипузырного применения гиалуроната натрия [45]. 50% респондентов сообщили о полной ремиссии без дополнительной терапии, а 41,7% – об улучшении после повторного курса лечения.
Хондроитинсульфат
Внутрипузырные инстилляции хондроитинсульфата продемонстрировали эффективность в 2 нерандомизированных пилотных исследованиях [46]. Steinhoff выполнял инстилляции хондроитинсульфата 1 р./нед. На протяжении 4 нед. и далее 1 р./мес. на протяжении 12 мес. [47]. Результаты после 3-12 нед. терапии были следующими:
– хороший эффект – у 46,2%,
– положительный эффект – у 15,4%,
– частичный эффект – у 30,8%, отсутствие эффекта – 7,7%.
Во втором исследовании пациенты были пролечены раствором хондроитинсульфата высокой концентрации (2%): 2 инстилляции в неделю на протяжении 2 нед. и затем 0,2% раствором 1 р./нед. в течение 4 нед., далее 1 р./мес. в течение 1 года [48].
Положительные результаты продемонстрировали 73,1% пациентов, время до достижения максимального эффекта составляло 4-6 месяцев. Поддерживающие инстилляции 2% раствором были более эффективны, чем раствором 0,2%.
Результаты сравнительных рандомизированных плацебо-контролируемых исследований показали, что эффективность инстилляций хондроитинсульфата (39,4%) выше по сравнению с эффективностью плацебо (22,6%), хотя разница была статистически недостоверна [49, 50].
Диметилсульфоксид
Эффективность инстилляций димексида при интерстициальном цистите была обнаружена эмпирически, однако сейчас является стандартным лечением. В плацебоконтролируемом исследовании пациенты получали инстилляции димексида 1 раз в 2 нед. – 8 инстилляций на курс.
Терапия оказалась эффективна по субъективной оценке в 53% случаев по сравнению 18% в группе плацебо. Объективное улучшение продемонстрировали 93% пациентов по сравнению с 35% соответственно [51].
Заключение
Несмотря на достаточное количество предлагаемых методов лечения, интерстициальный цистит все еще представляется практически неизлечимым заболеванием.
Таким образом, целью терапии является достижение более или менее длительной ремиссии либо адекватный контроль над болевым синдромом и поллакиурией. С этой целью чаще всего применяются:
I. Пероральная терапия:
– амитриптилин – с 12,5 мг 2 р./сут, при необходимости дозировку повышают до 100 мг/сут;
– атаракс – 25 мг 2-3 р./сут;
– пентозан полисульфат – не менее 900 мг/сут в 3 приема с продолжительностью курса лечения не менее 6 мес.;
– хондроитинсульфат – не менее 900 мг/сут в 3 приема, 6 мес.
II. Внутрипузырная терапия:
– лидокаин 1-2% раствор – инстилляции в мочевой пузырь 3-7 р./нед;
– глюкокортикоиды;
– димексид 5% – инстилляции в мочевой пузырь 2-3 р./нед., 8 инстилляций на курс лечения;
– гиалуронат натрия 0,08% или 0,12% раствор – инстилляции в мочевой пузырь 1-2 р./нед., до 24 инстилляций на курс лечения;
– гепарин – 10 000 Ед внутрипузырно 1-2 р./нед.;
– хондроитинсульфат 0,2%, 2% раствор – инстилляции в мочевой пузырь 1-2 р./нед., до 24 инстилляций на курс лечения.
Читать следующую статью
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Nickel JC. Opioids for chronic proitis and interstitial cystitis: lessons learned from the 11th World Congress on Pain. Urology. 2006 Oct;68(4):697-701.
2. Badenoch AW. Chronic interstitial cystitis. Br J Urol 1971 Dec;43(6):718-21.
3. Pool TL. Interstitial cystitis: clinical considerations and treatment. Clin Obstet Gynecol. 1967 Mar;10(1):185-91.
4. Soucy F, Gregoire M. Efficacy of prednisone for severe refractory ulcerative interstitial cystitis. J Urol. 2005 Mar;173(3):841-3;ion 3.
5. Theoharides TC. Hydroxyzine in the treatment of interstitial cystitis. Urol Clin North Am. 1994 Feb;21(1):113-9.
6. Seshadri P, Emerson L, Morales A. Cimetidine in the treatment of interstitial cystitis. Urology. 1994 Oct;44(4):614-6.
7. Theoharides TC. Hydroxyzine for interstitial cystitis. J Allergy Clin Immunol. 1993 Feb;91(2):686-7.
8. Theoharides TC, Sant GR. Hydroxyzine therapy for interstitial cystitis. Urology. 1997 May;49
9. Sant GR, Propert KJ, Hanno PM, et al. A pilot clinical trial of oral pentosan polysulfate and oral hydroxyzine in patients with interstitial cystitis. J Urol 2003 Sep;170(3):810-5.
10. Baldessarini R. Drugs and the treatment of psychiatric disorders. Goodman and Gilman’s the pharmacological basis of therapeutics / eds. New York: Macmillan; 1985.
11. Hand JR. Interstitial cystitis; report of 223 cases (204 women and 19 men). J Urol 1949 Feb;61(2):291-310.
12. Hanno PM, Buehler J, Wein AJ. Use of amitriptyline in the treatment of interstitial cystitis. J Urol 1989 Apr;141(4):846-8. 13. Kirkemo A, Miles B, Peters J. Use of amitriptyline in interstitial cystitis. J Urol 1990;143 (Suppl): 279A.
14. Van Ophoven A, Pokupic S, Heinecke A, Hertle L. A prospective, randomized, placebo controlled, double-blind study of amitriptyline for the treatment of interstitial cystitis. J Urol 2004 Aug;172(2):533-6.
15. Van Ophoven A, Hertle L. Long-term results of amitriptyline treatment for interstitil cystitis. J Urol 2005 Nov;174(5):1837-40.
16. Foster HE Jr, Hanno PM, Nickel JC et al. Effect of amitriptyline on symptoms in treatment naive patients with interstitial cystitis/painful bladder syndrome. J Urol 2010 May;183(5):1853-8.
17. Fritjofsson A, Fall M, Juhlin R et al. Treatment of ulcer and nonulcer interstitialcystitis with sodium pentosanpolysulfate: a multicenter trial. J Urol 1987 Sep;138(3):508-12.
18. Van Ophoven A, Heinecke A, Hertle L.Safety and efficacy of concurrent applicationof oral pentosan polysulfate and subcutaneous low-dose heparin for patients with interstitial cystitis. Urology. 2005 Oct;66(4):707-11.
19. Fersino S1, Fiorentino A, Giaj Levra N, Mazzola R, Ricchetti F, Di Paola G, Cavalleri S, Alongi F. mpact of Ialuril Soft Gels in reducing urinary toxicity during radical hypofractionated radiotherapy in proe cancer: a preliminary experience. Minerva Urol Nefrol. 2016 Feb;68(1):9-13. Epub 2015 Oct 22.
20. Warren JW, Horne LM, Hebel JR et al. Pilot study of sequential oral antibiotics for the treatment of interstitial cystitis. J Urol 2000 Jun;163(6):1685-8.
21. Oravisto KJ, Alfthan OS. Treatment of interstitial cystitis with immunosuppression and chloroquine derivatives. Eur Urol 1976;2(2):82-4.
22. Forsell T, Ruutu M, Isoniemi H et al. Cyclosporine in severe interstitial cystitis. J Urol 1996 May;155(5):1591-3.
23. Moran PA, Dwyer PL, Carey MP et al. Oral methotrexate in the management of refractory interstitial cystitis. Aust N Z J Obstet Gynaecol. 1999 Nov;39(4):468-71.
24. Sairanen J, Forsell T, Ruutu M. Long-term outcome of patients with interstitial cystitis treated with low dose cyclosporine A. J Urol 2004 Jun;171(6 Pt 1):2138-41.
25. Sairanen J, Tammela TL, Leppilahti M et al. Cyclosporine A and pentosan polysulfate sodium for the treatment of interstitial cystitis: arandomized comparative study. J Urol 2005 Dec;174(6):2235-8.
26. Hansen HC. Interstitial cystitis and the potential role of gabapentin. South Med J. 2000 Feb;93(2): 238-42.
27. Sasaki K, Smith CP, Chuang YC et al. Oral gabapentin (neurontin) treatment of refractory genitourinary tract pain. Tech Urol 2001 Mar;7(1):47-9.
28. Katske F, Shoskes DA, Sender M et al. Treatment of interstitial cystitis with a quercetin supplement. Tech Urol 2001 Mar;7(1):44-6.
29. Theoharides TC, Sant GR. A pilot open label study of Cystoprotek in interstitial cystitis. Int J Immunopathol Pharmacol. 2005 Jan-Mar;18(1):183-8.
30. Evans RJ, Moldwin RM, Cossons N et al. Proof of concept trial of tanezumab for the treatment of symptoms associated with interstitial cystitis. J Urol 2011 May; 185(5):1716-21.
31. Asklin B, Cassuto J. Intravesical lidocaine in severe interstitial cystitis. Case report. Scand J Urol Nephrol 1989;23(4):311-2.
32. Giannakopoulos X, Champilomatos P. Chronic interstitial cystitis. Successful treatment with intravesical lidocaine. Arch Ital Urol Nefrol Androl 1992 c;64(4):337-9.
33. Henry R, Patterson L, Avery N et al. Absorption of alkalized intravesical lidocaine in normal and inflamed bladders: a simple method for improving bladder anaesthesia. J Urol 2001 Jun;165(6 Pt 1):1900-3.
34. Parsons CL. Successful downregulation of bladder sensory nerves with combination of heparin and alkalinized lidocaine in patients with interstitial cystitis. Urology 2005 Jan;65(1):45-8.
35. Nickel JC, Moldwin R, Lee S et al. Intravesical alkalinized lidocaine (PSD597) offers sustained relief from symptoms of interstitial cystitis and painful bladder syndrome. BJU Int 2009 Apr;103(7):910-8.
36. Bade JJ, Laseur M, Nieuwenburg A et al. A placebo-controlled study of intravesical pentosanpolysulphate for the treatment of interstitial cystitis. Br J Urol 1997 Feb;79(2):168-71.
37. Davis EL, El Khoudary SR, Talbott EO et al. Safety and efficacy of the use of intravesical and oral pentosan polysulfate sodium for interstitial cystitis: a randomizeddouble-blind clinical trial.J Urol 2008 Jan;179(1):177-85.
38. Parsons CL, Housley T, Schmidt JD et al. Treatment of interstitial cystitis with intravesical heparin. BrJ Urol 1994 May;73(5):504-7.
39. Kuo HC. Urodynamic results of intravesical heparin therapy for women with frequency urgency syndrome and interstitial cystitis. J Formos Med Assoc 2001 May;100(5):309-14.
40. Baykal K, Senkul T, Sen B, et al. Intravesical heparin and peripheral neuromodulation on interstitial cystitis. Urol Int 2005;74(4):361-4.
41. Morales A, Emerson L, Nickel JC et al. Intravesical hyaluronic acid in the treatment of refractory interstitial cystitis. Urology 1997 May;49(5A Suppl):111-3.
42. Nordling J, Jorgensen S, Kallestrup E. Cysti for the treatment of interstitial cystitis: a 3-year followup study. Urology 2001 Jun;57(6 Suppl 1):123.
43. Kallestrup EB, Jorgensen S, Nordling J, et al. Treatment of interstitial cystitis with Cysti: a hyaluronic acid product. Scand J Urol Nephrol 2005;39(2):143-7.
44. Daha LK, Riedl CR, Lazar D et al. Do cystometric findings predict the results of intravesical hyaluronic acid in womenwith interstitial cystitis? Eur Urol 2005 Mar;47(3):393-7; ion 397.
45. Engelhardt PF, Morakis N, Daha LK et al. Long-term results of intravesical hyaluronan therapy in bladder pain syndrome/ interstitial cystitis. Int Urogynecol J Pelvic Dysfunct 2011 Apr;22(4):401-5.
46. Palylyk-Colwell E. Chondroitin sulfate for interstitial cystitis. Issues Emerg Health Technol 2006 May(84);1-4.
47. Steinhoff G. The efficacy of chondroitin sulfate 0.2% in treating interstitial cystitis. Can J Urol 2002Feb;9(1):1454-8.
48. Sorensen RB. Chondroitin sulphate in the treatment of interstitial cystitis and chronic inflammatory disease of the urinary bladder. Eur Urol 2003;Suppl 2:16-8.
49. Nickel JC, Egerdie B, Downey J et al. A real-life multicentre clinical practice study to evaluate the efficacy and safety of intravesical chondroitin sulphate for the treatment of interstitial cystitis. BJU Int2009 Jan;103(1):56-60.
50. Nickel JC, Egerdie RB, Steinhoff G et al. A multicenter, randomized, double-blind, parallel group pilot evaluation of the efficacy and safety of intravesical sodium chondroitin sulfate versus vehicle control inpatients with interstitial cystitis/painful bladder syndrome. Urology 2010 Oct;76(4):804-9.
51. Perez-Marrero R, Emerson LE, Feltis JT. A controlled study of dimethyl sulfoxide in interstitial cystitis. J Urol 1988 Jul;140(1):36-9.
Источник
