Цистит после рака шейки матки
Лучевой цистит – это специфическое поражение мочевого пузыря, возникающее в ответ на воздействие ионизирующего излучения на область малого таза.
Лучевая терапия является одним из основных методов лечения рака органов малого таза. При отсутствии регионарных метастазов она позволяет добиться полной или частичной регрессии опухоли более чем у 70% пациентов. При этом продолжительность жизни таких больных остается достаточно высокой.
Однако радиация действует не только на злокачественные клетки. В зону риска попадают ткани с высокой пролиферативной активностью, в частности, мочевой пузырь. Его слизистая отличается высокой чувствительностью к действию ионизирующего излучения, в результате чего возникает нарушение его тканевой структуры, кровоснабжения и иннервации, и, как следствие, развивается воспаление, кровотечения и изъязвления. Основные механизмы, лежащие в основе развития лучевого цистита следующие:
- Некротизирующие повреждения эпителия.
- Воспалительные реакции.
- Повреждение кровеносных сосудов, нарушение трофики и развитие ишемии.
- Присоединение бактериальной инфекции.
Чаще всего лучевые повреждения возникают при дистанционной терапии, когда невозможно защитить нецелевые органы. При брахитерапии такие осложнения возникают редко.
Классификация лучевых циститов
В зависимости от сроков возникновения симптоматики, выделяют следующие виды лучевого цистита:
- Острый лучевой цистит – развивается либо во время проведения ЛТ, либо в ближайшее время после ее окончания (до 100 дней).
- Хронический лучевой цистит. При нем симптомы возникают более, чем через 3 месяца после окончания лучевой терапии. У некоторых пациентов заболевание может обнаружиться даже через десятки лет после окончания лечения.
В зависимости от морфологических изменений выделяют:
- Телеангиоэктазии мочевого пузыря. При этом виде лучевого цистита возникают повреждения кровеносных сосудов. Они расширяются, сливаются между собой и образуют кровоточащие конгломераты.
- Катаральный цистит – при нем превалируют воспалительные процессы. Стенка мочевого пузыря отечна, гиперемирована, могут присутствовать единичные язвы и телеангиоэктазии.
- Лучевые язвы. Основным патологическим процессом является образование язв в стенке мочевого пузыря. Они имеют расширенные кровеносные сосуды, часть их поверхности может быть инкрустирована солями мочевой кислоты, фибрином или конкрементами.
- Инкрустирующий цистит – клинически и морфологически сходен с язвенным.
- Псевдорак – на месте лучевых повреждений образуется новообразование на широком основании. Его поверхность может быть покрыта фибринозным налетом или кристаллами солей. Необходима биопсия для дифдиагностики злокачественных процессов.
Симптомы лучевого цистита
- Учащенное мочеиспускание, в ряде случаев может доходить до 40 раз в сутки.
- Наличие примесей крови в моче. В ряде случаев это макрогематурия с появлением кровяных сгустков.
- Наличие патологических примесей в моче: «песок», соли, хлопья, слизь.
- Боли и рези во время мочеиспускания.
- Боли и рези внизу живота, в области лона.
Диагностика лучевого цистита
Диагностика лучевого цистита должна быть комплексной и включать следующие элементы:
- Цистоскопия – эндоскопическое исследование мочевого пузыря. Оно позволяет рассмотреть стенку мочевого пузыря и дифференцировать вид лучевого поражения и оценить его степень.
- Уродинамические исследования позволяют оценить функцию мочевого пузыря и сфинктера уретры. С этой целью проводят урофлуориметрию, цистометрию наполнения, электромиографию и другие тесты.
- Биопсия. Исследование фрагмента ткани стенки мочевого пузыря позволит провести дифференциальную диагностику лучевого цистита. Особенно это актуально при псевдораке.
Методы лечения лучевого цистита
Лечение лучевых повреждений мочевого пузыря требует комплексного подхода и включает следующие мероприятия.
Медикаментозная терапия
Назначаются обезболивающие и противовоспалительные препараты. Для предотвращения развития бактериальных осложнений применяются антибиотики. При длительных кровотечениях может развиться декомпенсация системы гемостаза (кровесвертывающей системы). Чтобы это предотвратить, назначают гемостатики – аминокапроновую кислоту, викасол и др. При развитии анемии применяют препараты железа.
Инстилляции
Инстилляция – это введение лекарственных препаратов непосредственно в полость органа, в нашем случае в мочевой пузырь. При лучевых циститах проводят инстилляции антисептиков, протеолитических и противовоспалительных препаратов, а также лекарственных средств, которые стимулируют регенерацию тканей.
Хирургическое лечение
Хирургическое лечение проводится при осложненных формах лучевых циститов. С помощью эндоскопической хирургии производят коагуляцию кровоточащих сосудов и телеангиоэктазий, также возможно удаление патологических сращений, инкрустраций и камней. Также хирургическое вмешательство требуется при образовании свищей.
Хронический лучевой цистит
Хронические лучевые циститы возникают не ранее, чем через 3 месяца после окончания лучевой терапии. Они сложнее поддаются лечению, склонны к упорным рецидивам и могут приводить к уменьшению емкости мочевого пузыря. Для борьбы с этой проблемой применяются лечебно-диагностическую процедуру под названием гидродистензия. Ее суть заключается в заполнении мочевого пузыря большим объемом жидкости под контролем давления. Это позволит увеличить
объем органа и устранить императивные позывы на мочеиспускание.
Профилактика
Самым действенным методом профилактики лучевого цистита является тщательное планирование полей облучения, таким образом, чтобы нецелевые ткани в них не попадали. Наилучшие результаты в этом плане показывает брахитерапия, которая позволяет подвести максимальную дозу непосредственно к опухоли.
Прогноз
Прогноз лучевого цистита зависит не только от тяжести симптомов, но и от сроков их развития. Наиболее благоприятно протекают острые лучевые реакции, которые развиваются в ближайшие 3 месяца после окончания радиолечения. При хронических постлучевых циститах могут развиться стойкие нарушения, требующие хирургического вмешательства.
Цены на лечение лучевых циститов определяются тяжестью патологии. При легких формах достаточно медикаментозной терапии и инстилляций. При тяжелых процессах может понадобиться эндоскопическое вмешательство и даже проведение хирургических операций.
У врачей Европейской клиники имеется большой опыт лечения рака мочевого пузыря, в том числе такого осложнения, как лучевой цистит. Это позволяет в каждом конкретном случае достигать максимально возможных результатов.
Источник
Специалисты из Института рака штата Сан-Паулу провели исследование, в котором оценили реальную частоту возникновения инфекции мочевых путей (ИМП) у пациентов с симптомами цистита, получающих лучевую терапию на область малого таза. Определенная в результате заболеваемость ИМП оказалась гораздо ниже той, о которой сообщалось ранее. Авторы заключили, что предыдущие подсчеты были неверными из-за того, что к группе ИМП ошибочно относили больных с асимптоматической бактериурией, у которых развивался вторичный цистит вследствие лучевой терапии. По их мнению, высокая частота ошибочных диагнозов ведет к чрезмерному применению эмпирической антибиотикотерапии в данной группе пациентов. Работа была опубликована в журнале Clinics (São Paulo, Brazil).
Лучевая терапия онкологических заболеваний органов малого таза часто сопровождается повреждением тканей мочевого пузыря. Воздействие радиации на эпителиальные клетки может вызывать острые функциональные нарушения, в том числе учащенные мочеиспускания, дизурию и гематурию, которые имитируют симптомы ИМП.
В общей популяции диагностика ИМП, как правило, основывается на наличии таких симптомов, как дизурия, полиурия, частые позывы к мочеиспусканию, надлобковая боль, лейкоцитурия и бактериурия (без вагинальных симптомов у женщин). Это служит достаточным основанием для назначения эмпирической антибиотикотерапии, которую применяют до получения результатов культурального исследования мочи.
Однако подобный подход, вероятно, не может быть применен к пациентам, проходящим лучевую терапию по поводу злокачественных образований малого таза. В данной популяции отмечается высокая частота развития вторичных циститов, связанных с самим раком или его лечением. У части пациентов с радиационным циститом в моче также обнаруживается высокий уровень лейкоцитов, что считается классическим маркером инфекционного цистита. Почти у половины пациентов с локализованным раком предстательной железы в процессе курса облучения развиваются симптомы со стороны мочевых путей. Тем не менее, истинная частота ИМП у таких больных остается неясной и в разных источниках варьирует от 6% до 45%.
В настоящее время нет доступных инструментов для клинического разграничения инфекционного и радиационного циститов. Это ставит под угрозу безопасность пациентов и приводит к чрезмерному назначению антибиотиков.
Задачей бразильских специалистов было оценить истинную распространенность инфекций мочевых путей среди пациентов с симптомами цистита, которым проводится лучевая терапия по поводу онкозаболеваний органов малого таза, и выявить возможные прогностические факторы ИМП.
В проспективное когортное исследование были отобраны пациенты, соответствующие следующим критериям: 1) с первичным раком органов малого таза, получающие лечение, направленное на борьбу с заболеванием, 2) старше 18 лет, 3) с хорошим статусом работоспособности. Из исследования были исключены пациенты, лечившиеся от ИМП, с катетеризацией мочевого пузыря, находящиеся на диализе, перенесшие цистостомию или нефростомию или принимавшие антибиотики в период лечения. До начала лучевой терапии проводились общий анализ и бактериологическое исследование мочи. Пациенты с положительными результатами посева также были исключены.
Во время проведения лучевой терапии симптомы со стороны мочевых путей оценивались еженедельно. В случае появления новых или ухудшения имеющихся симптомов проводились повторное исследование мочи и анкетирование пациентов. Диагноз ИМП подтверждался при выделении уропатогена в концентрации более 104 КОЕ/мл мочи.
Всего с сентября 2014 г. по ноябрь 2015 г. в исследование были отобраны 112 пациентов, из них 72 (64%) соответствовали критериям включения. В период наблюдения у 24 (33%) пациентов появились новые или усугубились ранее существовавшие симптомы со стороны мочевых путей. По результатам культурального исследования мочи диагноз ИМП был подтвержден только у одного пациента (1,4%). Частота встречаемости патологии оказалась гораздо ниже той, о которой сообщалось ранее.
Прогностические факторы ИМП в группе установлены не были (вследствие низкой распространенности).
Авторы заключили, что полученные результаты подчеркивают важность правильного подхода к диагностике ИМП у пациентов, получающих лучевую терапию на область малого таза. По их мнению, в данной популяции больным с симптомами цистита без нейтропении и лихорадки не следует назначать антибиотикотерапию до получения результатов бактериологического исследования.
Источник: V. F. Xavier et al. Clinics (Sao Paulo) 74, e1388. 2019. PMID: 31778433.
Источник
В статье проанализированы результаты лечения больных с поздними лучевыми повреждениями мочевого пузыря (осложненными и неосложненными циститами). Отмечается, что выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования. Так, при выраженном болевом синдроме и инкрустированной форме лучевого цистита наилучшие результаты отмечались на фоне внутрипузырного применения Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой предпочтение следует отдать инстилляциям УРО-ГИАЛА. Рексод продемонстрировал эффективность у больных с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Таблица 1. Сравнительная характеристика результатов лечения больных первой группы до и после внутрипузырного применения Димексида
Таблица 2. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных первой группы до и после внутрипузырного применения Димексида
Таблица 3. Сравнительная характеристика больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 4. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 5. Сравнительная характеристика больных третьей группы до и после внутрипузырного применения Рексода
Таблица 6. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных третьей группы до и после внутрипузырного применения Рексода
Введение
В настоящее время лучевая терапия является одним из основных методов лечения злокачественных новообразований органов малого таза. При отсутствии метастазов в регионарные лимфоузлы применение лучевой терапии позволяет добиться полной или частичной регрессии опухоли (рак тела и шейки матки, рак предстательной железы, в меньшей степени рак мочевого пузыря и прямой кишки) в среднем в 70-75% случаев. При этом продолжительность жизни после окончания курса лечебных мероприятий остается относительно высокой и составляет около четырех-пяти лет [1-3].
К сожалению, у части таких больных (10-15%) формируются лучевые повреждения органов малого таза: мочевого пузыря, прямой кишки и внутритазовой клетчатки [4, 5]. Оценивая данные литературы, можно констатировать неудовлетворительные результаты диагностики и лечения лучевых повреждений органов малого таза. Это выражается в частых рецидивах цистита с исходом в сморщивание мочевого пузыря, внутритазовом лучевом фиброзе со сдавлением интрамурального и юкставезикального отделов мочеточников и развитии хронической почечной недостаточности [7-8].
Проведение лучевой терапии может осложниться развитием радиационно-индуцированного фиброза, выраженность которого прямо пропорциональна величине суммарной поглощенной дозы, режиму фракционирования и времени после проведения лучевой терапии. Микроскопическое исследование тканей с радиационно-индуцированным фиброзом показало, что его формирование сопровождается развитием каркаса в подслизистом слое стенки мочевого пузыря, в сетях которого фиксируются стенки мелких артерий и вен. Происходит лучевое повреждение и самой сосудистой стенки, особенно ее адвентиции, что приводит к потере сосудами эластичности и появлению ломкости. Клинически это обнаруживается различной степенью гематурии, вплоть до профузного кровотечения. Развитие в последующем лучевого фиброза всей стенки мочевого пузыря значительно отягощает клинические симптомы и выраженность лучевого цистита [9-11].
В диагностике лучевых циститов важное значение имеют общеклинические, рентгенологические и инструментальные методы исследования. Ведущим методом исследования мочевого пузыря остается цистоскопия, позволяющая достоверно установить локализацию и степень выраженности лучевого повреждения, то есть выявить органические изменения слизистой оболочки, наличие камней и видимых опухолевых элементов, оценить состояние устьев мочеточников.
Материал и методы
В настоящей работе проведено исследование эффективности новых методов местного лечения осложненных и неосложненных лучевых циститов. 139 больных были разделены на три группы. Первую группу составили 49 пациентов (17 с неосложненными циститами и 32 – с осложненными). Они получали традиционное местное лечение: Димексид, Колларгол, синтезоновая эмульсия и облепиховое масло. Во вторую группу вошли 52 больных (26 с неосложненными циститами и 26 – с осложненными), у которых для местного лечения использовался препарат УРО-ГИАЛ. В местной терапии третьей группы – 38 пациентов (13 с неосложненными циститами и 25 – с осложненными) – применялась супероксиддисмутаза (препарат Рексод). Кроме того, всем пациентам была назначена антибактериальная, антикоагулянтная, вазоактивная, симптоматическая и иммунная терапия.
Местное лечение больных первой группы начиналось с инстилляций 10%-ного Димексида в объеме 20 мл. Применение этого препарата патогенетически обосновано, поскольку он обладает выраженным противовоспалительным, противоотечным и обезболивающим эффектом. В связи с тем что Димексид является органическим растворителем и легко проникает в ткани, в раствор добавлялись антибиотики (гентамицин, амикацин), фибролизирующие (Лидаза) и противовоспалительные препараты (преднизолон). Инстилляции проводились ежедневно по 20 мл (от 10 до 15 процедур). У больных с микрогематурией или неинтенсивной примесью крови в моче для инстилляций мочевого пузыря дополнительно применялся 3%-ный Колларгол 20 мл на одно введение. При неэффективности монотерапии Колларголом для усиления гемостатического эффекта его чередовали с охлажденной аминокапроновой кислотой. После стихания воспалительных процессов внутрипузырно в подогретом виде один раз в сутки в течение 10-15 дней вводились синтезоновая эмульсия и облепиховое масло. Действие этих препаратов направлено на усиление репараторных процессов в стенке мочевого пузыря. Благодаря жировой основе они оказывают выраженное обволакивающее и обезболивающее действие.
Местное лечение больных второй группы подразумевало применение препарата на основе гиалуроновой кислоты УРО-ГИАЛ. УРО-ГИАЛ – вязкоэластичный протектор межклеточного вещества уротелия мочевого пузыря и уретры. УРО-ГИАЛ позволяет создать вязкоэластичную пленку на слизистой, тем самым защищая ее от агрессивного воздействия мочи и препятствуя адгезии микробов к поврежденной поверхности. Инстилляции УРО-ГИАЛА проводились через день в течение 12-15 дней, затем в режиме одно введение в неделю.
В третьей группе пациентам назначался препарат супероксиддисмутазы Рексод. Рексод прямо инактивирует свободные радикалы, блокирует реакцию перекисных радикалов с арахидоновой кислотой, ослабляет активное действие лейкотриена В4, ингибирует хемотаксис лейкоцитов, значительно уменьшает синтез коллагена фибробластами (способствует регрессии радиационно-индуцированного фиброза). Рексод вводился внутрь мочевого пузыря, при этом содержимое флакона растворяли непосредственно перед введением в 10 мл стерильного физиологического раствора. Инстилляции проводились один раз в сутки на протяжении 15-20 дней.
Результаты и обсуждение
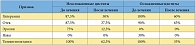
Результаты лечения больных первой группы представлены в таблице 1. Приведенные данные свидетельствуют о значительном уменьшении частоты ночного мочеиспускания и снижении бактериурии у большинства больных как с осложненными, так и с неосложненными циститами. Несмотря на по-прежнему высокий уровень лейкоцитурии, она носила менее выраженный характер. Макрогематурия после лечения не выявлялась у пациентов с неосложненными циститами, но сохранялась у 18% пациентов с осложненными циститами.
Сравнительный анализ УЗИ-признаков лучевых циститов у больных первой группы продемонстрировал, что внутрипузырное применение Димексида позволило очистить мочевой пузырь от солевой инкрустации более чем в 50% случаев. К сожалению, основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) были купированы у незначительного числа пациентов.
Динамика выраженности цистоскопических признаков лучевых циститов у больных первой группы до и после лечения продемонстрирована в таблице 2. У пациентов как с неосложненными, так и осложненными циститами сохранялись воспаление (гиперемия и отек) и телеангиоэктазии. Таким образом, внутрипузырное применение Димексида было наиболее эффективным у пациентов с выраженным болевым синдромом и инкрустированной формой лучевого цистита.
Результаты лечения больных второй группы представлены в таблице 3. Следует отметить выраженное противовоспалительное действие УРО-ГИАЛА. Так, частота ночного мочеиспускания сократилась в два раза более чем у 56% пациентов с неосложненными циститами и у 59% с осложненными циститами. Лейкоцитурия уменьшилась в два раза у больных с осложненными циститами и практически не выявлялась у пациентов с неосложненными циститами (12%), а бактериурия сохранилась только у 27 и 25% больных в обеих подгруппах соответственно.
Основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) исчезли у подавляющего числа больных. Однако УРО-ГИАЛ практически не оказал действия на инкрустированные циститы, особенно у больных со сниженным объемом мочевого пузыря.
Характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после лечения продемонстрирована в таблице 4. Гиперемия и отек беспокоили менее чем 25% больных как с неосложненной, так и осложненной формой цистита. Частота эрозии у пациентов с неосложненными циститами уменьшилась в четыре раза. Однако более чем у 70% пациентов сохранились телеангиоэктазии. Язва мочевого пузыря у больных с осложненными циститами уменьшилась в размерах и очистилась от фибрина.
Можно сделать вывод, что применяемая схема лечения – инстилляции УРО-ГИАЛА – наиболее эффективна у пациентов с выраженным воспалительным процессом и болевым синдромом, связанным с воспалением стенок мочевого пузыря, и может применяться у больных с любой формой лучевого цистита, осложненного бактериальной инфекцией.
Результаты лечения больных третьей группы представлены в таблице 5. Почти у половины больных с неосложненными и осложненными циститами в два раза уменьшилась частота ночного мочеиспускания. У 75 и 90% пациентов соответственно сохранилась лейкоцитурия. Однако бактериурия почти у половины больных в обеих подгруппах не определялась, а макрогематурия исчезла у всех пациентов.
Сравнительная характеристика УЗИ-признаков лучевых циститов у больных третьей группы продемонстрировала достоверное увеличение объема мочевого пузыря у пациентов с микроцистисом, однако в меньшей степени Рексод оказал положительное действие на инкрустацию стенок мочевого пузыря и наличие взвеси в его просвете.
Что касается выраженности цистоскопических признаков лучевых циститов у больных третьей группы (табл. 6), то в результате лечения язва мочевого пузыря исчезла у всех больных, однако более чем у 60% пациентов с осложненными циститами сохранялись признаки воспаления (гиперемия и отек). Таким образом, Рексод можно рекомендовать больным с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Заключение
Следует отметить, что используемые препараты (Димексид, УРО-ГИАЛ и Рексод) имеют разную направленность действия. В частности, при выраженном фиброзе стенки мочевого пузыря предпочтение следует отдавать применению инстилляций раствора Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой наиболее эффективным оказалось применение УРО-ГИАЛА. У больных с гематурией и глубокими нарушениями целостности слизистой мочевого пузыря (язвенно-некротический цистит) наиболее высокие результаты продемонстрировало применение супероксиддисмутазы. Выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования.
Источник
