Брахитерапия и цистит лечение
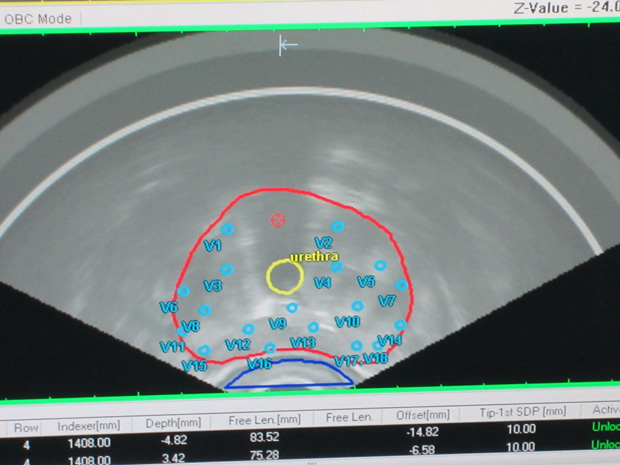
Брахитерапия относится к наиболее востребованным методам лечения рака предстательной железы. В первую очередь интерес к этому методу продиктован небольшим количеством возможных осложнений, возможностью сохранения потенции, низким риском недержания мочи, которая отмечается у каждого пятого больного, прошедшего хирургическое лечение.
Тем не менее, и брахитерапия, в некоторых случаях, может привести к развитию побочных эффектов:
- Затруднение мочеиспускания.
Самым частым осложнением после брахитерапии рака предстательной железы является затруднение мочеиспускания, которое отмечается у 1%-5% больных. Как правило, задержка мочеиспускания (обструктивные нарушения) после брахитерапии возникает у больных с аденомой предстательной железы, которая вызывает заметные нарушения мочеиспускания еще до начала лучевого лечения. Поэтому, все больные раком предстательной железы пред проведением брахитерапии проходят тщательное обследование (урофлоуметрия, определение объема остаточной мочи, заполнение специальных опросников).Это позволяет выделить ту группу больных, которым проведение лучевого лечения рака предстательной железы не желательно из-за повышенного риска осложнений. Остальным пациентам лечение может быть выполнено без значительного риска возникновения побочных эффектов. - Нарушения со стороны прямой кишки.
Вторым, наиболее частым осложнением после брахитерапии рака предстательной железы являются нарушения со стороны прямой кишки, которые проявляются в виде болевых ощущений, явлений постлучевого воспаления, кровянистых выделений из прямой кишки. Наиболее часто эти побочные эффекты наблюдаются после проведения дистанционной лучевой терапии (по данным некоторых авторов, их частота достигает 10%-15%). Несколько реже, подобные осложнения возникают после, так называемой, низкодозной (классической) брахитерапии
Как избежать осложнений после брахитерапии рака предстательной железы?
Самым действенным способом борьбы с указанными последствиями лечения является тщательное планирование терапии и точное подведение запланированной дозы.
Наиболее эффективно указанные задачи помогает решать самый современный вариант брахитерапии – высокодозная брахитерапия. За счет точного подведения запланированной дозы на предстательную железу и небольшой лучевой нагрузки на окружающие нормальные ткани высокодозная брахитерапия позволяет снизить риск осложнений со стороны прямой кишки до минимума (0%-2%).

Кроме того, при таком лечении обеспечиваются наиболее благоприятные условия для сохранения у пациентов потенции и снижается риск возникновения недержания мочи с 15%-20% (хирургическое лечение) до 0%-1%. Эти особенности высокодозной брахитерапии позволяют достигать выздоровления больных раком предстательной железы при сохранении нормальной жизненной активности и минимальном риске возникновения тяжелых побочных эффектов лечения.
Например, по данным специалистов НИИ онкологии им. Н.Н. Петрова, которые провели более 500 сеансов высокодозной брахитерапии, риск возникновения серьезных нарушений мочеиспускания составил 1.1% (в основном, эти осложнения отмечались у больных, прошедших трансуретральную резекцию аденомы предстательной железы), осложнений со стороны прямой кишки — менее 1%, случаев недержания мочи зарегистрировано не было.
Что нельзя делать после возникновения осложнений брахитерапии рака предстательной железы?
Нередко, пациенты, прошедшие лучевое лечение рака предстательной железы, в том числе, брахитерапию, при возникновении осложнений попадают на лечение в поликлинику или стационары общей лечебной сети. В этом случае, больным нередко предлагают хирургические методы лечения:
- трансуретральную резекцию при нарушениях мочеиспускания,
- биопсию стенки прямой кишки — при осложнениях со стороны прямой кишки.
Следует помнить, что любые инвазивные (хирургические) манипуляции на уретре, мочевом пузыре, прямой кишке после проведения брахитерапии крайне нежелательны. Они могут выполняться только после предварительной консультации с Вашим лечащим врачом-радиотерапевтом.
Какие лечебные мероприятия могут помочь при возникновении побочных эффектов брахитерапии?
В большинстве случаев осложнения брахитерапии имеют временный преходящий характер. Они возникают в течение первых нескольких недель и стихают в течение последующих нескольких месяцев. При длительном сохранении нежелательных последствий, как правило, используются лекарственные методы лечения. Например, при затруднении мочеиспускания назначаются препараты из группы альфа-блокаторов, при наличии болей в области прямой кишки — активно используются противовоспалительные препараты, свечи, мази и т.д.
Самым важным правилом, которое должны помнить все пациенты, прошедшие лечение рака предстательной железы, заключается в том, что при возникновении тех или иных побочных эффектов брахитерапии, в первую очередь, необходимо обратиться к своему лечащему врачу-радиотерапевту.
Источник
Брахитерапия является разновидностью лучевой терапии, основной особенностью которой является непосредственный контакт источника ионизирующего излучения с опухолевой тканью. Брахитерапия может быть как самостоятельным методом лучевой терапии, так и применяться, как часть сочетанного лучевого лечения после проведения дистанционного этапа.
Впервые брахитерапия была проведена в 1901 году доктором по фамилии Данло, который прикладывал к поверхности опухоли соли радия, содержащиеся в запаянных стеклянных трубочках, а уже в 1903 году Аббе начал проводить внутритканевую терапию путём внедрения трубочек с радием непосредственно в ткань опухоли. Несомненно, за прошедшее столетие методика проведения брахитерапии неоднократно совершенствовалась, но принцип остался исходным — максимально близкий контакт источника с опухолевой тканью для максимального её облучения и щажения окружающих здоровых тканей.
Виды брахитерапии
Выделяют низкомощностную брахитерапию, при которой выполняется имплантация микроисточников низкой мощности дозы (изотопы I-125, Pd-103, Cs-131) на постоянной основе, и высокомощностную брахитерапию, при которой облучение обеспечивается временным контактом с источниками высокой мощности дозы (изотопы Ir-192, Co-60, Cs-137), брахитерапию. Кроме того, существует так называемая pulse-dose rate, или импульсная, брахитерапия, при которой облучение идёт короткими импульсами со значительными, до часа, перерывами. Низкомощностная брахитерапия обычно применяется при планируемой дозе 2 Гр в час и менее, высокомощностная — при дозе 12 Гр в час и более. В зависимости от степени автоматизации процесса введения радиоактивных изотопов выделяют методику manual loading, при которой установка производится вручную, и remote afterloading, при которой установка производится автоматически согласно разработанному плану лечения.
Выделяют несколько видов брахитерапии в зависимости от локализации опухолевого процесса:
- Внутриполостная. Применяется для лечения злокачественных новообразований полых органов — влагалища, шейки и тела матки, анального канала, пищевода. Источники ионизирующего излучения крепятся в специальном эндостате, который и устанавливается в просвете поражённого опухолью органа.
- Интерстициальная. Другое название — внутритканевая, название котороей отражает суть метода: радиоактивный источник в виде микрокапсул («зёрен») или игл погружается непосредственно в опухолевую ткань. Преимущественно применяется при лечении рака предстательной железы.
- Внутрисосудистая. Является эффективным методом лечения повторного сужения просвета коронарных сосудов после стентирования. Сразу после выполнения баллонной ангиопластики по тому же катетеру к атересклеротической бляшке подводятся зерна, содержащие радиоактивные изотопы, на 15-20 минут.
- Поверхностная. Другое название — аппликационная; применяется при наружных локализациях опухоли, в первую очередь при раке кожи. Аппликаторы для данного метода брахитерапии должны обладать достаточной пластичностью для тесного контакта с опухолью на всём её протяжении. Применяется обычно изотоп Ir-192.
- Офтальмологическая. Проводится с помощью специальных аппликаторов с радиоизотопами Ru-106 и Sr-90 с целью лечения опухолевых поражений в области глаза — сосудистой оболочки (меланома, метастаз рака молочной железы), сетчатки (ретинобластома). Аппликатор устанавливается в условиях операционной под комбинированным наркозом (внутривенным и местным обезболиванием) — напрямую подшивается к поверхности глазного яблока в проекции опухоли. В течение нескольких дней, пока проходит лечение, пациент находится в стационаре. После достижения требуемой суммарной дозы лучевого воздействия на опухоль аппликатор снимают, также оперативным путём.
- Интраоперационная. Проводится, как ясно из названия, в ходе оперативного вмешательства на ложе удалённой опухоли. Применяется при раке молочной железы и может стать альтернативой послеоперационной дистанционной лучевой терапии, что особенно важно при лечении рецидивной опухоли, когда ранее уже проводилась дистанционная лучевая терапия, а также при саркомах мягких тканей — в случаях, когда функционально невозможно достичь «чистых» краёв резекции.
Заболевания, при которых проводится брахитерапия
В отдельных клинических ситуациях брахитерапию рассматривают как адекватную альтернативу дистанционной лучевой терапии, в других же — как обязательный компонент комплексного лечения.
Основными злокачественными опухолями, по поводу которых проводится брахитерапия, являются:
- Рак предстательной железы. Основными критериями, по которым отбираются больные, которым возможно провести брахитерапию, являются следующие: клиническая стадия Т1—Т2аN0M0, общее значение баллов по шкале Глисона ≤6 (3+3) либо 7 (3+4), ПСА ≤10 нг/мл, объем предстательной железы ≤50 cм 3 — то есть пациенты, относящиеся к благоприятной прогностической группе. Следует отметить, что в рекомендациях Американской ассоциации брахитерапии показания для проведения интерстициальной брахитерапии значительно шире и предполагают возможность проведения такого лечения и пациентам с Т2с-Т3 стадиями, суммой баллов по шкале Глисона до 10 и уровнем ПСА до 50 нг/мл. Однако для больных с неблагоприятным и промежуточным прогнозом брахитерапия рекомендуется как часть комбинированного лечения — в сочетании с дистанционной лучевой терапией иили гормонотерапией.
- Рак шейки матки. Брахитерапия проводится всем пациенткам, которым не планируется проведение хирургического лечения, а также как послеоперационное лечение в случае значительного риска рецидива во влагалище или параметрии после завершения дистанционного этапа.
- Рак тела матки. Возможно проведение брахитерапии как в послеоперационном, так и в послеоперационном варианте. Так, при II стадии заболевания достаточно проведения одной только брахитерапии при низком риске рецидива и при адекватном объёме удаленных лимфоузлов, а при высоких группах риска и в отсутствие лимфодиссекции брахитерапия дополняется дистанционным облучением.
- Базальноклеточный рак кожи. Так как данная опухоль часто располагается в области лица, проведение хирургического лечения может привести к появлению значимого косметического дефекта. С другой стороны, базалиома может быть излечена только лучевым методом, поэтому проведение аппликационной брахитерапии может быть методом выбора у достаточно широкого круга пациентов.
- Опухоли головы и шеи. В настоящее время брахитерапия не является стандартной опцией для лечения опухолей данной локализации, но эта возможность активно исследуется для опухолей наружной локализации (например, в полости рта) на ранних стадиях.
- Рак пищевода. Брахитерапия может быть проведена в рамках комплексного лечения местнораспространённой опухоли как дополнительный по отношению к дистанционной лучевой терапии метод.
- Саркомы мягких тканей. Проведение брахитерапии позволит локально — на собственно опухолевый узел или на край операционной раны, в котором выявлены опухолевые клетки, — подвести большую дозу и тем самым не только улучшить результаты лечения, но и избежать как возможной калечащей операции, так и серьёзных осложнений (атрофия мышц, контрактура суставов). Особое значение брахитерапия сарком имеет у пациентов детского возраста, так как позволяет снизить дозную нагрузку на зоны роста.
Подготовка к брахитерапии
Как и перед любым другим этапом противоопухолевого лечения, требуется тщательная диагностика для оценки текущего состояния пациента и степени прогрессирования его заболевания. Планирование брахитерапии происходит в специализированной компьютерной программе, аналогичной таковой для планирования дистанционной лучевой терапии. Оконтуривание объёмов, которые необходимо подвергнуть лучевому воздействию, и здоровые структуры определяются на основании данных топометрической компьютерной томографии; более современной методикой является планирование на основании данных магнитно-резонансной томографии. Возможно совмещение изображений, полученных во время КТ, МРТ и ПЭТ, для большей точности определения облучаемых объёмов. Следует отметить, что внедрение эндостатов осуществляется до топометрической предлучевой подготовки. В случае проведения внутритканевой брахитерапии зерна или иглы, несущие изотоп, имплантируются после расчёта плана облучения. Установка как эндостатов, как и зёрен и игл, проводится под местной анестезией; при лечении рака предстательной железы выполняется эпидуральная анестезия.
В случае проведения низкомощностной внутриполостной брахитерапии пациент остаётся в изолированном помещении до удаления источника из его тела (как правило, от 12 до 24 часов), поэтому для проведения такого вида лечения требуется госпитализация. Напротив, при проведении высокомощностной брахитерапии процедура длится значительно более короткий период времени (около получаса), и поэтому может быть проведена амбулаторно.
Разовая и суммарная дозы излучения, равно и количество фракций, назначаются индивидуально в зависимости от локализации опухолевого процесса, стадии заболевания и проведённого ранее лечения. Так, для базальноклеточного рака кожи требуемая суммарная доза составляет 24-36 Гр, разовая доза составляет 3-5 Гр; при раке тела матки разовые дозы составляют 7 Гр по 3 фракции или 6 Гр по 5 фракций при радикальном курсе, 5 Гр по 4 фракции при послеоперационном курсе в сочетании с дистанционной лучевой терапией.
Побочные эффекты
Несмотря на то, что брахитерапия значительно минимизирует дозную нагрузку на прилежащие здоровые ткани, полностью исключить её невозможно. Побочные эффекты при брахитерапии аналогичны таковым при дистанционной лучевой терапии и зависят от локализации опухолевого процесса. Так, при лечении по поводу рака кожи возможно появление эритемы, при лечении органов малого таза — реакции со стороны мочевого пузыря и кишечника. Для их купирования врачом назначается соответствующая сопроводительная терапия.
Помимо рекомендаций по предупреждению и лечению реакций, связанных непосредственно с проведением брахитерапии, существует и ряд общих рекомендаций после выполнения внутритканевой брахитерапии:
- Ограничение физических нагрузок,
- Соблюдение диеты, исключающей острую, жареную и жирную пищу,
- Не сажать на колени маленьких детей первые два месяца после операции и не находиться вблизи беременных женщин. Это связано с тем, что во время полураспада введённых изотопов существует риск лучевого воздействия, хоть и незначительного, на окружающих.
- В случае назначения лечения по поводу другого заболевания, особенно физиотерапевтических процедур, необходима предварительная консультация онколога до начала их выполнения.
Наконец, важно помнить о динамическом наблюдении. Дата визита к онкологу назначается, исходя из локализации опухолевого процесса, по поводу которого проводилось лечение. Так, в случае офтальмологической патологии контрольный визит назначается обычно спустя 3-4 месяца после завершения брахитерапии, при раке предстательной железы — спустя 2-3 месяца.
Список литературы:
- Рак шейки матки. Клинические рекомендации Ассоциации Онкологов России. 2020.
- Рак тела матки и саркомы матки. Клинические рекомендации Ассоциации Онкологов России. 2020.
- Рак предстательной железы. Клинические рекомендации Ассоциации Онкологов России. 2020.
- Каприн А.Д. и соавт. Внутритканевая лучевая терапия (брахитерапия) рака предстательной железы. Собственный опыт работы Национального медицинского исследовательского радиологического центра Минздрава России. Русский медицинский журнал. 2017, № 27. С.2011-2014.
- Винокурова А.С. и соавт. Аппликационная брахитерапия в лечении местнораспространённого базальноклеточного рака кожи. Академический журнал Западной Сибири. 2017. Том 13, № 3 (70), с. 31-33.
- Белоусов А.В., Лыкова Е.Н. Введение в брахитерапию. Москва, 2019.
- Жуманкулов А.М. и соавт. Брахитерапия злокачественных опухолей полости рта и ротоглотки. Опухоли головы и шеи. 2015. № 4, том 5. С. 41-46.
- Литвинов Р.П. и соавт. Брахитерапия местнораспространённого рака пищевода как компонент радикального лечения: преимущества и риски. Злокачественные опухоли. 2016. № 4.
Источник
Одним из важнейших свойств брахитерапии является то, что такой метод лечения в меньшей степени нарушает сексуальную функцию, чем хирургическое вмешательство. По сравнению с радикальной простатэктомией и дистанционной лучевой терапией, у брахитерапии меньше побочных эффектов, но они, тем не менее, могут возникнуть.
Последствия после брахитерапии
В ближайший послеоперационный период возможны:
- учащенное мочеиспускание
- примесь крови в моче и сперме
- болезненные ощущения во время эякуляции.
Послеоперационные рекомендации
- Непосредственно после проведения сеанса брахитерапии пациент помещается в палату. Вставать и ходить нельзя до следующего утра.
- В случае примеси крови в моче рекомендуется обильное питье.
- Как правило, на следующий день или через день после процедуры пациент самостоятельно покидает клинику.
- Если до начала лечения он имел существенные нарушения мочеиспускания, ему назначаются препараты группы Альфа1-адреноблокаторов (Омник, Дальфаз и др.), продолжительность приема которых подбирается индивидуально.
После брахитерапии нельзя:
1. Поднимать тяжести более 10 кг
В течение недели после процедуры пациенту не рекомендуется подвергать себя большим физическим нагрузкам, поднимать вес, превышающий 10кг. Но эти ограничения накладываются не на долгий срок, уже спустя месяц после лечения можно окончательно вернуться к дооперационному уровню физической активности.
2. Употреблять алкоголь, есть острую и чрезмерно соленую пищу
В течение месяца после брахитерапии следует воздерживаться от употребления алкоголя, острой или чрезмерно соленой пищи.
3. Употреблять БАДы
В некоторых случаях мы рекомендуем ограничить прием биологически активных добавок стимулирующих восстановление тканей, поскольку это может увеличить вероятность рецидива заболевания.
4. Загорать и долго находится на солнце
Ультрафиолет является доказанным канцерогеном, поэтому в дальнейшем нужно избегать длительного пребывания на открытом солнце. Загорание необходимо исключить совсем.
5. Физически воздействовать на область малого таза
Следует избегать физических воздействий на область малого таза: любые физиотерапевтические процедуры на эту область – противопоказаны. Посещение парилки в бане так же следует исключить.
К физическим воздействиям на область предстательной железы так же можно отнести езду на велосипеде и занятия на велотренажере, однако однозначного ответа на вопрос можно ли заниматься на велотренажере или кататься на велосипеде после брахитерапии — нет, ввиду отсутствия достоверных данных по этой теме.
В течение полугода после окончания сеанса брахитерапии не рекомендуется проведение оперативных манипуляций в области малого таза. В том случае, когда имеется необходимость хирургического лечения хронических заболеваний этой области (таких как геморрой, полипы прямой и сигмовидной кишки, мочевого пузыря и др.) следует сделать это до начала лучевого лечения.
Жизнь после брахитерапии
После проведения высокодозной брахитерапии предстательной железы, пациент не является источником ионизирующего излучения, кроме того в теле пациента не остается инородных тел. Поэтому нет необходимости ограничивать свое общение с близкими, и не возникает сложностей при проходе контроля в аэропортах.
После окончания лечения пациент также получает подробные рекомендации относительно дальнейшего лечения и плана обследования, а также диеты, сексуальной жизни, которые даются исходя из индивидуальных особенностей его организма и с учетом сопутствующих заболеваний.
Источник
