Автономная нейропатия мочевого пузыря

Продолжая разговор об автономной нейропатии, расскажем вам о нарушении работы мочеполовой системы при некомпенсированном сахарном диабете – диабетической урогенитальной нейропатии.
При длительно повышенном уровне глюкозы крови могут повреждаться нервы, контролирующие работу мочевого пузыря и мочеточников (по ним моча поступает из почек в мочевой пузырь). Развивается так называемый нейрогенный мочевой пузырь – понятие, объединяющее в себя разные симптомы, которые могут встречаться при многих заболеваниях. При этом сахарный диабет – не самая частая причина.
Если развивается данное осложнение сахарного диабета, то с уверенностью можно сказать, что есть у человека есть и другие формы автономной нейропатии, поэтому важно пройти комплексное обследование.
Симптомы могут быть различными и их можно разделить на два типа:
- По гипотоническому типу – гипоактивный мочевой пузырь – то есть снижается тонус мышц мочевого пузыря и мочеточников
- По гипертоническому типу – гиперактивный мочевой пузырь – тонус повышен, возникает спазм мускулатуры мочевыделительной системы
Симптомы:
При гипоактивном мочевом пузыре возникает отсутствие нормального мочеиспускания даже при наличии в организме большого количества мочи (более 1500 мл). Что при этом происходит?
- Перезаполнение мочевого пузыря и неспособность чувствовать, когда мочевой пузырь полон – не возникает желания сходить в туалет
- Неполное опорожнение пузыря (чувство наполненности)
- Регулярно вялая струя мочи
- Боль при мочеиспускании
- Недержание мочи (из-за слабости мышцы, закрывающей выход из мочевого пузыря)
Задержка мочи увеличивает риск развития инфекции мочевыводящих путей.
При гиперактивном мочевом пузыре появляется чрезмерная активность мышц мочевыделительной системы. Мочеиспускание может возникнуть в любой период времени и зачастую в неудобном месте, поскольку нейрогенная дисфункция мочевого пузыря делает невозможным произвольно контролировать акт мочеиспускания. Что может при этом беспокоить?
- Частые позывы при небольшом количестве мочи
- Недержание (мгновенное истечение при сильном внезапном позыве)
- Перенапряжение мышц тазового дна и даже обратное попадание мочи из мочевого пузыря в почки
- Учащенные ночные мочеиспускания
- Боль в мочеиспускательном канале (странгурия)
Влияние некомпенсированного сахарного диабета на половые органы.
По данным статистики до 75% мужчин с сахарным диабетом могут испытывать различные сексуальные проблемы, выраженные в той или иной степени. Конечно, речь не идет о случаях хорошо компенсированного диабета.
Высокий уровень глюкозы крови также приводит к повреждению сосудов и нерва, регулирующего работу половых органов. Все это может приводить к нарушению эрекции, эякуляции. Но также это может быть и симптомом других заболеваний, поэтому важно пройти обследование, сдать анализ крови на пролактин, тиреотропный гормон (ТТГ), общий тестостерон, эстрадиол и другие гормоны.
Стресс, курение, избыточный вес также играют немаловажную роль!
Влияет ли сахарный диабет на женщин?
При некомпенсированном сахарном диабете часто возникают различные инфекции половых органов (кандидоз или молочница, бактериальный вагинит, цистит и пр.), которые в свою очередь могут вызывать разные неприятные симптомы – дискомфорт, зуд, боль при половом акте. Конечно, стресс, психологическое «выгорание» от диабета тоже значимо влияют на либидо. В таким случае может помощь работа с психологом.
Можно ли вылечить такое осложнение сахарного диабета?
Конечно, можно, и в основе лечения лежат:
- Длительная компенсация сахарного диабета
- Постепенное достижение целевого гликированного гемоглобина (обговорите с врачом необходимые его значения)
- Важно не просто достичь хорошего гликированного, но и стараться не допускать «скачков» сахара от низких к высоким и наоборот
- Откажитесь от курения!
- При развитии инфекции мочевыводящих путей применяются антибактериальные препараты
- В тяжелых случаях гипоактивного мочевого пузыря врач назначает препараты, усиливающие тонус мочевыводящих путей или проводится катетеризация мочевого пузыря.
Источник
Нейрогенный мочевой пузырь – это дисфункция мочевого пузыря, обусловленная врожденной или приобретенной патологией нервной системы. В зависимости от состояния детрузора дифференцируют гипер- и гипорефлекторный тип патологии. Заболевание может проявляться поллакиурией, недержанием мочи или ее патологической задержкой. Диагностика синдрома заключается в полном невролого-урологическом обследовании (анализы, урография, УЗИ почек и мочевого пузыря, урофлоурометрия, цистография и цистоскопия, сфинктерометрия, рентгенография и МРТ позвоночника, МРТ головного мозга и пр.). Лечение может включать немедикаментозную и лекарственную терапию, катетеризацию мочевого пузыря, оперативное вмешательство.
Общие сведения
Нейрогенный мочевой пузырь – достаточно распространенное состояние в клинической урологии, связанное с невозможностью осуществления произвольно-рефлекторного накопления и выделения мочи из-за органического и функционального поражения нервных центров и путей, регулирующих данный процесс. Расстройства мочеиспускания имеют социальный аспект, поскольку могут ограничивать физическую и психическую активность человека, создавать проблему его социальной адаптации в обществе.
Патология часто сопровождается миофасциальным синдромом, синдромом тазовой венозной конгестии (венозного застоя). Более чем в 30% случаев наблюдается развитие вторичных воспалительно-дистрофических изменений со стороны мочевыделительной системы: пузырно-мочеточникового рефлюкса, хронического цистита, пиелонефрита и уретерогидронефроза, приводящих к артериальной гипертензии, нефросклерозу и хронической почечной недостаточности, что может грозить ранней инвалидизацией.
Нейрогенный мочевой пузырь
Причины
Сбой, происходящий на любом этапе сложной многоуровневой регуляции процесса мочеиспускания, может привести к развитию одного из многочисленных клинических вариантов нейрогенного мочевого пузыря. У взрослых синдром связан с повреждением головного и спинного мозга (при инсульте, сдавлении, хирургическом вмешательстве, переломе позвоночника), а также с воспалительно-дегенеративными и опухолевыми заболеваниями нервной системы – энцефалитом, рассеянным энцефаломиелитом, полинейропатией, полирадикулоневритом, туберкуломой, холестеатомой и т. д.
Нейрогенный мочевой пузырь у детей может иметь место при врожденных дефектах развития ЦНС, позвоночника и мочевыделительных органов, после перенесенной родовой травмы. Недержание мочи может быть вызвано снижением растяжимости и емкости мочевого пузыря вследствие цистита или неврологических заболеваний.
Классификация
Выделяют гиперрефлекторный нейрогенный мочевой пузырь, проявляющийся в фазу накопления гиперактивностью детрузора (при надсегментарных поражениях нервной системы) и гипорефлекторный – со сниженной активностью детрузора в фазу выделения (при поражении сегментарно-периферического аппарата регуляции мочеиспускания). Синдром может иметь в основе рассинхронизацию деятельности детрузора и сфинктера мочевого пузыря (внутренняя и наружная детрузорно-сфинктерная диссинергия).
Симптомы
Синдром нейрогенного мочевого пузыря может иметь постоянные, периодические или эпизодические проявления, а многообразие его клинических вариантов определяется различием уровня, характера, степени тяжести и стадии поражения нервной системы. Типичными для гиперактивного варианта патологии являются поллакиурия, в т. ч. никтурия, императивные позывы и недержание мочи. Преобладание тонуса детрузора ведет к значительному повышению внутрипузырного давления при малом количестве мочи, что при слабости сфинктеров вызывает императивные позывы и учащенное мочеиспускание.
Гиперактивный тип синдрома характеризуется спастическим состоянием и опорожнением при накоплении менее 250 мл мочи; отсутствием или малым объемом остаточной мочи, затруднением произвольного начала и самого акта мочеиспускания; появлением вегетативных симптомов (потливости, подъема артериального давления, усиления спастики) перед микцией в отсутствии позывов; возможностью спровоцировать мочеиспускание раздражением области бедра и над лобком. При наличии ряда неврологических нарушений может возникать неконтролируемое стремительное выделение большого объема мочи – «церебральный незаторможенный мочевой пузырь».
Относительное преобладание тонуса сфинктеров при детрузорно-сфинктерной диссинергии выражается полной задержкой мочи, мочеиспусканием при натуживании, наличием остаточной мочи. Гипоактивный нейрогенный мочевой пузырь проявляется снижением или отсутствием сократительной активности и опорожнения при полном и даже переполненном пузыре в фазу выделения.
Из-за гипотонии детрузора нет повышения внутрипузырного давления, необходимого для преодоления сопротивления сфинктера, что ведет к полной задержке или вялому мочеиспусканию, натуживанию во время микции, наличию большого (до 400 мл) объема остаточной мочи и сохранению ощущения наполненности пузыря. При гипотоничном растянутом мочевом пузыре возможно недержание мочи (парадоксальная ишурия), когда при переполнении органа происходит механическое растяжение внутреннего сфинктера и неконтролируемое выделение мочи каплями или небольшими порциями наружу.
Осложнения
Денервация вызывает развитие выраженных трофических нарушений и осложнений в виде интерстициального цистита, приводящего к склерозированию и сморщиванию мочевого пузыря. В мочевыводящих путях могут формироваться камни, нарушающие отток мочи, провоцирующие развитие инфекции. В случае спазма сфинктера может возникать пузырно-мочеточниковый рефлюкс (обратный заброс мочи в мочеточники и почки, приводящий к воспалению). Синдром часто сопровождается функциональными невротическими расстройствами, которые в дальнейшем могут стать определяющими.
Диагностика
Для диагностики необходимо провести тщательный сбор анамнеза, лабораторное и инструментальное обследование. В опросе родителей ребенка с нейрогенным мочевым пузырем выясняют, как протекали роды, имеется ли наследственная предрасположенность к заболеванию. Для исключения воспалительных заболеваний мочевыделительной системы выполняют анализ крови и мочи – общий, по Нечипоренко, функциональную пробу Зимницкого, биохимическое исследование мочи и крови.
Основными методами инструментальной диагностики синдрома являются УЗИ почек и мочевого пузыря, цистоскопия, МРТ, рентгенологическое исследование мочевыводящих путей (обычная и микционная уретроцистография, экскреторная урография, восходящая пиелография, радиоизотопная ренография), уродинамические исследования (цистометрия, сфинктерометрия, профилометрия, урофлоуметрия).
При отсутствии заболеваний со стороны мочевыделительной системы проводят неврологическое обследование для выявления патологии головного и спинного мозга с применением электроэнцефалографии, КТ, МРТ, рентгенографии черепа и позвоночника. Осуществляется дифференциальная диагностика с гипертрофией простаты, стрессовым недержанием мочи у пожилых людей. При невозможности установить причину заболевания говорят о нейрогенном мочевом пузыре с неясной этиологией (идиопатическом).
Лечение нейрогенного мочевого пузыря
Терапия проводится совместно врачом-урологом и неврологом; ее план зависит от установленной причины, типа, степени выраженности дисфункции мочевого пузыря, сопутствующей патологии (осложнений), эффективности ранее проведенного лечения. Применяют немедикаментозное, медикаментозное и хирургическое лечение, начиная с менее травматичных и более безопасных лечебных мероприятий.
Гиперактивный вариант лучше поддается лечению. Используют лекарственные средства, снижающие тонус мышц мочевого пузыря, активизирующие органное кровообращение и устраняющие гипоксию: антихолинергические препараты (гиосцин, пропантелин, оксибутинин), трициклические антидепрессанты (имипрамин), антагонисты кальция (нифедипин), альфа-адреноблокаторы (фентоламин, феноксибензамин).
В последнее время довольно перспективным в лечении гиперрефлексии, детрузорно-сфинктерной диссенергии и инфравезикальной обструкции считают применение инъекций ботулотоксина в стенку мочевого пузыря или уретры, внутрипузырное введение капсаицина и резинфератоксина. В дополнение назначают препараты на основе янтарной кислоты, L-карнитин, гопантеновая кислота, N-никотиноил-гамма-аминобутировая кислота, коферментные формы витаминов, обладающие антигипоксическим и антиоксидантным действием.
Параллельно применяют немедикаментозные методы лечения нейрогенного мочевого пузыря: лечебную физкультуру (специальные упражнения для тазовых мышц), физиотерапию (электростимуляцию, лазеротерапию, гипербарическую оксигенацию, диадинамотерапию, тепловые аппликации, ультразвук), тренировку мочевого пузыря, нормализацию режима питья и сна, психотерапию.
Гипоактивный вариант болезни труднее поддается терапии. Имеющиеся застойные явления в мочевом пузыре создают риск присоединения инфекции, развития вторичных поражений мочевой системы. В лечении нейрогенного синдрома с признаками гипотонии важно обеспечение регулярного и полного опорожнения мочевого пузыря (с помощью принудительных мочеиспусканий, наружной компрессии (прием Креде), методами физиотерапии, тренировки мышц мочевого пузыря и тазового дна, периодической или постоянной катетеризацией).
В качестве медикаментозной терапии применяют непрямые и М-холиномиметики (бетанехол хлорид, дистигмина бромид, ацеклидин, галантамин), позволяющие усиливать моторику мочевого пузыря, снижать его эффективный объем и количество остаточной мочи. Индивидуально назначают альфа-адреноблокаторы (феноксибензамин – при внутренней детрузорно-сфинктерной диссинергии, диазепам и баклофен – при внешней детрузорно-сфинктерной диссинергии), альфа-симпатомиметики (мидодрин и имипрамин – в случае недержания мочи при напряжении).
При медикаментозной терапии нейрогенного мочевого пузыря для профилактики мочевых инфекций необходимы контроль количества остаточной мочи и прием антибактериальных препаратов (нитрофуранов, сульфаниламидов), особенно пациентам с пузырно-мочеточниковым рефлюксом.
Хирургическое эндоскопическое вмешательство при гипотонии органа заключается в трансуретральной воронкообразной резекции шейки мочевого пузыря, обеспечивающей в дальнейшем возможность опорожнения слабым нажатием снаружи. При гиперрефлекторном варианте (со спастикой тазового дна и детрузорно-сфинктерной диссинергией) проводят надрез наружного сфинктера, что снижает напор мочеиспускания, а в последующем – гиперреактивность детрузора, увеличивая вместимость пузыря.
Также возможно оперативное увеличение мочевого пузыря (с использованием пластики тканей), ликвидация пузырно-мочеточникового рефлюкса, постановка цистостомического дренажа для опорожнения мочевого пузыря. Патогенетическое лечение синдрома нейрогенного мочевого пузыря позволяет уменьшить риск повреждения мочевыделительных органов и необходимость оперативного вмешательства в будущем.
Источник
Нейропатия, имеющая характерную клиническую картину, в большинстве случаев свидетельствует о наличии различных патологических состояний. В настоящее время насчитывается около 400 заболеваний, одним из проявлений которых является поражение нервных волокон. Большинство из этих заболеваний встречается довольно редко, поэтому для многих практикующих врачей основной патологией, сопровождающейся симптомами нейропатии, является сахарный диабет (СД). Он занимает одно из первых мест по частоте возникновения нейропатии в развитых странах (около 30%). Согласно различным исследованиям, диабетическая полинейропатия (ДПН) встречается у 10-100% больных с СД.
Патогенез и классификация
В патогенезе ДПН важную роль играют следующие факторы:
1. Микроангиопатия (функциональные и/или структурные изменения капилляров, отвечающих за микроциркуляцию нервных волокон).
2. Метаболические нарушения:
- Активизация полиолового шунта (альтернативный путь метаболизма глюкозы, при котором она превращается в сорбитол (с помощью фермента альдозоредуктазы) и затем во фруктозу; накопление этих метаболитов ведет к повышению осмолярности межклеточного пространства).
- Снижение уровня мио-инозитола, которое ведет к уменьшению синтеза фосфоинозитола (компонента мембран нервных клеток), способствующее в конечном итоге снижению энергетического обмена и нарушению проведения нервного импульса.
- Неферментативное и ферментативное гликирование белков (гликирование миелина и тубулина (структурных компонентов нерва) приводит к демиелинизации и нарушению проведения нервного импульса, гликирование белков базальной мембраны капилляров ведет к ее утолщению и нарушению обменных процессов в нервных волокнах).
- Усиление окислительного стресса (увеличение окисления глюкозы и липидов, снижение антиоксидантной защиты способствует накоплению свободных радикалов, обладающих прямым цитотоксическим действием).
- Выработка аутоиммунных комплексов (по некоторым данным, антитела к инсулину угнетают фактор роста нервов, что ведет к атрофии нервных волокон).
Взаимосвязь между различными факторами патогенеза ДПН показана на рисунке 1.
Классификация и основные клинические проявления ДПН
Симметричные нейропатии
Дистальная сенсорная или сенсомоторная нейропатия
С преимущественным поражением малых волокон:
- жжение или острые стреляющие боли;
- гипералгезия;
- парестезии;
- потеря болевой или температурной чувствительности;
- язвенные дефекты стоп;
- отсутствие висцеральных болей.
С преимущественным поражением больших волокон:
- потеря вибрационной чувствительности;
- потеря проприоцептивной чувствительности;
- арефлексия.
Нейропатия, обусловленная лекарственными препаратами
Гипергликемическая нейропатия
Острая болевая нейропатия
Хроническая воспалительная демиелинизирующая нейропатия
Автономная нейропатия:
- Нарушенный зрачковый рефлекс.
- Нарушение потоотделения.
- Бессимптомные гипогликемии.
- Автономная нейропатия ЖКТ:
- атония желудка;
- атония желчного пузыря;
- диабетическая энтеропатия («ночная диарея»);
- запоры;
- недержание кала.
- Автономная нейропатия сердечно-сосудистой системы:
- безболевая ишемия миокарда;
- ортостатическая гипотония;
- нарушения сердечного ритма;
- ортостатическая тахикардия;
- тахикардия покоя;
- фиксированный сердечный ритм;
- изменения циркадного ритма;
- снижение толерантности к физическим нагрузкам.
- Автономная нейропатия мочевого пузыря.
- Автономная нейропатия половой системы (эректильная дисфункция, ретроградная эякуляция).
Фокальные и мультифокальные нейропатии
Краниальная нейропатия
- Глазодвигательный нерв (III).
- Отводящий нерв (VI).
- Блоковый нерв (IV).
Асимметричная проксимальная нейропатия нижних конечностей
- Ассиметричная проксимальная моторная нейропатия.
- Боли в спине, бедрах, коленях.
- Слабость и атрофия сгибательных, приводящих и четырехглавых мышц бедер.
- Потеря рефлекса с сухожилий четырехглавых мышц.
- Небольшие сенсорные изменения.
- Снижение массы тела.
Радикулопатия
- Боль локализуется в спине, грудной клетке, животе.
- Снижение чувствительности или дизестезия.
Мононейропатия конечностей
- Компрессионная (тоннельная):
- верхняя конечность: срединный нерв в области запястного канала;
- нижняя конечность: большеберцовый нерв; малоберцовый нерв.
- Некомпрессионная.
Диагностика ДПН
1. Сбор анамнеза и жалоб больного (вопросы для определения субъективных симптомов различных форм нейропатии приведены в таблице 1).

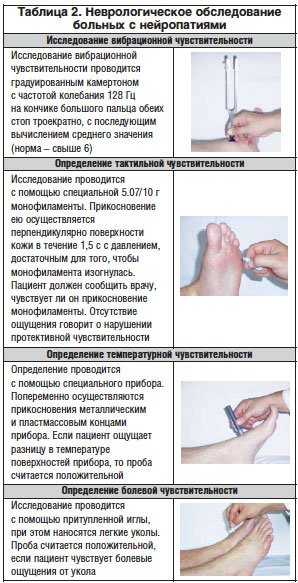
2. Неврологическое обследование (табл. 2).
Представленные в таблицах 1 и 2 тесты позволяют быстро и грамотно выявить проявления периферической ДПН. Для более детальной диагностики и выявления других форм нейропатии проводятся следующие исследования:
1. Электромиография.
2. Электрокардиография (определение вариабельности сердечного ритма, тесты с глубоким дыханием, проба Вальсальвы, проба с изменением положения тела).
3. Измерение артериального давления (проба с изменением положения тела).
4. Рентген желудка с/без контрастирования.
5. Ультразвуковое исследование брюшной полости.
6. Внутривенная урография, цистоскопия и др.
Лечение и профилактика ДПН
Основной задачей лечения и профилактики ДПН является оптимизация гликемического контроля. Многочисленные исследования, проведенные в последние годы, убедительно доказали, что достижение оптимального уровня глюкозы в крови в течение 1 сут препятствует развитию проявлений ДПН. Самое современное и грамотное лечение нейропатии будет неэффективно без стойкой компенсации СД.
Известно, что при СД имеется дефицит многих витаминов и микроэлементов, однако для лечения ДПН наиболее важную роль играет устранение дефицита витаминов группы В. Нейротропные витамины (группы В) являются коферментами, участвующими в различных биохимических процессах, улучшают энергетику нервной клетки, препятствуют образованию конечных продуктов гликирования белков. Препараты этих витаминов применялись для лечения ДПН достаточно длительное время. Однако отдельное применение каждого из витаминов группы В добавляет к лечению пациентов еще несколько инъекций или таблеток, что крайне неудобно. Препарат Нейромультивит позволяет избегать дополнительного приема многих препаратов, поскольку одна таблетка, покрытая пленочной оболочкой, уже содержит:
- тиамина гидрохлорид (витамин B1) – 100 мг;
- пиридоксина гидрохлорид (витамин B6) – 200 мг;
- цианокобаламин (витамин B12) – 0,2 мг.
Тиамин (витамин В1) в организме человека в результате процессов фосфорилирования превращается в кокарбоксилазу, которая является коферментом, участвующим во многих ферментных реакциях. Тиамин играет важную роль в углеводном, белковом и жировом обмене, активно участвует в процессах проведения нервного возбуждения в синапсах.
Пиридоксин (витамин В6) необходим для нормального функционирования центральной и периферической нервной системы. В фосфорилированной форме является коферментом, участвующим в метаболизме аминокислот (декарбоксилирование, переаминирование и др.). Выступает в качестве кофермента важнейших ферментов, действующих в нервных тканях. Участвует в биосинтезе многих нейромедиаторов, таких как допамин, норадреналин, адреналин, гистамин и γ-аминомасляная кислота.
Цианокобаламин (витамин В12) необходим для нормального кроветворения и созревания эритроцитов, также участвует в ряде биохимических реакций, обеспечивающих жизнедеятельность организма: в переносе метильных групп (и других одноуглеродистых фрагментов), в синтезе нуклеиновых кислот, белка, в обмене аминокислот, углеводов, липидов. Оказывает благоприятное влияние на процессы в нервной системе (синтез нуклеиновых кислот и липидный состав цереброзидов и фосфолипидов). Коферментные формы цианокобаламина – метилкобаламин и аденозилкобаламин необходимы для репликации и роста клеток.
Исследования состояния периферической нервной системы у больных СД 2-го типа показали, что Нейромультивит оказывает достоверно положительное влияние на тактильную и вибрационную чувствительность стоп, а также значительно уменьшает интенсивность болевого синдрома. Это позволяет говорить о снижении риска развития трофических язв стоп и повышении качества жизни больных с дистальной формой ДПН. Следует также отметить удобство проведения курса лечения в амбулаторных условиях, т. к. препарат не требует парентерального введения.
Альфа-липоевая кислота является коэнзимом ключевых ферментов цикла Кребса, что позволяет восстановить энергетический баланс нервных структур, а также антиоксидантом (будучи естественным окислителем), что дает возможность предотвратить дальнейшее повреждение нервных структур и защитить нервную ткань от воздействия свободных радикалов. Вначале, на протяжении 2-4 нед. (минимальный курс – 15, оптимально – 20) α-липоевая кислота назначается в виде ежедневных в/в капельных вливаний 600 мг/сут. В дальнейшем переходят на прием таблеток, содержащих 600 мг α-липоевой кислоты по 1 таблетке/сут в течение 1,5-2 мес.
Для лечения болевой формы ДПН к вышеперечисленным препаратам могут добавляться простые анальгетики, нестероидные противовоспалительные препараты (ацетилсалициловая кислота, парацетамол). Среди них стоит отметить препарат Нейродикловит, содержащий диклофенак и витамины группы В (В1, В6, В12), оказывающий выраженное анальгезирующее, противовоспалительное и жаропонижающее действие.
Показано применение таких групп препаратов, как трициклические антидепрессанты (амитриптиллин 25-50-100 мг на ночь), габапентин (начальная доза – 300 мг, повышение на 300 мг каждые 1-3 дня, максимальная доза – 3600 мг), прегабалин (начальная доза – 150 мг, повышение до 300 мг через 3-7 дней, максимальная доза – 600 мг (делится на 2-3 приема)), дулоксетин (начальная доза – 60 мг 1 р./сут, иногда повышение до 60 мг 2 р./сут, максимальная доза – 120 мг).
Для лечения автономной нейропатии ЖКТ используются:
- при атонии желудка: цизаприд (5-40 мг 2-4 р./сут за 15 мин до еды), метоклопрамид (5-10 мг 3-4 р./сут), домперидон (10 мг 3 р./сут);
- при энтеропатии (диарее): лоперамид (первая доза – 2 мг, далее 2-12 мг/сут до частоты стула 1-2 р./сут, но не более 6 мг на каждые 20 кг веса больного в 1 сут).
Для лечения автономной нейропатии сердечно-сосудистой системы (тахикардии покоя) применяются кардиоселективные β-блокаторы, блокаторы кальциевых каналов (например, верапамил, Дилтиазем Ланнахер).
Для лечения эректильной дисфункции применяются ингибиторы фосфодиэстеразы 5-го типа (если нет противопоказаний), интракавернозное введение алпростадила, протезирование, психологическое консультирование.
Для общей профилактики гиповитаминоза и осложнений больным СД назначаются поливитаминные препараты. В этом случае также эффективно назначение витминов группы В в терапевтических дозировках (Нейромультивит).
Источник
